铬铁矿的主要成分可表示为FeO•Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:

已知:① Na2CO3+Al2O3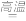 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
② Cr2O72 -+ H2O 2CrO42-+2H+
2CrO42-+2H+
根据题意回答下列问题:
(1)请完成下列化学方程式的配平:
____ FeO•Cr2O3 + ___ Na2CO3 + ___ O2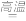
___ Na2CrO4 + ___ Fe2O3 + ____ CO2↑;
(2)固体X的主要成分是_______ .
(3)酸化步骤用醋酸调节溶液pH<5,其目的是__________ ;
(4)操作Ⅲ由多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、_______ 、过滤、______ 、干燥;
(5)某种酒精测试仪中,K2Cr2O7在酸性条件下将乙醇氧化成乙醛,自身被还原为三价铬离子。
该反应的离子方程式为______________________________________________

已知:① Na2CO3+Al2O3
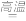 2NaAlO2+CO2↑;
2NaAlO2+CO2↑; ② Cr2O72 -+ H2O
 2CrO42-+2H+
2CrO42-+2H+根据题意回答下列问题:
(1)请完成下列化学方程式的配平:
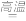
(2)固体X的主要成分是
(3)酸化步骤用醋酸调节溶液pH<5,其目的是
(4)操作Ⅲ由多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、
(5)某种酒精测试仪中,K2Cr2O7在酸性条件下将乙醇氧化成乙醛,自身被还原为三价铬离子。
该反应的离子方程式为
更新时间:2016-12-09 16:06:33
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出),请回答下列问题:
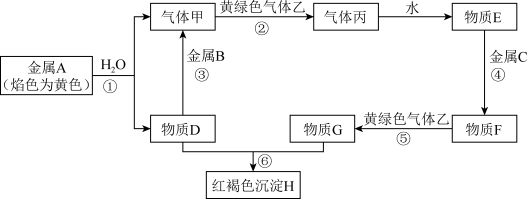
(1)写出下列物质的化学式:B___________ 、乙___________ 。
(2)写出下列反应的化学方程式:
反应①___________ ;
反应③___________ ;
(3)如果要检验物质G中的金属阳离子,最好选择下列哪种试剂___________
A. B.
B. C.
C. D.
D.
用所选择的试剂检验时,可观察到的现象:___________ 。

(1)写出下列物质的化学式:B
(2)写出下列反应的化学方程式:
反应①
反应③
(3)如果要检验物质G中的金属阳离子,最好选择下列哪种试剂
A.
 B.
B. C.
C. D.
D.
用所选择的试剂检验时,可观察到的现象:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】为将某部分被氧化的废铜屑[主要含Cu、CuO、 ]转化为铜单质,同时制备绿矾(
]转化为铜单质,同时制备绿矾( ),某实验小组设计如图所示流程.
),某实验小组设计如图所示流程.

回答下列问题:
(1)“浸泡”时,Cu发生反应的离子方程式为______ , 的作用为
的作用为______ .
(2)“滤液1”中所含溶质的主要成分为______ .
(3)“分铜”时的操作名称是______ .
(4)“滤液2”容易被空气中的氧气氧化,长时间保存“滤液2”时需向其中加入一定量______ .
(5)向“滤液2”中滴加NaOH溶液,观察到的实验现象为______ ;发生反应的化学方程式为______ 和______ .
 ]转化为铜单质,同时制备绿矾(
]转化为铜单质,同时制备绿矾( ),某实验小组设计如图所示流程.
),某实验小组设计如图所示流程.
回答下列问题:
(1)“浸泡”时,Cu发生反应的离子方程式为
 的作用为
的作用为(2)“滤液1”中所含溶质的主要成分为
(3)“分铜”时的操作名称是
(4)“滤液2”容易被空气中的氧气氧化,长时间保存“滤液2”时需向其中加入一定量
(5)向“滤液2”中滴加NaOH溶液,观察到的实验现象为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
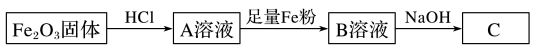
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色:A_________ ,B_________ 。
(2)写出上述过程中有关反应的化学方程式: →A
→A_________ ,A→B_________ 。
(3)向B溶液中逐滴加入NaOH得到C,此过程中可观察到的现象是_________ 。
(4)将A的饱和溶液滴入沸水中并不断加热,可制得_________ 胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为_________ 。
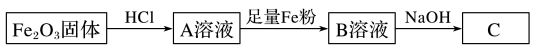
(1)往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色:A
(2)写出上述过程中有关反应的化学方程式:
 →A
→A(3)向B溶液中逐滴加入NaOH得到C,此过程中可观察到的现象是
(4)将A的饱和溶液滴入沸水中并不断加热,可制得
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】乙酰苯胺(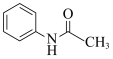 )作为一种常用药,具有解热镇痛的效果。乙酰苯胺可通过苯胺(
)作为一种常用药,具有解热镇痛的效果。乙酰苯胺可通过苯胺(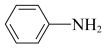 )和冰醋酸反应制得,该反应是放热的可逆反应。
)和冰醋酸反应制得,该反应是放热的可逆反应。
已知:I.苯胺在空气中易被氧化。
Ⅱ.可能用到的有关性质如表:
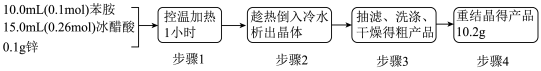
制备乙酰苯胺的具体流程如图:
(1)写出制备乙酰苯胺的化学方程式_____ 。
(2)加入的冰醋酸要过量的目的是_____ 。
(3)步骤1所用装置如图所示。_____ (填“A”、“B”或“C”),该仪器的名称是_____ 。
②反应体系的温度控制在100℃~105℃,目的是_____ 。
(4)步骤3中洗涤乙酰苯胺粗产品最合适的试剂是_____ (填标号)。
(5)步骤4中重结晶的过程:粗产品溶于沸水中配成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→_____ →冷却结晶→过滤→洗涤→干燥。
 )作为一种常用药,具有解热镇痛的效果。乙酰苯胺可通过苯胺(
)作为一种常用药,具有解热镇痛的效果。乙酰苯胺可通过苯胺( )和冰醋酸反应制得,该反应是放热的可逆反应。
)和冰醋酸反应制得,该反应是放热的可逆反应。已知:I.苯胺在空气中易被氧化。
Ⅱ.可能用到的有关性质如表:
| 名称 | 熔点/℃ | 沸点/℃ | 溶解度/g(20℃) | |
| 水 | 乙醇 | |||
| 苯胺 | -6.3 | 184 | 3.4 | 任意比混合 |
| 冰醋酸 | 16.6 | 118 | 任意比混合 | 任意比混合 |
| 乙酰苯胺 | 114.3 | 304 | 0.46 | 36.9 |
| (温度高溶解度大) | ||||
(1)写出制备乙酰苯胺的化学方程式
(2)加入的冰醋酸要过量的目的是
(3)步骤1所用装置如图所示。
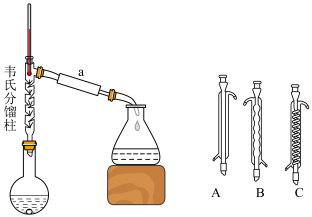
②反应体系的温度控制在100℃~105℃,目的是
(4)步骤3中洗涤乙酰苯胺粗产品最合适的试剂是
| A.冰水 | B.热水 | C.15%的乙醇溶液 | D.NaOH溶液 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】实验室利用橄榄石尾矿(主要成分为MgO及少量FeO、Fe2O3、Al2O3等)制备纯净氯化镁晶体(MgCl2·6H2O),实验流程如下:

已知几种金属阳离子形成氢氧化物沉淀时的pH如下表:
回答下列问题:
(1)“浸取”步骤中,能加快浸取速率的方法有____ (任写一种)。
(2)滤渣1为Fe(OH)3,则调节pH的范围为____ 。
(3)“一系列操作”主要包括加入足量盐酸,然后经过蒸发浓缩、冷却结晶、过滤、洗涤,即得到氯化镁晶体。加入足量 盐酸的作用为①溶解滤渣2,②____ 。
(4)准确称取2.000 g氯化镁晶体产品于250 mL锥形瓶中,加50 mL蒸馏水使其完全溶解,在不断振荡下,调节pH并加入合适的指示剂,用0.5000 mol/L的EDTA(在方程式中用Y4−表示)标准溶液进行滴定,其反应原理为Mg2++Y4− = MgY2−,滴定达到终点时消耗EDTA标准溶液的体积为19.00 mL。
①计算产品中MgCl2·6H2O的质量分数。____ (写出计算过程,结果保留三位有效数字)。
②下列滴定操作会导致测量结果偏高的是____ (填字母)。
a.滴定终点时仰视读数
b.锥形瓶洗涤后没有干燥
c.滴定时锥形瓶中有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后气泡消失

已知几种金属阳离子形成氢氧化物沉淀时的pH如下表:
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时 | 7.6 | 2.7 | 4.2 | 9.6 |
| 沉淀完全时 | 9.6 | 3.7 | 5.4 | 11.1 |
回答下列问题:
(1)“浸取”步骤中,能加快浸取速率的方法有
(2)滤渣1为Fe(OH)3,则调节pH的范围为
(3)“一系列操作”主要包括加入足量盐酸,然后经过蒸发浓缩、冷却结晶、过滤、洗涤,即得到氯化镁晶体。加入
(4)准确称取2.000 g氯化镁晶体产品于250 mL锥形瓶中,加50 mL蒸馏水使其完全溶解,在不断振荡下,调节pH并加入合适的指示剂,用0.5000 mol/L的EDTA(在方程式中用Y4−表示)标准溶液进行滴定,其反应原理为Mg2++Y4− = MgY2−,滴定达到终点时消耗EDTA标准溶液的体积为19.00 mL。
①计算产品中MgCl2·6H2O的质量分数。
②下列滴定操作会导致测量结果偏高的是
a.滴定终点时仰视读数
b.锥形瓶洗涤后没有干燥
c.滴定时锥形瓶中有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后气泡消失
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】三氯氧磷( )和氯化亚砜(
)和氯化亚砜( )均为重要的化工产品。现以氯气、二氧化硫和三氯化磷为原料,采用二级间歇式反应装置联合制备三氯氧磷和氯化亚砜。实验过程中,控制氯气和二氧化硫通入的体积比为1:1,实验过程示意图如图:
)均为重要的化工产品。现以氯气、二氧化硫和三氯化磷为原料,采用二级间歇式反应装置联合制备三氯氧磷和氯化亚砜。实验过程中,控制氯气和二氧化硫通入的体积比为1:1,实验过程示意图如图:
(1)实验室制备氯气或二氧化硫时均可能用到的仪器有_______。
(2)A装置的作用为:_______ 、______ 、使气体充分混合。
(3)B中发生反应的化学方程式是__________ ,反应结束后,B瓶中的物质可采用_______ (填实验方法)使其分离。
(4)实验开始时需水浴加热,一段时间后改为冷水浴,其原因是_________ 。
(5)反应5~6小时后,暂停通入气体。将B瓶拆下,C瓶装在图中B瓶处,并在原C瓶处重新装上一个盛有 的圆底烧瓶。继续通气反应一段时间后重复以上步骤,上述操作的优点是
的圆底烧瓶。继续通气反应一段时间后重复以上步骤,上述操作的优点是________ 。
(6)已知反应前加入三氯化磷 ,最终得到
,最终得到 氯化亚砜,则三氯氧磷的产率为
氯化亚砜,则三氯氧磷的产率为________ 。
 )和氯化亚砜(
)和氯化亚砜( )均为重要的化工产品。现以氯气、二氧化硫和三氯化磷为原料,采用二级间歇式反应装置联合制备三氯氧磷和氯化亚砜。实验过程中,控制氯气和二氧化硫通入的体积比为1:1,实验过程示意图如图:
)均为重要的化工产品。现以氯气、二氧化硫和三氯化磷为原料,采用二级间歇式反应装置联合制备三氯氧磷和氯化亚砜。实验过程中,控制氯气和二氧化硫通入的体积比为1:1,实验过程示意图如图:
| 名称 | 熔点/℃ | 沸点/℃ | 溶解性 | 理化性质 |
| 三氯氧磷 | 2 | 105.3 | 可溶于有机溶剂 | 遇水分解 |
| 氯化亚砜 | 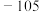 | 78.8 | 可溶于有机溶剂 | 遇水分解,加热分解 |
(1)实验室制备氯气或二氧化硫时均可能用到的仪器有_______。
| A.温度计 | B.酒精灯 | C.牛角管 | D.圆底烧瓶 |
(2)A装置的作用为:
(3)B中发生反应的化学方程式是
(4)实验开始时需水浴加热,一段时间后改为冷水浴,其原因是
(5)反应5~6小时后,暂停通入气体。将B瓶拆下,C瓶装在图中B瓶处,并在原C瓶处重新装上一个盛有
 的圆底烧瓶。继续通气反应一段时间后重复以上步骤,上述操作的优点是
的圆底烧瓶。继续通气反应一段时间后重复以上步骤,上述操作的优点是(6)已知反应前加入三氯化磷
 ,最终得到
,最终得到 氯化亚砜,则三氯氧磷的产率为
氯化亚砜,则三氯氧磷的产率为
您最近一年使用:0次



