质量之比为16:7:6的三种气体SO2、CO、NO,分子数之比为_____________ ,氧原子数之比为_____________ ,相同条件下的体积之比为_____________ 。
更新时间:2016-12-09 16:07:06
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)物质的量相等的 CO 和 CO2 中,同温同压下所占的体积比为____ ,原子个数之比为______ ;
(2)1.8g水与_______ mol硫酸所含的分子数相等,它们所含氧原子数之比是________ ,其中氢原子数之比是___________ 。
(3)3.2g某气体中含有的分子数约为3.01×1022,此气体的摩尔质量为________ 。
(4)可用于分离或提纯物质的方法有:
A 过滤 B 萃取 C 渗析 D 蒸馏 E 灼热氧化 F 分液.
如欲分离或提纯下列各组混合物,请选择上述方法中最合适者,并将相应字母填入题后空格内:
①除去淀粉溶液中的少量碘化钠________ ; ②提取溴水中的溴单质______ ;
③除去水中的Na+、 、Cl-等杂质
、Cl-等杂质________ ; ④除去CuO中的Cu ______ ;
(2)1.8g水与
(3)3.2g某气体中含有的分子数约为3.01×1022,此气体的摩尔质量为
(4)可用于分离或提纯物质的方法有:
A 过滤 B 萃取 C 渗析 D 蒸馏 E 灼热氧化 F 分液.
如欲分离或提纯下列各组混合物,请选择上述方法中最合适者,并将相应字母填入题后空格内:
①除去淀粉溶液中的少量碘化钠
③除去水中的Na+、
 、Cl-等杂质
、Cl-等杂质
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】简要回答或计算。
(1)Bi2Cl 离子中铋原子的配位数为5,配体呈四角锥型分布,画出该离子的结构并指出Bi原子的杂化轨道类型
离子中铋原子的配位数为5,配体呈四角锥型分布,画出该离子的结构并指出Bi原子的杂化轨道类型______ 。
(2)在液氨中,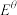 (Na+/Na)=-1.89V,
(Na+/Na)=-1.89V,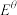 (Mg2++Mg)=-1.74V,但可以发生Mg置换Na的反应:Mg+2NaI=MgI2+2Na。指出原因
(Mg2++Mg)=-1.74V,但可以发生Mg置换Na的反应:Mg+2NaI=MgI2+2Na。指出原因_______ 。
(3)将Pb加到氨基钠的液氨溶液中,先生成白色沉淀Na4Pb,随后转化为Na4Pb9(绿色)而溶解。在此溶液中插入两块铅电极,通直流电,当1.0mol电子通过电解槽时,在哪个电极(阴极或阳极)上沉积出铅____ ?写出沉积铅的量____ 。
(4)下图是某金属氧化物的晶体结构示意图。图中,小球代表金属原子,大球代表氧原子,细线框处是其晶胞。
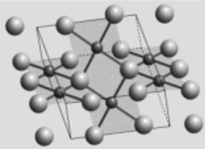
①写出金属原子的配位数(m)和氧原子的配位数(n):_______ 。
②写出晶胞中金属原子数(p)和氧原子数(q):________ 。
③写出该金属氧化物的化学式(金属用M表示)__________ 。
(5)向含[cis-Co(NH3)4(H2O)2]3+的溶液中加入氨水,析出含{Co[Co(NH3)4(OH)2]3}6+的难溶盐。{Co[Co(NH3)4(OH)2]3}6+是以羟基为桥键的多核络离子,具有手性。画出其结构____________ 。
(6)向K2Cr2O7和NaCl的混合物中加入浓硫酸制得化合物X(154.9g·mol-1)。X为暗红色液体,沸点117°C,有强刺激性臭味,遇水冒白烟,遇硫燃烧。X分子有两个相互垂直的镜面,两镜面的交线为二重旋转轴。写出X的化学式并画出其结构式___________ 。
(7)实验得到一种含钯化合物Pd[CxHyNz](ClO4)2,该化合物中C和H的质量分数分别为30.15%和5.06%。将此化合物转化为硫氰酸盐Pd[CxHyNz](SCN)2,则C和H的质量分数分别为40.46%和5.94%。通过计算确定Pd[CxHyNz](ClO4)2的组成___________ 。
(8)甲烷在汽车发动机中平稳、完全燃烧是保证汽车安全和高能效的关键。甲烷与空气按一定比例混合,氧气的利用率为85%,计算汽车尾气中O2、CO2、H2O和N2的体积比________ 。(空气中O2和N2体积比按21:79计;设尾气中CO2的体积为1)。
(1)Bi2Cl
 离子中铋原子的配位数为5,配体呈四角锥型分布,画出该离子的结构并指出Bi原子的杂化轨道类型
离子中铋原子的配位数为5,配体呈四角锥型分布,画出该离子的结构并指出Bi原子的杂化轨道类型(2)在液氨中,
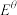 (Na+/Na)=-1.89V,
(Na+/Na)=-1.89V,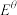 (Mg2++Mg)=-1.74V,但可以发生Mg置换Na的反应:Mg+2NaI=MgI2+2Na。指出原因
(Mg2++Mg)=-1.74V,但可以发生Mg置换Na的反应:Mg+2NaI=MgI2+2Na。指出原因(3)将Pb加到氨基钠的液氨溶液中,先生成白色沉淀Na4Pb,随后转化为Na4Pb9(绿色)而溶解。在此溶液中插入两块铅电极,通直流电,当1.0mol电子通过电解槽时,在哪个电极(阴极或阳极)上沉积出铅
(4)下图是某金属氧化物的晶体结构示意图。图中,小球代表金属原子,大球代表氧原子,细线框处是其晶胞。

①写出金属原子的配位数(m)和氧原子的配位数(n):
②写出晶胞中金属原子数(p)和氧原子数(q):
③写出该金属氧化物的化学式(金属用M表示)
(5)向含[cis-Co(NH3)4(H2O)2]3+的溶液中加入氨水,析出含{Co[Co(NH3)4(OH)2]3}6+的难溶盐。{Co[Co(NH3)4(OH)2]3}6+是以羟基为桥键的多核络离子,具有手性。画出其结构
(6)向K2Cr2O7和NaCl的混合物中加入浓硫酸制得化合物X(154.9g·mol-1)。X为暗红色液体,沸点117°C,有强刺激性臭味,遇水冒白烟,遇硫燃烧。X分子有两个相互垂直的镜面,两镜面的交线为二重旋转轴。写出X的化学式并画出其结构式
(7)实验得到一种含钯化合物Pd[CxHyNz](ClO4)2,该化合物中C和H的质量分数分别为30.15%和5.06%。将此化合物转化为硫氰酸盐Pd[CxHyNz](SCN)2,则C和H的质量分数分别为40.46%和5.94%。通过计算确定Pd[CxHyNz](ClO4)2的组成
(8)甲烷在汽车发动机中平稳、完全燃烧是保证汽车安全和高能效的关键。甲烷与空气按一定比例混合,氧气的利用率为85%,计算汽车尾气中O2、CO2、H2O和N2的体积比
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】近期,我国科学家通过将电催化与生物合成相结合,成功实现了利用二氧化碳为原料合成葡萄糖,相关的研究成果以封面文章的形式发表在《NatureCatalysis》期刊。这项研究让人工可控合成“粮食”成为可能。
(1)常温常压下,用等质量的a.H2、b.CO2、c.O2、d.Cl2四种气体分别吹出四个气球,请按照气球体积由大到小排列的顺序是_____ (填序号)。
(2)如表的体检报告中表示葡萄糖指标的物理量是_____ 。如果某人的血糖(血液中的葡萄糖)检测结果为60mg/dL,参照如图体检报告中的相关标准,他的血糖____ (填“偏高”“正常”或“偏低”)【葡萄糖分子式:C6H12O6】
(3)一袋250mL规格的医用葡萄糖注射液含葡萄糖25g,在实验室准确配制一份这样的葡萄糖溶液,需用到的玻璃仪器有:烧杯、玻璃棒、_____ 、_____ 、细口瓶。
(4)如图为二氧化碳合成高能量长链食物分子示意图。在合成过程的某一阶段中,O2、CH4和CO组成的混合气体在同温同压下与氮气的密度相同,此时混合气体中O2、CH4和CO的体积可能为_____ (填序号)。
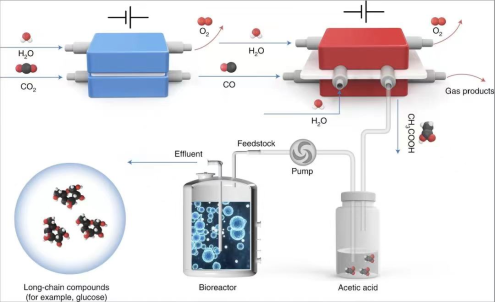
(5)向含有NaOH和Ca(OH)2的混合溶液中缓缓通入CO2直到过量。其现象为:______ ;请按照先后顺序写出相应生成盐的化学式:①_____ 、②_____ 、③_____ 、④_____ 。
(1)常温常压下,用等质量的a.H2、b.CO2、c.O2、d.Cl2四种气体分别吹出四个气球,请按照气球体积由大到小排列的顺序是
| 序号 | 项目名称 | 英文缩写 | 检查结果 | 单位 | 参考单位 |
| 1 | *钾 | K | 4.1 | mmol/L | 3.5-5.5 |
| 2 | *钠 | Na | 140 | mmol/L | 135-145 |
| 3 | 胱抑素 | CyaC | 0.78 | mg/L | 0.59-1.03 |
| 4 | *尿素 | Urea | 4.18 | mmol/L | 2.78-7.14 |
| 5 | *葡萄糖 | Glu | 5.1 | mmol/L | 3.9-6.1 |
| 6 | *无机磷 | P | 1.19 | mmol/L | 0.81-1.45 |
| 7 | *总胆固醇 | TC | 4.65 | mmol/L | 2.85-5.70 |
| 8 | *甘油三酯 | TG | 1.50 | mmol/L | 0.45-1.70 |
| 9* | 高密度脂蛋白胆固醇 | HDL-V | 1.08 | mmol/L | 0.93-1.83 |
(2)如表的体检报告中表示葡萄糖指标的物理量是
(3)一袋250mL规格的医用葡萄糖注射液含葡萄糖25g,在实验室准确配制一份这样的葡萄糖溶液,需用到的玻璃仪器有:烧杯、玻璃棒、
(4)如图为二氧化碳合成高能量长链食物分子示意图。在合成过程的某一阶段中,O2、CH4和CO组成的混合气体在同温同压下与氮气的密度相同,此时混合气体中O2、CH4和CO的体积可能为

| A.9:3:7 | B.6:5:15 | C.27:9:29 | D.7:4:12 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】为测定某抗胃酸药片中碳酸钙的质量分数(设该药片中的其他成分不与盐酸或氢氧化钠反应):
I.向0.1000 g药片粉末中依次加入20.00 mL蒸馏水、25.00 mL 0.1000 mol/L稀盐酸,使之充分反应。
II.中和过量的盐酸,消耗0.1000 mol/L NaOH溶液13.00 mL。
请计算:
(1)II中消耗NaOH的物质的量为_______ mol。
(2)0.1000 g药片消耗HCl的物质的量为_______ mol。
(3)药片中碳酸钙的质量分数为_______ 。
I.向0.1000 g药片粉末中依次加入20.00 mL蒸馏水、25.00 mL 0.1000 mol/L稀盐酸,使之充分反应。
II.中和过量的盐酸,消耗0.1000 mol/L NaOH溶液13.00 mL。
请计算:
(1)II中消耗NaOH的物质的量为
(2)0.1000 g药片消耗HCl的物质的量为
(3)药片中碳酸钙的质量分数为
您最近一年使用:0次
【推荐2】有10种物质:①液态氯化氢②乙醇③熔融的KNO3④铜线⑤Na2O固体⑥氨水⑦NaHCO3溶液⑧醋酸⑨NaOH溶液⑩BaCl2溶液
(1)属于电解质的是___________ ;属于非电解质的有___________ ;能导电的是___________ 。
(2)用电子式表示⑤的形成过程___________ 。
(3)写出⑦中溶质的电离方程式___________ 。
(4)写出⑧在水溶液中的电离方程式___________ 。
(5)写出⑦和⑨反应的离子方程式___________ 。
(6)用10mL0.1mol·L-1的⑩恰好使相同体积的Fe2(SO4)3、ZnSO4和KAl(SO4)2三种溶液中的硫酸根离子完全转化为硫酸钡沉淀。则三种硫酸盐溶液的物质的量浓度之比是___________ 。
(7)已知亚磷酸H3PO3是二元弱酸,其与足量⑨反应后的产物为水和___________ 。
(1)属于电解质的是
(2)用电子式表示⑤的形成过程
(3)写出⑦中溶质的电离方程式
(4)写出⑧在水溶液中的电离方程式
(5)写出⑦和⑨反应的离子方程式
(6)用10mL0.1mol·L-1的⑩恰好使相同体积的Fe2(SO4)3、ZnSO4和KAl(SO4)2三种溶液中的硫酸根离子完全转化为硫酸钡沉淀。则三种硫酸盐溶液的物质的量浓度之比是
(7)已知亚磷酸H3PO3是二元弱酸,其与足量⑨反应后的产物为水和
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】计算题:
(1)一定量的H2和Cl2充分燃烧后,将反应生成的气体通入100mL1.0mol/L的NaOH溶液中,两者恰好完全反应,生成NaClO为0.01mol。则燃烧前H2和Cl2的物质的量之比为___ 。
(2)将标准状况下的HCl气体4.48L溶于水形成100mL溶液,然后与足量的铁屑充分反应。回答下列问题:
①参加反应的铁的质量为___ 。
②生成H2的体积(标准状况)为___ 。
③取反应后的溶液10mL,其中FeCl2的物质的量浓度为___ ;溶液中Fe2+和Cl-的质量比为___ 。
(1)一定量的H2和Cl2充分燃烧后,将反应生成的气体通入100mL1.0mol/L的NaOH溶液中,两者恰好完全反应,生成NaClO为0.01mol。则燃烧前H2和Cl2的物质的量之比为
(2)将标准状况下的HCl气体4.48L溶于水形成100mL溶液,然后与足量的铁屑充分反应。回答下列问题:
①参加反应的铁的质量为
②生成H2的体积(标准状况)为
③取反应后的溶液10mL,其中FeCl2的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求完成下列填空:
(1)已知在标准状况下的四种气体①6.72LCH4;②3.01×1023个HCl分子;③13.6克H2S;④0.2molNH3 用相应的序号填写下列空白:
体积最大的是_________ ;质量最小的是_________ ;含氢原子数最多的是_________ 。
(2)等物质的量的氧气与臭氧质量之比为_______ , 分子个数之比为__________ ,氧原子个数之比为_____________ 。
(3)某金属氯化物MCl3 26.7 g,含有0.600mol Cl-。则金属M的摩尔质量为__________ 。
(4)现有10克由2H和16O组成的水分子,其中含质子数为___________ mol, 中子数为___________ mol 。
(1)已知在标准状况下的四种气体①6.72LCH4;②3.01×1023个HCl分子;③13.6克H2S;④0.2molNH3 用相应的序号填写下列空白:
体积最大的是
(2)等物质的量的氧气与臭氧质量之比为
(3)某金属氯化物MCl3 26.7 g,含有0.600mol Cl-。则金属M的摩尔质量为
(4)现有10克由2H和16O组成的水分子,其中含质子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】甲烷(CH4)是一种高效清洁能源,见天然气的主要成分。2017年我国在南海海域首次发现裸露的可燃冰,可燃冰是天然气水合物晶体,假设可燃冰的水笼里装的都是甲烷,理想的甲烷水合物的化学式为CH4·8H2O。请回答下列问题:
(1)甲烷水合物(CH4·8H2O)的摩尔质量为___________ ,其中质量分数最大的元素为___________ (填元素符号)。
(2)含有4.214×1024个氢原子的CH4的物质的量为___________ mol,质量为___________ g
(3)含0.2NA个氢原子的CH4,在标准状况下的体积约为___________ L
(4)常温常压下,等质量的CH4和H2的体积之比V(CH4):V(H2)=___________ ,前者所含氢原子个数与后者所含氢原子个数之比为___________
(1)甲烷水合物(CH4·8H2O)的摩尔质量为
(2)含有4.214×1024个氢原子的CH4的物质的量为
(3)含0.2NA个氢原子的CH4,在标准状况下的体积约为
(4)常温常压下,等质量的CH4和H2的体积之比V(CH4):V(H2)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列各题:
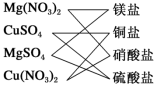
(1)如图所示的分类方法属于___________(填字母)。
(2)碱式碳酸铜[Cu2(OH)2CO3]可以看作是Cu(OH)2和CuCO3按照1∶1组成的混合型化合物,写出它与足量盐酸反应的化学方程式:___________ 。
(3)设NA为阿伏加德罗常数,标准状况下某种O2和N2的混合气体m g含有b个分子,则n g该混合气体在相同状况下所占的体积应是___________ L。
(4)0.01 mol某气体的质量为0.28 g,该气体的摩尔质量为___________ ,标准状况下该气体的体积是___________ L。
(5)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为___________ 。

(1)如图所示的分类方法属于___________(填字母)。
| A.交叉分类法 | B.树状分类法 |
(3)设NA为阿伏加德罗常数,标准状况下某种O2和N2的混合气体m g含有b个分子,则n g该混合气体在相同状况下所占的体积应是
(4)0.01 mol某气体的质量为0.28 g,该气体的摩尔质量为
(5)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
您最近一年使用:0次



