硼氢化钠(NaBH4)为白色粉末,容易吸水潮解,可溶于异丙胺(熔点:-101℃,沸点:33℃),在干空气中稳定,在湿空气中分解,是无机合成和有机合成中常用的选择性还原剂.某研究小组采用偏硼酸钠(NaBO2)为主要原料制备NaBH4,其流程如下:
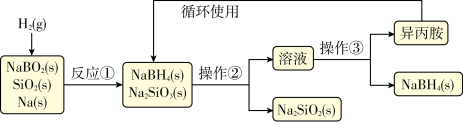
下列说法不正确的是( )

下列说法不正确的是( )
| A.实验室中取用少量钠需要用到的实验用品有镊子、滤纸、玻璃片和小刀 |
| B.操作②、操作③分别是过滤与蒸发结晶 |
| C.反应①加料之前需将反应器加热至100℃以上并通入氩气 |
| D.反应①中氧化剂与还原剂的物质的量之比为1:2 |
更新时间:2016-07-12 19:56:38
|
相似题推荐
单选题
|
困难
(0.15)
名校
【推荐1】将一定量的锌、镁合金与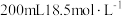 浓硫酸充分反应后,固体完全溶解,同时生成气体
浓硫酸充分反应后,固体完全溶解,同时生成气体 (生成气体全部逸出,测定条件为标准状况)。将反应后的溶液稀释到
(生成气体全部逸出,测定条件为标准状况)。将反应后的溶液稀释到 ,测得稀释后溶液中的
,测得稀释后溶液中的 浓度为
浓度为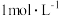 。向反应后的溶液中加入
。向反应后的溶液中加入 溶液
溶液 时,所得沉淀质量最大,其质量为
时,所得沉淀质量最大,其质量为 。下列叙述中错误的是
。下列叙述中错误的是
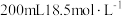 浓硫酸充分反应后,固体完全溶解,同时生成气体
浓硫酸充分反应后,固体完全溶解,同时生成气体 (生成气体全部逸出,测定条件为标准状况)。将反应后的溶液稀释到
(生成气体全部逸出,测定条件为标准状况)。将反应后的溶液稀释到 ,测得稀释后溶液中的
,测得稀释后溶液中的 浓度为
浓度为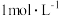 。向反应后的溶液中加入
。向反应后的溶液中加入 溶液
溶液 时,所得沉淀质量最大,其质量为
时,所得沉淀质量最大,其质量为 。下列叙述中错误的是
。下列叙述中错误的是A.气体A中 和 和 的体积比为 的体积比为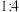 | B.该合金中锌、镁的物质的量之比为 |
C.该实验所有 的浓度是 的浓度是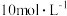 | D.沉淀质量最大时,溶液中所含溶质的质量为 |
您最近一年使用:0次
【推荐2】二氧化氯(ClO2)是一种安全消毒剂,有强氧化性,易溶于水,沸点为11℃,在空气中体积分数超过10%时有爆炸性。工业上利用硫铁矿[主要成分为(FeS2)]还原氯酸钠(NaClO3)制取ClO2。利用下图装置模拟工业制备ClO2:向三颈烧瓶中加入NaClO3溶液、浓H2SO4并通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿。
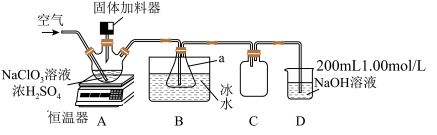
实验结束后,装置D中检测到含氯微粒有Cl-、ClO 和ClO
和ClO ,下列说法正确的是
,下列说法正确的是

实验结束后,装置D中检测到含氯微粒有Cl-、ClO
 和ClO
和ClO ,下列说法正确的是
,下列说法正确的是| A.35ClO2与37ClO2之间互为同位素 |
| B.若不考虑其他反应,装置D溶液可吸收0.2molClO2 |
C.反应后溶液中Cl-和ClO 的物质的量之比等于1:5 的物质的量之比等于1:5 |
D.反应后溶液中一定存在n(Na+)=n(Cl-)+n(ClO )+n(ClO )+n(ClO ) ) |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐1】通过CH4超干重整CO2技术可得到富含CO的化工原料,其过程如下图所示。下列说法错误的是( )
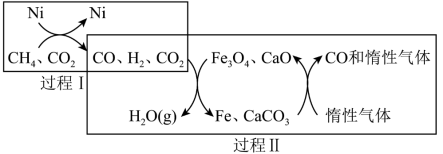
A.过程Ⅰ的化学方程式为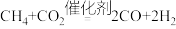 |
B.过程Ⅱ的化学方程式为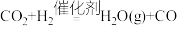 |
| C.该技术实现了含碳物质与含氢物质的分离 |
| D.Ni、Fe、CaCO3均是上述过程中用到的催化剂 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐2】从含有KI、KNO3等成分的工业废水中回收I2和KNO3,其流程如下:
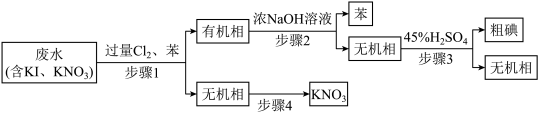
下列说法错误的是

下列说法错误的是
| A.流程中至少发生了5个氧化还原反应 |
| B.步骤1中应将无机相从分液漏斗下端放出 |
| C.步骤3需使用蒸馏烧瓶、温度计、冷凝管 |
| D.步骤4为蒸发浓缩、降温结晶、过滤 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐3】工业上以铝土矿(主要成分 Al2O3·3H2O) 为原料生产铝, 主要包括下列过程:
ⅰ. 将粉碎、 筛选、 湿磨后的铝土矿浸泡在氢氧化钠溶液中, 过滤;
ⅱ. 通入过量二氧化碳使ⅰ所得滤液中析出氢氧化铝固体, 过滤;
ⅲ. 使ⅱ中所得氢氧化铝脱水生成氧化铝;
ⅳ. 电解熔融氧化铝生成铝。 下列说法正确的是
ⅰ. 将粉碎、 筛选、 湿磨后的铝土矿浸泡在氢氧化钠溶液中, 过滤;
ⅱ. 通入过量二氧化碳使ⅰ所得滤液中析出氢氧化铝固体, 过滤;
ⅲ. 使ⅱ中所得氢氧化铝脱水生成氧化铝;
ⅳ. 电解熔融氧化铝生成铝。 下列说法正确的是
| A.过程ⅰ说明氧化铝具有酸性氧化物的性质 |
| B.过程ⅱ说明碳酸的酸性比氢氧化铝的酸性弱 |
| C.过程ⅲ发生的反应类型属于氧化还原反应 |
| D.过程ⅳ也可以用热分解法代替电解法冶炼铝 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
解题方法
【推荐1】某工厂采用辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制备
)联合焙烧法制备 ,工艺流程如图所示。焙烧时过量的
,工艺流程如图所示。焙烧时过量的 分解为
分解为 ,下列说法错误的是
,下列说法错误的是

 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制备
)联合焙烧法制备 ,工艺流程如图所示。焙烧时过量的
,工艺流程如图所示。焙烧时过量的 分解为
分解为 ,下列说法错误的是
,下列说法错误的是
A. 和 和 联合焙烧转化为 联合焙烧转化为 、 、 |
B.水浸所得滤液的主要成分是 |
C.酸浸所得滤渣的主要成分是 ,气体A为 ,气体A为 |
D.向酸浸滤液中加入金属Bi的目的是消耗 ,促进 ,促进 水解 水解 |
您最近一年使用:0次
【推荐2】二氧化氯(ClO2)是一种安全消毒剂,有强氧化性,易溶于水,沸点为11℃,在空气中体积分数超过10%时有爆炸性。工业上利用硫铁矿[主要成分为(FeS2)]还原氯酸钠(NaClO3)制取ClO2。利用下图装置模拟工业制备ClO2:向三颈烧瓶中加入NaClO3溶液、浓H2SO4并通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿。

实验结束后,装置D中检测到含氯微粒有Cl-、ClO 和ClO
和ClO ,下列说法正确的是
,下列说法正确的是

实验结束后,装置D中检测到含氯微粒有Cl-、ClO
 和ClO
和ClO ,下列说法正确的是
,下列说法正确的是| A.35ClO2与37ClO2之间互为同位素 |
| B.若不考虑其他反应,装置D溶液可吸收0.2molClO2 |
C.反应后溶液中Cl-和ClO 的物质的量之比等于1:5 的物质的量之比等于1:5 |
D.反应后溶液中一定存在n(Na+)=n(Cl-)+n(ClO )+n(ClO )+n(ClO ) ) |
您最近一年使用:0次



