分A、B、C、D、E是中学常见的五种化合物,它们之间有下列转化关系:
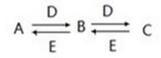
已知A溶液显碱性,可促进水的电离;D溶液显酸性,A、D溶液焰色反应均为黄色。
(1)若A、B、C中含有相同的金属元素,且B能溶于酸也能溶于碱,D能与Ba(OH)2反应生成不溶于盐酸的白色沉淀。则A的化学式为____________ ,D的化学式为_____________ ;A、C反应生成B的离子方程式为________________ 。
(2)若C是一种无色无味的气体,且能使澄清石灰水变浑浊。用离子方程式表示A溶液显碱性的原因_________________ ; C与E反应生成B的化学方程式为______________ 。
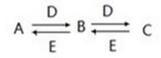
已知A溶液显碱性,可促进水的电离;D溶液显酸性,A、D溶液焰色反应均为黄色。
(1)若A、B、C中含有相同的金属元素,且B能溶于酸也能溶于碱,D能与Ba(OH)2反应生成不溶于盐酸的白色沉淀。则A的化学式为
(2)若C是一种无色无味的气体,且能使澄清石灰水变浑浊。用离子方程式表示A溶液显碱性的原因
更新时间:2016-12-09 17:16:28
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A~I分别表示中学化学中常见的一种物质,它们之间的相互关系如下图所示:已知G在生产中可作为一种耐火材料,F是红褐色难溶于水的沉淀,A、B、C、D、E、F六种物质中均含同一种元素,其中I+B→A+G属于置换反应。(部分反应物、生成物没有列出)。请填写下列空白:
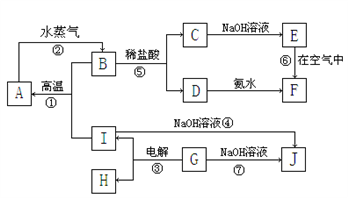
(1)如何检验D中阳离子___________________________________________ 。
(2)写出反应②的化学方程式:__________________ 。写出反应④的离子方程式:__________________________ 。
(3)若D溶液中混有C,用离子方程式表示除去的方法:____________________ 。
(4)E在空气中变成F的实验现象是_________________________________ 。
(5)写出反应⑥的化学方程式,并用单线桥标出电子转移的方向和数目:_______ 。

(1)如何检验D中阳离子
(2)写出反应②的化学方程式:
(3)若D溶液中混有C,用离子方程式表示除去的方法:
(4)E在空气中变成F的实验现象是
(5)写出反应⑥的化学方程式,并用单线桥标出电子转移的方向和数目:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】I.下图是某元素及其重要化合物之间的相互转化关系图(生成物中不含该元素的物质均已略去)。其中A是单质,D在常温下呈气态,F可用作氮肥。
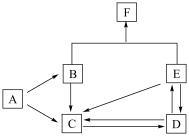
据此,请回答下列问题:
(1)写出以下物质的化学式:A_______ ,D_______ ,F_______ 。
(2)写出下列变化的化学方程式:
BC_______
EC_______
II.氢燃料电池车是北京冬奥会期间的交通服务用车,酸性氢氧燃料电池的构造如图所示。
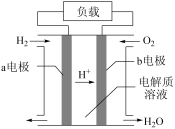
(3)若该电池中的电解质溶液是稀硫酸溶液,则a电极上发生反应的电极反应式为_______ 。
(4)b电极是该电池的_______ 极(填“正”或“负”),从氧化还原反应的角度分析,该电极发生的反应属于_______ 反应。
(5)当转移0.2mol电子时,需要消耗标况下的氢气体积是_______ L。

据此,请回答下列问题:
(1)写出以下物质的化学式:A
(2)写出下列变化的化学方程式:
BC
EC
II.氢燃料电池车是北京冬奥会期间的交通服务用车,酸性氢氧燃料电池的构造如图所示。

(3)若该电池中的电解质溶液是稀硫酸溶液,则a电极上发生反应的电极反应式为
(4)b电极是该电池的
(5)当转移0.2mol电子时,需要消耗标况下的氢气体积是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知:X、Y分别是地壳中含量最高的金属和非金属元素的单质,D、E、F为气体,X在酸性或碱性溶液中均可与NO3-发生氧化还原反应,气体D和G反应可生成盐,气体D和A溶液反应生成白色沉淀,气体E和F在NaOH溶液中按1:1反应钠盐M,各物质转化关系如下:
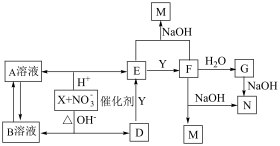
请回答下列问题:
(1)M的化学式__________ 。
(2)请写出D的溶液与A溶液反应的离子方程式:___________
(3)写出X在碱性条件下与NO3-反应的离子方程式:_____________
(4)标况下,若E,F的混合气体共48mL,恰好被10mL菜浓度的NaOH溶液吸收,则该NaOH溶液浓度为______ mol,若反应后所得溶液中M和N的浓度之比为7:1,则原来气体中E与F的体积比为________ 。

请回答下列问题:
(1)M的化学式
(2)请写出D的溶液与A溶液反应的离子方程式:
(3)写出X在碱性条件下与NO3-反应的离子方程式:
(4)标况下,若E,F的混合气体共48mL,恰好被10mL菜浓度的NaOH溶液吸收,则该NaOH溶液浓度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铁和铝是两种重要的金属,它们的单质及其化合物有着各自的用途。用工业烧渣(主要成分为 、
、 ,含少量FeO等)回收并分离
,含少量FeO等)回收并分离 和
和 ,工艺流程图如下所示:
,工艺流程图如下所示:

已知: 。
。
回答下列问题:
(1)“烧渣”中加入NaOH溶液发生反应的化学方程式为___________ 。
(2)“物质X”的俗称为___________ 。物质X也可以通过向饱和氯化钠溶液中先后通入足量的氨气和二氧化碳制得,写出反应的化学方程式:___________ 。
(3)向“滤渣I”中加入盐酸溶解后,再加入双氧水的目的是___________ ,发生反应的离子方程式为___________ 。
(4)写出“物质Y”的一种用途:___________ 。
(5)若将“滤渣1”用适量硫酸恰好完全溶解后,进行过滤得到 和
和 的混合溶液。通过元素分析测得其中Fe和S的物质的量之比
的混合溶液。通过元素分析测得其中Fe和S的物质的量之比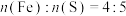 ,则此溶液中
,则此溶液中 和
和 的物质的量之比为
的物质的量之比为___________ 。
 、
、 ,含少量FeO等)回收并分离
,含少量FeO等)回收并分离 和
和 ,工艺流程图如下所示:
,工艺流程图如下所示:
已知:
 。
。回答下列问题:
(1)“烧渣”中加入NaOH溶液发生反应的化学方程式为
(2)“物质X”的俗称为
(3)向“滤渣I”中加入盐酸溶解后,再加入双氧水的目的是
(4)写出“物质Y”的一种用途:
(5)若将“滤渣1”用适量硫酸恰好完全溶解后,进行过滤得到
 和
和 的混合溶液。通过元素分析测得其中Fe和S的物质的量之比
的混合溶液。通过元素分析测得其中Fe和S的物质的量之比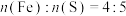 ,则此溶液中
,则此溶液中 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】铬盐是一种重要的战略资源,广泛用于电镀、涂料、木材防腐等领域。其中,红矾钠(即重铬酸钠晶体Na2Cr2O7•2H2O)作为铬盐的母系产品,常用于制造其他铬系产品。铬的主要自然资源则是铬铁矿FeCr2O4(含有Al2O3、MgO、SiO2等杂质),生产红矾钠的主要流程如图所示:
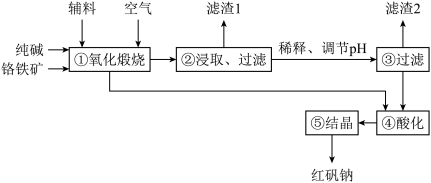
(1)已知Fe(CrO2)2中铁元素为+2价,则铬元素的化合价为____ 价,其基态原子的价电子排布式为____ 。
(2)①中的主反应为:4FeCr2O4+8Na2CO3+7O2 8Na2CrO4+2Fe2O3+8CO2;其中一个副反应为:Al2O3+Na2CO3
8Na2CrO4+2Fe2O3+8CO2;其中一个副反应为:Al2O3+Na2CO3 2NaAlO2↑+CO2,写出另一个副反应的化学方程式
2NaAlO2↑+CO2,写出另一个副反应的化学方程式____ ;③中滤渣2的主要成分是____ 。
(3)进入步骤④酸化的气体过量,该反应的离子方程式为____ ;该反应在不同温度下反应进行2小时,测得反应温度对反应转化率的影响如图所示:
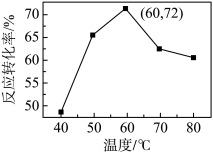
60~80℃条件下,反应转化率降低的原因可能是____ 。
(4)用含FeCr2O4为40%的铬铁矿1000kg,酸化反应在60℃条件下进行2小时,其余各步均完全转化,最终制得红矾钠(M=298g/mol)的质量为____ kg。(保留整数)
(5)Cr2O3为重要铬系产品,我国科学家采用Cr2O3(SG)和H-SAPO-34复合催化剂极大提高短链烯烃选择性。CO2和H2在催化剂Cr2O3(SG)表面转化为甲醇的各步骤所需要克服的能垒及甲醇在H-SAPO-34作用下产生乙烯、丙烯示意图如图。
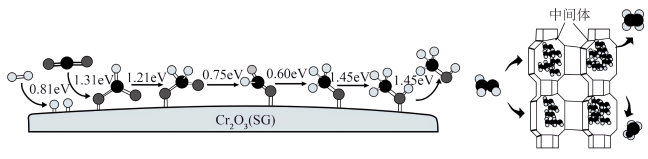
①二氧化碳→甲醇过程中,____ 的生成是决速步骤(填化学式)。
②H-SAPO-34具有氧八元环构成的笼状结构,笼口为小的八环孔(直径0.38nm)。从结构角度推测、短链烯烃选择性提高的原因是_____ 。

(1)已知Fe(CrO2)2中铁元素为+2价,则铬元素的化合价为
(2)①中的主反应为:4FeCr2O4+8Na2CO3+7O2
 8Na2CrO4+2Fe2O3+8CO2;其中一个副反应为:Al2O3+Na2CO3
8Na2CrO4+2Fe2O3+8CO2;其中一个副反应为:Al2O3+Na2CO3 2NaAlO2↑+CO2,写出另一个副反应的化学方程式
2NaAlO2↑+CO2,写出另一个副反应的化学方程式(3)进入步骤④酸化的气体过量,该反应的离子方程式为

60~80℃条件下,反应转化率降低的原因可能是
(4)用含FeCr2O4为40%的铬铁矿1000kg,酸化反应在60℃条件下进行2小时,其余各步均完全转化,最终制得红矾钠(M=298g/mol)的质量为
(5)Cr2O3为重要铬系产品,我国科学家采用Cr2O3(SG)和H-SAPO-34复合催化剂极大提高短链烯烃选择性。CO2和H2在催化剂Cr2O3(SG)表面转化为甲醇的各步骤所需要克服的能垒及甲醇在H-SAPO-34作用下产生乙烯、丙烯示意图如图。

①二氧化碳→甲醇过程中,
②H-SAPO-34具有氧八元环构成的笼状结构,笼口为小的八环孔(直径0.38nm)。从结构角度推测、短链烯烃选择性提高的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取Al2O3的两种工艺的流程如图所示:
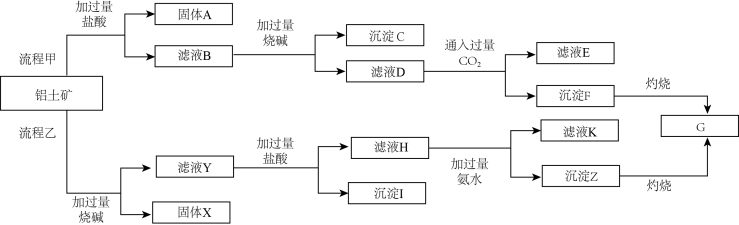
请回答下列问题:
(1)流程乙加入烧碱后和Al2O3反应的离子方程式为_________ 。
(2)流程甲滤液D中通入过量CO2的化学方程式为_________ 。
(3)验证滤液B中是否含有Fe3+的方法:_________ 。
(4)写出滤液E中溶质的一种用途:_________ 。
(5)由物质G制取铝的化学方程式为_________ 。
(6)氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AlN与一种中学常见气体X。已知每转移3mole-,有1.5mol化合物X生成,此反应的化学方程式为_________ 。

请回答下列问题:
(1)流程乙加入烧碱后和Al2O3反应的离子方程式为
(2)流程甲滤液D中通入过量CO2的化学方程式为
(3)验证滤液B中是否含有Fe3+的方法:
(4)写出滤液E中溶质的一种用途:
(5)由物质G制取铝的化学方程式为
(6)氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AlN与一种中学常见气体X。已知每转移3mole-,有1.5mol化合物X生成,此反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】黄铜矿是一种铜铁硫化物矿物(主要成分为 ,含少量杂质
,含少量杂质 等),工业上利用黄铜矿可生产硫酸铜、氧化铁红及亚硫酸铵,主要流程如下:
等),工业上利用黄铜矿可生产硫酸铜、氧化铁红及亚硫酸铵,主要流程如下:
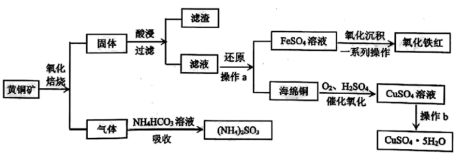
(1)黄铜矿在氧化焙烧前磨成精粉目的是___________ ;滤渣的主要成分___________ 。
(2)操作b流程依次为蒸发浓缩、___________ 、过滤、洗涤干燥。
(3)氧化焙烧反应为: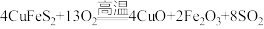 ,则反应中生成
,则反应中生成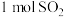 转移电子物质的量为
转移电子物质的量为___________ mol。
(4)写出滤液“还原”工艺中产生 的离子方程式
的离子方程式___________ 。
(5)湿法催化氧化制备硫酸铜相比传统法有很多优点,请写出海绵铜“催化氧化”中化学反应方程式___________ 。
(6)上述工艺生产的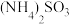 暴露在空气中易变质,请设计实验验证
暴露在空气中易变质,请设计实验验证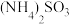 是否变质
是否变质___________ 。
 ,含少量杂质
,含少量杂质 等),工业上利用黄铜矿可生产硫酸铜、氧化铁红及亚硫酸铵,主要流程如下:
等),工业上利用黄铜矿可生产硫酸铜、氧化铁红及亚硫酸铵,主要流程如下:
(1)黄铜矿在氧化焙烧前磨成精粉目的是
(2)操作b流程依次为蒸发浓缩、
(3)氧化焙烧反应为:
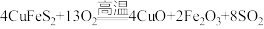 ,则反应中生成
,则反应中生成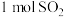 转移电子物质的量为
转移电子物质的量为(4)写出滤液“还原”工艺中产生
 的离子方程式
的离子方程式(5)湿法催化氧化制备硫酸铜相比传统法有很多优点,请写出海绵铜“催化氧化”中化学反应方程式
(6)上述工艺生产的
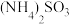 暴露在空气中易变质,请设计实验验证
暴露在空气中易变质,请设计实验验证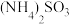 是否变质
是否变质
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】 是一种重要的化工产品,以黄铁矿烧渣(主要含
是一种重要的化工产品,以黄铁矿烧渣(主要含 、
、 、
、 等物质)为原料制备
等物质)为原料制备 的过程如下。
的过程如下。
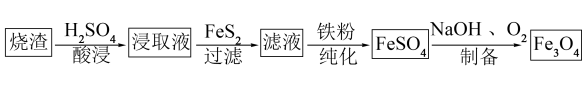
(1)酸浸、过滤
①酸浸过程 发生反应的离子方程式是
发生反应的离子方程式是___________ 。
②充分酸浸后浸取液中仍有 残留,加入
残留,加入 可进一步提高钙的脱除率,结合方程式解释原因
可进一步提高钙的脱除率,结合方程式解释原因___________ 。
(2)纯化
①Fe粉的作用是___________ 。
②检验纯化是否完全还原,应向滤液中加入___________ 。
a. 溶液 b.
溶液 b. 溶液 c.KSCN溶液
溶液 c.KSCN溶液
(3)制备
将NaOH溶液与 溶液(稍过量)按一定比例混合,产生白色沉淀,继而转变为墨绿色,最后变为黑色。溶液混合的同时通入空气并记录pH的变化,如图所示。
溶液(稍过量)按一定比例混合,产生白色沉淀,继而转变为墨绿色,最后变为黑色。溶液混合的同时通入空气并记录pH的变化,如图所示。
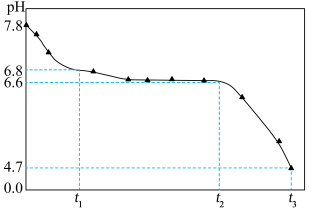
已知:
ⅰ.pH≈7.8时,浊液中主要存在 、
、 和少量
和少量
ⅱ.墨绿色物质主要成分为 制备过程可能发生了如下历程:
制备过程可能发生了如下历程:

①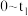 时段,pH明显降低。结合离子方程式解释原因:
时段,pH明显降低。结合离子方程式解释原因:___________ 。
② 时段,墨绿色物质的生成与转化(生成
时段,墨绿色物质的生成与转化(生成 )同时进行。
)同时进行。
a.生成墨绿色物质的方程式是:___________ 。
b.墨绿色物质转化为 的方程式是:
的方程式是:___________ 。
③ 时段,pH继续降低的原因是:
时段,pH继续降低的原因是:___________ 。
 是一种重要的化工产品,以黄铁矿烧渣(主要含
是一种重要的化工产品,以黄铁矿烧渣(主要含 、
、 、
、 等物质)为原料制备
等物质)为原料制备 的过程如下。
的过程如下。
(1)酸浸、过滤
①酸浸过程
 发生反应的离子方程式是
发生反应的离子方程式是②充分酸浸后浸取液中仍有
 残留,加入
残留,加入 可进一步提高钙的脱除率,结合方程式解释原因
可进一步提高钙的脱除率,结合方程式解释原因(2)纯化
①Fe粉的作用是
②检验纯化是否完全还原,应向滤液中加入
a.
 溶液 b.
溶液 b. 溶液 c.KSCN溶液
溶液 c.KSCN溶液(3)制备
将NaOH溶液与
 溶液(稍过量)按一定比例混合,产生白色沉淀,继而转变为墨绿色,最后变为黑色。溶液混合的同时通入空气并记录pH的变化,如图所示。
溶液(稍过量)按一定比例混合,产生白色沉淀,继而转变为墨绿色,最后变为黑色。溶液混合的同时通入空气并记录pH的变化,如图所示。
已知:
ⅰ.pH≈7.8时,浊液中主要存在
 、
、 和少量
和少量
ⅱ.墨绿色物质主要成分为
 制备过程可能发生了如下历程:
制备过程可能发生了如下历程:
①
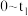 时段,pH明显降低。结合离子方程式解释原因:
时段,pH明显降低。结合离子方程式解释原因:②
 时段,墨绿色物质的生成与转化(生成
时段,墨绿色物质的生成与转化(生成 )同时进行。
)同时进行。a.生成墨绿色物质的方程式是:
b.墨绿色物质转化为
 的方程式是:
的方程式是:③
 时段,pH继续降低的原因是:
时段,pH继续降低的原因是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下图所涉及的物质中,C、D、E均为单质,且E为日常生活中常见金属,其余均为化合物。它们之间的转化关系如图所示(反应中生成的水及次要产物均已略去)。
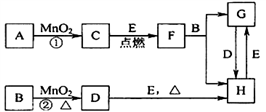
请回答:
(1)写出有关物质的化学式:A______ ,F______ ,H______ 。
(2)指出MnO2在相关反应中的作用:反应①中是_____ 剂,反应②中是_____ 剂。
(3)若反应①是在加热条件下进行,则A是__________ (填化学式)。
(4)写出反应②的化学方程式____________ 。
(5)向G中加入NaOH溶液,观察到的现象为____________ 。

请回答:
(1)写出有关物质的化学式:A
(2)指出MnO2在相关反应中的作用:反应①中是
(3)若反应①是在加热条件下进行,则A是
(4)写出反应②的化学方程式
(5)向G中加入NaOH溶液,观察到的现象为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
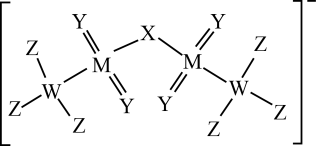
【推荐1】某离子液体的阴离子的结构如图所示,其中W、X、Y、Z、M为原子序数依次增大的短周期非金属元素,W是有机分子的骨架元素。W、X、Y、Z、M分别为_____________ 。

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中,A、C及B、D分别是同主族元素;A元素的原子半径是所有主族元素中原子半径最小的;B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍;四种元素所形成的单质中常温下A、B单质是气体,C、D单质是固体。
(1)写出四种元素的名称:A___________ B____________ C___________ D___________ 。
(2)用电子式表示A2B的形成过程:_________________________ 。
(3)由B、C两元素所形成的原子个数比为1:1的化合物属于__________ (填“离子”或“共价”)化合物,写出它与水反应的离子方程式______________________ 。
(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,其化学方程式为_____________ 。
(5)A2B和A2D的沸点较高者为______________ (填化学式)。
(1)写出四种元素的名称:A
(2)用电子式表示A2B的形成过程:
(3)由B、C两元素所形成的原子个数比为1:1的化合物属于
(4)实验室常用A、B两元素所形成的原子个数为1:1的化合物来制备一种常见气体,其化学方程式为
(5)A2B和A2D的沸点较高者为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13;B的化合物种类繁多,数目庞大;C、D 是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1:1的原子个数比形成的化合物的电子式:_______ ,F的原子结构示意图为_______ 。
(2)B、D形成的化合物 BD2中存在的化学键为_______ 键(填“离子”或“共价”,下同),A、C、F三种元素形成的化合物CA4F为_______ 化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性,则甲、乙反应的离子方程式为_______ 。
(4)A、C、D、E的原子半径由大到小的顺序是_______ (用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性_______ 于F(填“强”或“弱”),并用化学方程式证明上述结论_______ 。
(1)写出D与E以1:1的原子个数比形成的化合物的电子式:
(2)B、D形成的化合物 BD2中存在的化学键为
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性,则甲、乙反应的离子方程式为
(4)A、C、D、E的原子半径由大到小的顺序是
(5)元素B和F的非金属性强弱,B的非金属性
您最近一年使用:0次



