下列说法正确的是( )
| A.增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增加 |
| B.对于有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大 |
| C.改变条件能使化学反应速率增大的主要原因是增大了反应物分子中活化分子的有效碰撞几率 |
| D.对于本来不能发生的化学反应,改变条件可以使反应发生 |
2016高二·全国·课时练习 查看更多[5]
更新时间:2016-11-15 16:01:25
|
【知识点】 影响化学反应速率的外因
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 在空气中与
在空气中与 的反应是分两步完成的,其反应过程如图所示,下列有关说法错误的是
的反应是分两步完成的,其反应过程如图所示,下列有关说法错误的是

 在空气中与
在空气中与 的反应是分两步完成的,其反应过程如图所示,下列有关说法错误的是
的反应是分两步完成的,其反应过程如图所示,下列有关说法错误的是
A.反应①的方程式为 ,且为放热反应 ,且为放热反应 |
B.反应 的活化能为 的活化能为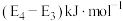 |
| C.第二步反应是该反应的决速步骤 |
D.如果加入合适的催化剂,可以改变该反应的 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某学习小组用足量大小相同的去膜镁条与体积均为40mL、浓度均为0.1mol·L-1的醋酸(A瓶)和盐酸(B瓶)分别反应,相同条件下(该条件下Vm=22.5L·mol-1)测得反应产生的气体体积与反应时间的关系如下表所示:
下列说法不正确的是
气体读数/mL 时间/s 物质 | 5 | 10 | 15 | 20 | …… | 45 |
| 醋酸(A瓶) | 88 | 170 | 248 | 326 | …… | 865 |
| 盐酸(B瓶) | 10 | 18 | 30 | 64 | …… | 464 |
下列说法不正确的是
| A.产生气体体积为0~5mL时,A瓶与B瓶反应速率不同的原因是c(H+)不同 |
| B.产生气体体积为5~10mL时,B瓶产生气体的平均速率为0.625mL·s-1 |
| C.产生气体体积为0~15mL时,A瓶反应速率增大是醋酸继续电离使c(H+)升高所致 |
| D.产生气体体积为0~45mL时,镁与盐酸反应的速率始终大于镁与醋酸反应的速率 |
您最近半年使用:0次

 的影响说法不正确的是
的影响说法不正确的是

