硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为______________ 。
(2)锗、砷、硒的第一电离能大小排序为_______________ 。H2SeO4的酸性比H2SeO3的强,其原因是______________________ 。
(3)H2SeO3的中心原子杂化类型是_________ ;SeO32-的立体构型是___________ 。与SeO42-互为等电体的分子有(写一种物质的化学式即可)_______________ 。
(4)H2Se属于_________ (填:极性或非极性)分子;单质硒的熔点为217℃,它属于________ 晶体。
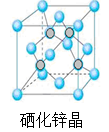
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为____________ ;若该晶胞密度为ρg•cm-3,硒化锌的摩尔质量为M g/mol。NA代表阿伏加德罗常数,则晶胞参数a为___________ pm。
(1)基态硒原子的价层电子排布式为
(2)锗、砷、硒的第一电离能大小排序为
(3)H2SeO3的中心原子杂化类型是
(4)H2Se属于
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为

更新时间:2016-12-09 17:22:53
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】过氧化钠是一种重要的强氧化剂,也能作为封闭生态系统的CO2吸收剂和生氧剂,其反应原理为:2Na2O2+2CO2=2NaCO3+O2。答下列问题:
(1)上述反应中两种同周期原子的半径大小为______ (填写元素符号)。反应中破坏的化学键类型有______ 。
(2)S和O位于元素周期表同一主族,非金属性:S______ O(填“<”、“>”或“=”),用一个化学方程式说明判断的理由:______ 。
(3)过氧化钠在日常保存时常因发生反应: ,而发生变质。
,而发生变质。
①该反应的平衡常数表达式为______ 。
②向保存在恒温密闭容器中过氧化钠中通入少量O2,固体质量将______ (“增大”、“减小”或“不变”,下同),达到新平衡时容器内气体的压强将______ 。
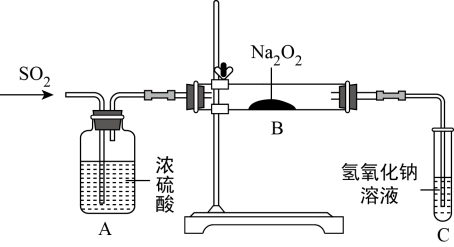
(4)利用如图装置探究Na2O2与SO2反应的产物。实验中当通入二氧化硫气体,将带有火星的木条插入试管C中,木条复燃。有同学猜测,B中反应后的固体产物可能是亚硫酸钠和硫酸钠的混合物。
①该同学认为存在硫酸钠的原因是______ (用化学方程式解释)。
②设计一个简单的实验证明是否存在硫酸钠。简要地写出实验的步骤、现象和结论______ 。
(1)上述反应中两种同周期原子的半径大小为
(2)S和O位于元素周期表同一主族,非金属性:S
(3)过氧化钠在日常保存时常因发生反应:
 ,而发生变质。
,而发生变质。①该反应的平衡常数表达式为
②向保存在恒温密闭容器中过氧化钠中通入少量O2,固体质量将
(4)利用如图装置探究Na2O2与SO2反应的产物。实验中当通入二氧化硫气体,将带有火星的木条插入试管C中,木条复燃。有同学猜测,B中反应后的固体产物可能是亚硫酸钠和硫酸钠的混合物。

①该同学认为存在硫酸钠的原因是
②设计一个简单的实验证明是否存在硫酸钠。简要地写出实验的步骤、现象和结论
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过________ 方法区别晶体、准晶体和非晶体。
(2)基态Fe原子有_______ 个未成对电子,Fe3+的电子排布式为_________ 。可用硫氰化钾检验Fe3+,形成的配合物的颜色为____________ 。
(3)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道为___________ ,1mol乙醛分子中含有的 键的数目为
键的数目为___________ 。乙酸的沸点明显高于乙醛,其主要原因是_______________________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和定点,则该晶胞中有________ 个铜原子。
(4)Al单质为面心立方晶体,晶胞中铝原子的配位数为__ 。
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态Fe原子有
(3)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道为
 键的数目为
键的数目为(4)Al单质为面心立方晶体,晶胞中铝原子的配位数为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】铁和钴是两种重要的过渡元素。
(1)钴位于元素周期表的第______ 族,其基态原子中未成对电子个数为________ 。
(2)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为_________________________________ ,所含非金属元素的电负性由大到小的顺序是_____________________________ 。
(3)尿素[CO(NH2)2]分子中,碳原子为_______ 杂化,分子中σ键与π键的数目之比为_________ 。
(4)FeO晶体与NaCl晶体结构相似,比较FeO与NaCl的晶格能大小,还需知道的数据是________________________________________ 。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为___________________ 。
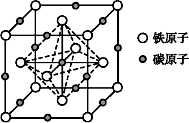
(6)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为____________ 。若晶体密度为d g·cm-3,则晶胞中最近的两个碳原子的距离为___________________ pm(阿伏伽德罗常数的值用NA表示,写出简化后的计算式即可)。
(1)钴位于元素周期表的第
(2)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为
(3)尿素[CO(NH2)2]分子中,碳原子为
(4)FeO晶体与NaCl晶体结构相似,比较FeO与NaCl的晶格能大小,还需知道的数据是
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为
(6)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示,则该物质的化学式为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】CoP、FeS2、NiS2等物质对电化学氢析出反应有良好的催化活性和稳定性。请回答下列问题:
(1)基态Co原子价层电子的电子排布图(轨道表达式)为________________ ,基态P原子的电子占据最高能级的电子云轮廓图为_______ 。
(2)PH3的沸点_____ (填“高于”或“低于”)NH3,原因是______________ 。
(3)下图为白磷(P4)的晶胞示意图,晶胞的边长为a nm,设阿伏加 德罗常数的数值为NA,其晶体密度的计算表达式为______ g·cm-3。

(1)基态Co原子价层电子的电子排布图(轨道表达式)为
(2)PH3的沸点
(3)下图为白磷(P4)的晶胞示意图,晶胞的边长为a nm,设阿伏加 德罗常数的数值为NA,其晶体密度的计算表达式为

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】硼和氮的单质及一些化合物在工农业生产等领域有重要应用。回答下列问题:
(1)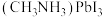 的晶胞结构如图所示,其中B代表
的晶胞结构如图所示,其中B代表 。
。

①原子分数坐标可用于表示晶胞内部各原子的相对位置。其中,原子分数坐标A为(0,0,0),则C的原子分数坐标为_______ 。
②该晶胞沿体对角线方向的投影图为_______ (填标号)。
a.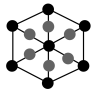 b.
b.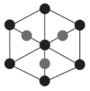 c.
c. d.
d.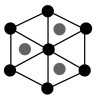
(2)晶体硼有多种变体,但其基本结构单元都是由硼原子组成的正二十面体(见图I),每个顶点为一个硼原子,每个三角形均为等边三角形,则每一个此基本结构单元由_______ 个硼原子构成。
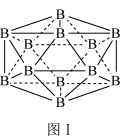
(3)硼和氮构成的一种氮化硼晶体的结构与石墨晶体结构相类似,硼、氮原子相互交替排列(见图II),其晶胞结构如图III所示。设层内B-N核间距为apm,面间距为bpm,则该氮化硼晶体的密度为_______ g/cm3(用含a、b、NA的代数式表示)。

(1)
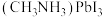 的晶胞结构如图所示,其中B代表
的晶胞结构如图所示,其中B代表 。
。
①原子分数坐标可用于表示晶胞内部各原子的相对位置。其中,原子分数坐标A为(0,0,0),则C的原子分数坐标为
②该晶胞沿体对角线方向的投影图为
a.
 b.
b. c.
c. d.
d.
(2)晶体硼有多种变体,但其基本结构单元都是由硼原子组成的正二十面体(见图I),每个顶点为一个硼原子,每个三角形均为等边三角形,则每一个此基本结构单元由

(3)硼和氮构成的一种氮化硼晶体的结构与石墨晶体结构相类似,硼、氮原子相互交替排列(见图II),其晶胞结构如图III所示。设层内B-N核间距为apm,面间距为bpm,则该氮化硼晶体的密度为

您最近一年使用:0次

 晶胞与
晶胞与 晶胞相似(如图),
晶胞相似(如图), 的位置
的位置 ,请计算
,请计算 。
。


