用硫酸酸化的草酸(H2C2O4,二元弱酸)溶液能将KMnO4溶液中的MnO4﹣转化为Mn2+。某化学小组研究发现,少量MnSO4可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,请完成以下实验设计表。
表中a、b的值分别为:a=__________ 、b=__________
(2)该反应的离子方程式_______________________ 。
(3)若t1<t2,则根据实验①和②得到的结论是______________________ 。
(4)请你设计实验④验证MnSO4对该反应起催化作用,完成下表中内容.
(5)某化学小组用滴定法测定KMnO4溶液物质的量浓度:取W g草酸晶体(H2C2O4•2H2O,其摩尔质量126 g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定两次,平均消耗KMnO4溶液V mL.请回答下列问题:
① 该测定方法中___________ (填“需要”或“不需要”)加入指示剂;
② 计算得KMnO4溶液的c(KMnO4)=________________ mol/L.(请写出最后化简结果)
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,请完成以下实验设计表。
| 实验 编号 | 温度 | 初始pH | 0.1mol/L 草酸溶液/mL | 0.01mol/L KMnO4溶的 体积/mL | 蒸馏水 体积/mL | 待测数据(反应混合液褪色 时间/s) |
| ① | 常温 | 1 | 20 | 50 | 30[ | t1 |
| ② | 常温 | 2 | 20 | 50 | 30 | t2 |
| ③ | 常温 | 2 | 40 | a | b | t3 |
表中a、b的值分别为:a=
(2)该反应的离子方程式
(3)若t1<t2,则根据实验①和②得到的结论是
(4)请你设计实验④验证MnSO4对该反应起催化作用,完成下表中内容.
| 实验方案(不要求写出具体操作过程) | 预期实验结果和结论 |
| 若反应混合液褪色时间小于实验①中的t1,则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
(5)某化学小组用滴定法测定KMnO4溶液物质的量浓度:取W g草酸晶体(H2C2O4•2H2O,其摩尔质量126 g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定两次,平均消耗KMnO4溶液V mL.请回答下列问题:
① 该测定方法中
② 计算得KMnO4溶液的c(KMnO4)=
16-17高二上·湖南株洲·期中 查看更多[2]
更新时间:2016/12/13 08:58:44
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】KMnO4在实验室和工业生产中有广泛用途。
Ⅰ.某小组拟用酸性KMnO4溶液与H2C2O4溶液(弱酸)的反应(此反应为放热反应)来探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol/L H2C2O4溶液、0.010 mol/L KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)
回答下列问题:
(1)完成上述反应原理的离子反应方程式_______________________。
(2)上述实验①②是探究____________对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则a为___________;乙是实验需要测量的物理量,则表格中“乙”应填写___________;上述实验②④是探究_________对化学反应速率的影响。

Ⅱ.某化学小组利用如图装置进行实验证明氧化性:KMnO4>Cl2>Br2。限选试剂:KBr溶液、KMnO4、浓盐酸、浓硫酸。
(3)装置d中观察到的现象为____________________;此实验装置的不足之处是无尾气吸收装置,请写出处理尾气的离子方程式_____________________。
Ⅰ.某小组拟用酸性KMnO4溶液与H2C2O4溶液(弱酸)的反应(此反应为放热反应)来探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol/L H2C2O4溶液、0.010 mol/L KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)
| 物理量 编号 | V(0.20 mol/LH2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010 mol/L KMnO4溶液)/mL | m(MnSO4固体)/g | T/℃ | 乙 |
| ① | 2.0 | 0 | 4.0 | 0 | 50 | |
| ② | 2.0 | 0 | 4.0 | 0 | 25 | |
| ③ | 1.0 | a | 4.0 | 0 | 25 | |
| ④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
(1)完成上述反应原理的离子反应方程式_______________________。
(2)上述实验①②是探究____________对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则a为___________;乙是实验需要测量的物理量,则表格中“乙”应填写___________;上述实验②④是探究_________对化学反应速率的影响。

Ⅱ.某化学小组利用如图装置进行实验证明氧化性:KMnO4>Cl2>Br2。限选试剂:KBr溶液、KMnO4、浓盐酸、浓硫酸。
(3)装置d中观察到的现象为____________________;此实验装置的不足之处是无尾气吸收装置,请写出处理尾气的离子方程式_____________________。
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】碘及其化合物在人类活动中占有重要地位。回答下列问题:
(1)“大象牙膏”实验中,将 、KI和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
、KI和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
第一步: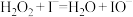
 慢反应
慢反应
第二步:
 快反应
快反应
①该反应的催化剂为_______ ,总反应方程式为_______ ;
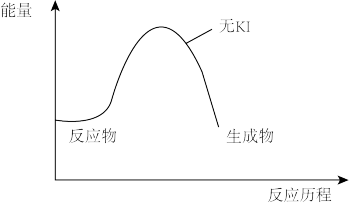
②在答题卡的图中画出有KI参与的两步反应的能量历程图。______
(2)已知:25℃下,
(i)
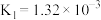
(ii)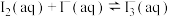

(iii)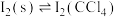

其中,反应ⅱ的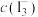 随温度的变化如如图:
随温度的变化如如图:

烧杯甲:将mg 加入20mL水中(含
加入20mL水中(含 沉淀);
沉淀);
烧杯乙:将mg 加入20mLKI溶液(含
加入20mLKI溶液(含 沉淀)。
沉淀)。
①甲中存在平衡i,乙中存在平衡i和ⅱ,不考虑碘与水的反应以及其它反应,下列说法正确的是_______ 。
A.烧杯乙中剩余的 沉淀质量比甲的
沉淀质量比甲的 沉淀质量小
沉淀质量小
B.室温下,甲中加水稀释,溶液中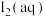 浓度一定减小
浓度一定减小
C.乙中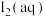 浓度与甲中
浓度与甲中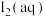 浓度相等
浓度相等
D.升高温度,反应ⅱ的平衡常数大于640
②为了探究乙中溶液含碘微粒的存在形式,进行实验:恒温25℃向10mL一定浓度的 溶液中加入10mL
溶液中加入10mL KI溶液,反应结束后碘元素的微粒主要存在平衡ii,相关微粒浓度如下:
KI溶液,反应结束后碘元素的微粒主要存在平衡ii,相关微粒浓度如下:
其中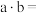
_______ (用含c的代数式表示),若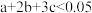 ,说明平衡体系中
,说明平衡体系中_______ 。
③计算25℃下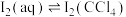 的平衡常数K=
的平衡常数K=_______ (取整数);已知用有机溶剂从水溶液中萃取 时,萃取效率=
时,萃取效率= ×100%,用等体积的
×100%,用等体积的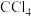 一次性萃取碘水[用
一次性萃取碘水[用 配制],萃取效率为
配制],萃取效率为_______ %(保留1位小数),若将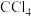 等分成2份,分两次萃取该碘水,萃取总效率
等分成2份,分两次萃取该碘水,萃取总效率_______ 一次性萃取的效率(填“大于”、“等于”、“小于”)。
(1)“大象牙膏”实验中,将
 、KI和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
、KI和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:第一步:
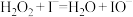
 慢反应
慢反应第二步:

 快反应
快反应①该反应的催化剂为
②在答题卡的图中画出有KI参与的两步反应的能量历程图。

(2)已知:25℃下,
(i)

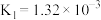
(ii)
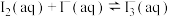

(iii)
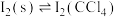

其中,反应ⅱ的
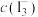 随温度的变化如如图:
随温度的变化如如图:
烧杯甲:将mg
 加入20mL水中(含
加入20mL水中(含 沉淀);
沉淀);烧杯乙:将mg
 加入20mLKI溶液(含
加入20mLKI溶液(含 沉淀)。
沉淀)。①甲中存在平衡i,乙中存在平衡i和ⅱ,不考虑碘与水的反应以及其它反应,下列说法正确的是
A.烧杯乙中剩余的
 沉淀质量比甲的
沉淀质量比甲的 沉淀质量小
沉淀质量小B.室温下,甲中加水稀释,溶液中
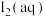 浓度一定减小
浓度一定减小C.乙中
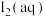 浓度与甲中
浓度与甲中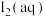 浓度相等
浓度相等D.升高温度,反应ⅱ的平衡常数大于640
②为了探究乙中溶液含碘微粒的存在形式,进行实验:恒温25℃向10mL一定浓度的
 溶液中加入10mL
溶液中加入10mL KI溶液,反应结束后碘元素的微粒主要存在平衡ii,相关微粒浓度如下:
KI溶液,反应结束后碘元素的微粒主要存在平衡ii,相关微粒浓度如下:| 微粒 |  | 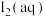 |  |
| 浓度/(mol/L) | a | b | c |
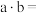
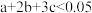 ,说明平衡体系中
,说明平衡体系中③计算25℃下
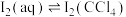 的平衡常数K=
的平衡常数K= 时,萃取效率=
时,萃取效率= ×100%,用等体积的
×100%,用等体积的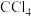 一次性萃取碘水[用
一次性萃取碘水[用 配制],萃取效率为
配制],萃取效率为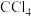 等分成2份,分两次萃取该碘水,萃取总效率
等分成2份,分两次萃取该碘水,萃取总效率
您最近半年使用:0次
【推荐3】烯丙醇是生产甘油、医药、农药、香料和化妆品的中间体。已知烯丙醇与水在一定条件下发生加成反应的原理如下:
Ⅰ:CH2=CHCH2OH(g)+H2O(g) HOCH2CH2CH2OH(g) △H1 △S1
HOCH2CH2CH2OH(g) △H1 △S1
Ⅱ:CH2=CHCH2OH(g)+H2O(g) CH3CH(OH)CH2OH(g) △H2
CH3CH(OH)CH2OH(g) △H2
已知:相关物质在298K时的标准摩尔生成焓(101kPa时,该温度下由最稳定单质生成1 mol某纯物质的焓变)如下表所示:
(1)△H2=_______ kJ/mol;反应CH2=CHCH2OH(g)+H2O(g) HOCH2CH2CH2OH(l)的熵变为△S1',则△S1
HOCH2CH2CH2OH(l)的熵变为△S1',则△S1_______ △S1' (填“>”“=”或“<”)。
(2)若向绝热恒容容器中加入CH2=CHCH2OH(g)和H2O(g),发生反应Ⅰ和Ⅱ,下列事实不能说明体系达到平衡状态的是_______(填选项字母)。
(3)已知:反应的压强平衡常数(K)满足方程Kp=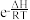 +C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为
+C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为_______ 和_______ 。
①该温度下,反应Ⅱ的压强平衡常数K=_______ 。
②若其他条件不变,初始时不充入He(g),而是按1:1的体积比充入CH2=CHCH2OH(g)和H2O(g),达到新平衡时,H2O(g)的转化率将_______ (填“增大”“减小”或“不变”),解释其原因为_______ 。
(5)烯丙醇的电氧化过程有重要应用。其在阳极放电时,同时存在三种电极反应(烯丙醇→丙烯酸、烯丙醇→丙烯醛、烯丙醇→丙二酸),各反应决速步骤的活化能如下表所示。
①该条件下,相同时间内,阳极产物中含量最多的为_______ 。
②碱性条件下,烯丙醇在电极上生成丙烯醛(CH2=CHCHO)的电极反应式为_______ 。
Ⅰ:CH2=CHCH2OH(g)+H2O(g)
 HOCH2CH2CH2OH(g) △H1 △S1
HOCH2CH2CH2OH(g) △H1 △S1Ⅱ:CH2=CHCH2OH(g)+H2O(g)
 CH3CH(OH)CH2OH(g) △H2
CH3CH(OH)CH2OH(g) △H2 已知:相关物质在298K时的标准摩尔生成焓(101kPa时,该温度下由最稳定单质生成1 mol某纯物质的焓变)如下表所示:
| 物质 | CH2=CHCH2OH(g) | H2O(g) | HOCH2CH2CH2OH(g) | CH3CH(OH)CH2OH(g) |
| 标准摩尔生成焓/(kJ/mol) | -171.8 | -241.8 | -464.9 | -485.7 |
(1)△H2=
 HOCH2CH2CH2OH(l)的熵变为△S1',则△S1
HOCH2CH2CH2OH(l)的熵变为△S1',则△S1(2)若向绝热恒容容器中加入CH2=CHCH2OH(g)和H2O(g),发生反应Ⅰ和Ⅱ,下列事实不能说明体系达到平衡状态的是_______(填选项字母)。
| A.容器内气体的压强不变 | B.容器内温度不变 |
| C.容器内气体的密度不变 | D.容器内气体的平均相对分子质量不变 |
(3)已知:反应的压强平衡常数(K)满足方程Kp=
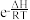 +C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为
+C(e为自然对数的底数, R、C均为常数)。据此判断,下图所示曲线L1~L5中,能分别代表反应Ⅰ和Ⅱ的Kp与温度T关系的曲线为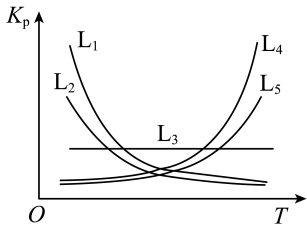
①该温度下,反应Ⅱ的压强平衡常数K=
②若其他条件不变,初始时不充入He(g),而是按1:1的体积比充入CH2=CHCH2OH(g)和H2O(g),达到新平衡时,H2O(g)的转化率将
(5)烯丙醇的电氧化过程有重要应用。其在阳极放电时,同时存在三种电极反应(烯丙醇→丙烯酸、烯丙醇→丙烯醛、烯丙醇→丙二酸),各反应决速步骤的活化能如下表所示。
| 反应 | 烯丙醇→丙烯酸 | 烯丙醇→丙烯醛 | 烯丙醇→丙二酸 |
| 活化能(单位:eV) | 8.6a | 2.5 a | 13.7a |
②碱性条件下,烯丙醇在电极上生成丙烯醛(CH2=CHCHO)的电极反应式为
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
(l)ClO2的制备:(已知:SO2+2NaClO3+H2SO4=2ClO2↑+2NaHSO4)
①装置A中反应的化学方程式为_______________ 。
②欲收集干燥的ClO2 ,选择上图中的装置,其连接顺序为 a→_________ (按气流方向,用小写字母表示)
③装置D的作用是_________ 。
(2)ClO2与 Na2S 的反应
将上述收集到的ClO2用 N2稀释以增强其稳定性,并将适量的稀释后的ClO2 通入上图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究 I 中反应的产物。
④ClO2与Na2S反应的离子方程式为__________ 。用于处理含硫废水时,ClO2相对于Cl2的优点是____________ (任写2条)。
(l)ClO2的制备:(已知:SO2+2NaClO3+H2SO4=2ClO2↑+2NaHSO4)
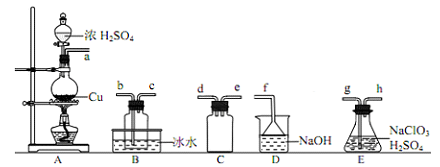
①装置A中反应的化学方程式为
②欲收集干燥的ClO2 ,选择上图中的装置,其连接顺序为 a→
③装置D的作用是
(2)ClO2与 Na2S 的反应
将上述收集到的ClO2用 N2稀释以增强其稳定性,并将适量的稀释后的ClO2 通入上图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究 I 中反应的产物。
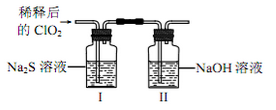
操作步骤 | 实验现象 | 结论 |
取少量Ⅰ中溶液于试管甲中, 加入Ba(OH)2溶液,振荡 | ① | 有硫酸根离子生成 |
另取少量Ⅰ中溶液于试管乙中, 滴加品红溶液和盐酸 | 品红溶液不翅色 | ② 无 |
若在试管甲中继续加Ba(OH)2溶液至 过量,静置,取上层清液于试管丙③ | 有白色沉淀生成 | 有Cl-生成 |
④ClO2与Na2S反应的离子方程式为
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】甲、乙两化学小组拟根据氨气还原氧化铜反应的原理测定某铜粉样品(混有CuO粉未)中金属铜的含量。
(1)甲小组利用下图装置(可以重复选用),通过测定反应生成水的质量来达到实验目的。
①按气流方向连接各仪器接口,顺序为______________ (填小写字母序号)。
②装置B中固体试剂的名称为____________________ 。
③装置A的作用为____________ 。
④下列两步操作应该先进行的是___________ (填序号):i.加热反应管 ii.向锥形瓶中逐滴滴加浓氨水,原因为________________________ 。
(2)乙小组利用上述装置通过测定反应前后装置C中固体的质量变化来达到实验目的。
①按气流方向连接各装置,顺序为______________ (填大写字母序号)。
②称取m1 g铜粉样品,测得反应前装置C的质量为m2 g,充分反应后装置C的质量为m3g。写出样品中金属铜的质量分数表达式__________________ 。
(3)从稀盐酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,重新设计一个测定样品中金属铜含量的实验方案(写出主要步骤,不必描述操作过程的细节)_____________________________ 。
(1)甲小组利用下图装置(可以重复选用),通过测定反应生成水的质量来达到实验目的。
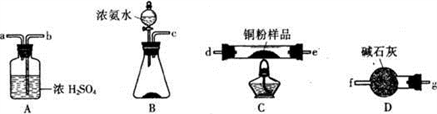
①按气流方向连接各仪器接口,顺序为
②装置B中固体试剂的名称为
③装置A的作用为
④下列两步操作应该先进行的是
(2)乙小组利用上述装置通过测定反应前后装置C中固体的质量变化来达到实验目的。
①按气流方向连接各装置,顺序为
②称取m1 g铜粉样品,测得反应前装置C的质量为m2 g,充分反应后装置C的质量为m3g。写出样品中金属铜的质量分数表达式
(3)从稀盐酸、浓硝酸、蒸馏水、双氧水中选用合适的试剂,重新设计一个测定样品中金属铜含量的实验方案(写出主要步骤,不必描述操作过程的细节)
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】实验室模拟合成硫酸的流程如图:

(1)从图中选择制取气体的合适装置
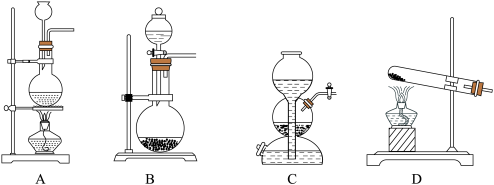
实验室用__ (填试剂)制取SO2,选择__ 装置;用氯酸钾和__ (填试剂)混合加热制取O2,选择__ 装置。
(2)SO2和O2通过甲装置,甲装置的作用除了将混合气体混合和控制SO2、O2的流速外,还有__ 作用。硬质玻璃管中发生反应的化学方程式是__ ;乙处导出的气体是__ 。

(3)使用乙处导出的有关气体制成硫酸,下列A、B、C三套装置中你选择的是__ ,该套装置与其它装置比较,其优点是(任写两点)__ 、__ 。
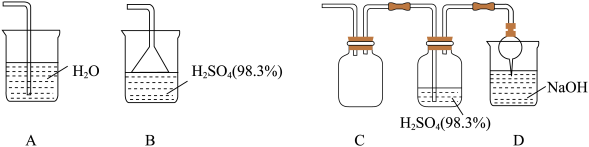

(1)从图中选择制取气体的合适装置

实验室用
(2)SO2和O2通过甲装置,甲装置的作用除了将混合气体混合和控制SO2、O2的流速外,还有

(3)使用乙处导出的有关气体制成硫酸,下列A、B、C三套装置中你选择的是

您最近半年使用:0次



