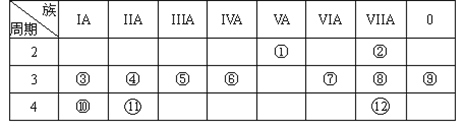
下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。
请按要求回答下列问题:
(1)元素③的最高价氧化物对应的水化物的化学式为___________________ ;
(2)②、③两元素的原子半径较大的是______________ (填元素符号);
(3)④和⑤两种元素的金属性较强的是_____________ (填元素符号);
(4)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式___________________ 。
 | IA | 0 | |||||||
| 1 | ① | II A | III A | IV A | V A | VI A | VIIA | ||
| 2 | ② | ③ | |||||||
| 3 | ④ | ⑤ | ⑥ | ||||||
请按要求回答下列问题:
(1)元素③的最高价氧化物对应的水化物的化学式为
(2)②、③两元素的原子半径较大的是
(3)④和⑤两种元素的金属性较强的是
(4)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式
更新时间:2017-02-17 14:46:07
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,请回答有关问题:
(1) 表中化学性质最不活泼的元素,其原子结构示意图为________________ 。
(2) 表中能形成两性氢氧化物的元素是________ (填元素名称),写出该元素的单质与⑨最高价氧化物的水化物反应的离子方程式____________________________________ 。
(3) ①、④、⑤、⑥、⑦、⑨六种元素的最高价氧化物的水化物中,按碱性减弱酸性增强的顺序排列为_____________________________________________ (用化学式表示)。
(4) ③元素与⑩元素两者核电荷数之差是_____________________________ 。
(5) 请写出②的氢化物发生催化氧化的化学方程式_______________________________ 。
(6) 请写出⑤元素的最高价氧化物与⑥元素的最高价氧化物的水化物反应的离子方程式___________________________________ 。
 主族 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1) 表中化学性质最不活泼的元素,其原子结构示意图为
(2) 表中能形成两性氢氧化物的元素是
(3) ①、④、⑤、⑥、⑦、⑨六种元素的最高价氧化物的水化物中,按碱性减弱酸性增强的顺序排列为
(4) ③元素与⑩元素两者核电荷数之差是
(5) 请写出②的氢化物发生催化氧化的化学方程式
(6) 请写出⑤元素的最高价氧化物与⑥元素的最高价氧化物的水化物反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】如表为元素周期表的一部分。
(1)表中元素___ 的非金属性最强;元素___ 的金属性最强;元素___ 的单质在室温下呈液态(填写元素符号)。
(2)表中元素③的原子结构示意图是___ 。
(3)表中元素⑥、⑦氢化物的稳定性顺序为___ >___ (填写化学式,下同)。
(4)表中元素最高价氧化物对应水化物酸性最强的酸的分子式是___ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ⑤ | |||||
| 3 | ③ | ⑥ | |||||
| 4 | ④ | ⑦ | |||||
(1)表中元素
(2)表中元素③的原子结构示意图是
(3)表中元素⑥、⑦氢化物的稳定性顺序为
(4)表中元素最高价氧化物对应水化物酸性最强的酸的分子式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】下表是ⅥA族部分元素的相关性质。
请回答下列问题:
(1)硒的熔点范围可能是_______ 。
(2)碲的化合价可能有_______ 。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是_______ (填化学式)。
(4)氢硒酸有较强的_______ (填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生的化学方程式为_______ 。
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:_______
_______Al2Te3+_______=2Al(OH)3↓+_______H2Te↑
| 元素 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
请回答下列问题:
(1)硒的熔点范围可能是
(2)碲的化合价可能有
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是
(4)氢硒酸有较强的
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
_______Al2Te3+_______=2Al(OH)3↓+_______H2Te↑
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据元素周期表回答下列问题。
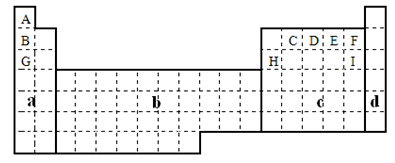
(1)在上面元素周期表中全部是金属元素的区域为___ 。
A.a B.b C.c D.d
(2)G元素与E元素形成的化合物的化学式是___ 、___ ,它们都是___ 。(填“共价化合物”或“离子化合物”)。表格中九种元素的最高价氧化物对应的水化物中,碱性最强的是___ (用化合物的化学式表示,下同),酸性最强的是__ ,属于两性氢氧化物的是___ ,写出此氢氧化物溶于强碱溶液的离子方程式___ 。
(3)①用元素符号将铁元素填写在上面元素周期表中对应的位置___ 。
②G、H两元素相比较,金属性较强的是___ (填名称),可以验证该结论的实验是___ 。(填编号)
(a)看哪种原子失去的电子越多,金属性越强。
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性

(1)在上面元素周期表中全部是金属元素的区域为
A.a B.b C.c D.d
(2)G元素与E元素形成的化合物的化学式是
(3)①用元素符号将铁元素填写在上面元素周期表中对应的位置
②G、H两元素相比较,金属性较强的是
(a)看哪种原子失去的电子越多,金属性越强。
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,请回答下列问题:(用元素符号或对应化学式回答问题)
(1) ④⑤⑥的原子半径由大到小的顺序为______
(2) ②③⑦的最高价含氧酸的酸性由强到弱的顺序为______
(3) ⑦⑧⑨的第一电离能由小到大的顺序为______
(4)比较④和⑨的氢化物的稳定性大小______ ,沸点高低______
(5)写出元素⑩的+1价含氧酸的结构式______
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
(1) ④⑤⑥的原子半径由大到小的顺序为
(2) ②③⑦的最高价含氧酸的酸性由强到弱的顺序为
(3) ⑦⑧⑨的第一电离能由小到大的顺序为
(4)比较④和⑨的氢化物的稳定性大小
(5)写出元素⑩的+1价含氧酸的结构式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】元素的金属性和非金属性强弱的判断方法
(1)元素的金属性强弱的判断方法
元素原子的________ 能力越强,元素的金属性越强,它的单质越容易_______ ,该元素的最高价氧化物对应水化物的_______ 越强。
(2)元素的非金属性强弱的判断方法
元素原子的_______ 能力越强,元素的非金属性越强,它的单质越容易________ ,气态氢化物的_________ 越强,该元素的最高价氧化物对应水化物的_________ 越强。
(1)元素的金属性强弱的判断方法
元素原子的
(2)元素的非金属性强弱的判断方法
元素原子的
您最近一年使用:0次
【推荐2】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素:

(1)K的元素名称为___________ 。
(2)基态时Q元素原子的电子排布式___________ ,
(3)下列对比正确的是___________ 。
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(4)由P、A、C三种元素形成的某化合物,对氢气的相对密度为15,则该分子的键角约为___________ 。
(5)元素B和C的气态氢化物热稳定性较强的是___________ (填化学式)。

(1)K的元素名称为
(2)基态时Q元素原子的电子排布式
(3)下列对比正确的是
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(4)由P、A、C三种元素形成的某化合物,对氢气的相对密度为15,则该分子的键角约为
(5)元素B和C的气态氢化物热稳定性较强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】为探究元素性质递变规律,设计如下实验。
(1)填写各实验步骤对应的实验现象(选填相应序号;不重复选)。
A.剧烈反应,迅速产生大量无色气体。
B.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。
C.反应不十分剧烈;产生无色气体。
D.有气体产生,溶液变成浅红色。
(2)实验④:向1mL1mol/LAlCl3溶液中滴加2mol/LNaOH溶液至过量,观察生成白色胶状沉淀,继而沉淀消失。
请用离子 方程式解释该实验现象:________ 、________ 。
(3)实验⑤:在试管中加入3~5mLNa2SiO3溶液,逐滴加入稀硫酸,边加边振荡。观察试管中出现白色凝胶。相应化学方程式:________ ,证明酸性:____ ﹥____ (用化学式表示)。
(4)实验⑥:向新制得的Na2S溶液中滴加新制的氯水。观察试管中出现黄色沉淀。相应离子 方程式:________ ,证明氧化性:______ ﹥_____ (用化学式表示)。
通过以上实验和讨论,推断钠、镁、铝的金属性逐渐________ (选填“增强”或“减弱”),硅、硫、氯的非金属性逐渐________ (选填“增强”或“减弱”)。
(1)填写各实验步骤对应的实验现象(选填相应序号;不重复选)。
| 实验序号 | 实验步骤 | 实验现象 |
| ① | 将一小块金属钠放入滴有酚酞溶液的冷水中。 | |
| ② | 将磨去表面氧化膜的一小段镁条放入试管中,加入2mL水,滴入2滴酚酞溶液,加热至水沸腾。 | |
| ③ | 将磨去表面氧化膜的一小段镁条投入2mL1mol/L盐酸中。 | |
| ④ | 将磨去表面氧化膜的一小片铝投入2mL1mol/L盐酸中。 |
A.剧烈反应,迅速产生大量无色气体。
B.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。
C.反应不十分剧烈;产生无色气体。
D.有气体产生,溶液变成浅红色。
(2)实验④:向1mL1mol/LAlCl3溶液中滴加2mol/LNaOH溶液至过量,观察生成白色胶状沉淀,继而沉淀消失。
请用
(3)实验⑤:在试管中加入3~5mLNa2SiO3溶液,逐滴加入稀硫酸,边加边振荡。观察试管中出现白色凝胶。相应化学方程式:
(4)实验⑥:向新制得的Na2S溶液中滴加新制的氯水。观察试管中出现黄色沉淀。相应
通过以上实验和讨论,推断钠、镁、铝的金属性逐渐
您最近一年使用:0次