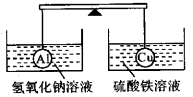
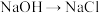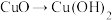能与Fe3+反应,且能证明Fe3+具有氧化性的是
①SCN-;②Fe;③Fe2+;④Cu;⑤I-;⑥OH-;⑦Cl2
①SCN-;②Fe;③Fe2+;④Cu;⑤I-;⑥OH-;⑦Cl2
| A.①②④ | B.②④⑤ | C.①③⑥ | D.②⑤⑦ |
更新时间:2016-12-29 14:32:16
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】根据表中信息,判断下列叙述中不正确的是
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① |  |  |  |  |  |
| ② |  |  | / |  | |
| ③ |  |  |  |  |  |
A.氧化性: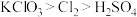 |
| B.由第①组的信息可知,氧化产物与还原产物的物质的量之比为1:1 |
C.第②组反应过程中,消耗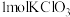 得 得 电子 电子 |
D.第③组反应的离子方程式为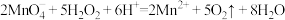 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列叙述正确的是
| A.浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气后都首先发生置换反应 |
| B.XCl3的溶液能与铜片发生反应,则铜的金属性一定比X强 |
| C.非金属X能将Fe氧化到+3价,但非金属Y不能,则Y的氧化性一定比X强 |
| D.Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化 |
您最近半年使用:0次
【推荐3】稀土金属是我国重要的战略资源。稀土金属铈(Ce)性质活泼,常见的化合价为+3和+4,可发生如下反应:①2CeO2+H2O2+6H+=2Ce3++O2+4H2O②H2O2+2I-+2H+=I2+2H2O③I2+SO2+2H2O=4H++2I-+ 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是| A.氧化性由强到弱的顺序是CeO2>H2O2>I2 |
| B.还原性由强到弱的顺序是I->SO2>Ce3+ |
| C.反应2CeO2+2I-+8H+=2Ce3++I2+4H2O可以进行 |
| D.H2O2在反应①中被氧化,在反应②中被还原 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是物质间发生化学反应的颜色变化,下表选项中的物质对应正确的是
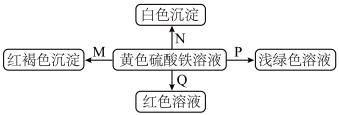

| 选项 | M | N | P | Q |
| A |  |  | 铜 | 石蕊溶液 |
| B | Na |  |  |  |
| C |  |  | 锌粉 |  |
| D |  |  | Fe | 石蕊溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验过程中的颜色变化,与氧化还原反应无关的是
| A.向FeSO4溶液中加入NaOH溶液,先产生白色沉淀,然后迅速变成灰绿色,最后变成红褐色 |
| B.向NaBr溶液中滴入少量氯水,溶液变为黄色 |
| C.向CuSO4溶液中逐滴加入氨水,先有蓝色沉淀生成,后沉淀溶解得到深蓝色的溶液 |
| D.将FeCl3溶液滴在淀粉—KI试纸上,试纸变蓝 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路(已知发生的反应为 2FeCl3+ Cu =2FeCl2+ CuCl2)。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取100 mL废液加入足量的AgNO3溶液,生成沉淀 86.1g。(2)另取100 mL废液放入铜片充分反应,铜片质量减少了2.56 g。下列关于原废液组成的判断错误的是
| A.c(Fe2+)︰c(Fe3+)︰c(Cu2+) = 2︰1 ︰1 |
| B.c(Fe2+)︰c(Cu2+) = 2︰1 |
| C.一定含有Fe 2+、Fe 3+、Cu2+、Clˉ |
| D.c(Clˉ) = 6mol / L,c(Fe 2+) =1.2mol / L |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】二氧化硫是形成酸雨的罪魁祸首之一,含硫煤燃烧的尾气处理一直是化学研究的重要课题。某工厂设计了新的治污方法,该工艺流程如图所示,下列叙述不正确的是( )
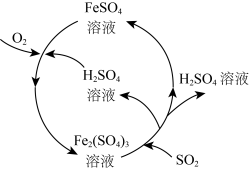

A.该过程中可得到化工产品 |
B.该工艺流程中 可以循环利用 可以循环利用 |
C.若处理含 的尾气,理论上需要通入相同条件下的空气约 的尾气,理论上需要通入相同条件下的空气约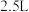 |
| D.可用澄清石灰水检验最终排出的气体是否含有二氧化硫 |
您最近半年使用:0次