现有几种元素的性质或原子结构如下表:
(1)工业制备X单质反应的化学方程式_______________________________ ;
(2)画出T的离子结构示意图__________ ;
(3)写出实验室利用浓盐酸和二氧化锰制取单质Z的离子方程式______________________ ;
(4)由T和Y两种元素组成的一种阴阳离子个数比为1:2的过氧化物,其电子式为___________ 。写出该物质的一种用途__________________________________
(5)T、Z的最高价氧化物对应的水化物相互反应的离子方程式为___________________ 。
| 元素编号 | 元素性质或原子结构 |
| T | 失去一个电子后,形成Ne原子电子层结构 |
| X | 短周期非金属,其最外层电子数是次外层电子数的一半 |
| Y | 其单质之一是空气中主要成分,最常见的助燃剂 |
| Z | 形成双原子单质分子,黄绿色气体 |
(2)画出T的离子结构示意图
(3)写出实验室利用浓盐酸和二氧化锰制取单质Z的离子方程式
(4)由T和Y两种元素组成的一种阴阳离子个数比为1:2的过氧化物,其电子式为
(5)T、Z的最高价氧化物对应的水化物相互反应的离子方程式为
更新时间:2017-03-19 21:12:27
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F、G、L、I九种主族元素分别位于三个不同的短周期,它们的原子序数依次增大,其中B、C、D位于同一周期,A与E、B与G、D与L分别位于同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F最外层电子数的2倍,C和D的最外层电子数之和为11.请回答下列问题:
(1)元素B在周期表中的位置___________ ,,以上元素中非金属所形成的最简单气态氢化物稳定性最弱的是(填化学式)___________ ,D、E、F、L所形成的简单离子的半径由大到小的顺序为(用离子符号表示)___________ 。
(2)L、I两元素可按原子个数比1:1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的结构式为___________ 。
(3)CI3常温下呈液态,可与水反应生成一种酸和一种碱,反应方程式为___________ 。
(4)固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生,写出该反应的化学方程式___________ 。
(1)元素B在周期表中的位置
(2)L、I两元素可按原子个数比1:1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的结构式为
(3)CI3常温下呈液态,可与水反应生成一种酸和一种碱,反应方程式为
(4)固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知a~f是原子序数依次增大前四周期的六种元素,a元素原子核外电子只有一种自旋取向;b元素原子最高能级的不同轨道都有电子且自旋方向相同;c元素原子的价层电子排布为 ,d元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;e与d的最高能层数相同,但其价电子层电子数等于其电子层数;f元素原子最外层只有1个电子,次外层内的所有轨道的电子均成对。请回答下列问题(答题时涉及a~f元素,要用元素符号表示):
,d元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;e与d的最高能层数相同,但其价电子层电子数等于其电子层数;f元素原子最外层只有1个电子,次外层内的所有轨道的电子均成对。请回答下列问题(答题时涉及a~f元素,要用元素符号表示):
(1)d其原子核外电子共有___________ 种空间运动状态;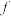 属于
属于___________ 区元素。
(2)b、c、d、e四种元素第一电离能由大到小的顺序为___________ 。
(3)与e元素处于对角线位置的第二周期元素的氢氧化物与 元素的最高价氧化物对应水化物反应的离子方程式为
元素的最高价氧化物对应水化物反应的离子方程式为___________ 。
(4) 能与
能与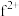 形成
形成 配离子,而
配离子,而 不能形成
不能形成 配离子,其原因是
配离子,其原因是___________ 。
(5)过渡金属离子与水分子形成的配合物是否有颜色,与其 轨道电子排布有关。一般而言,为
轨道电子排布有关。一般而言,为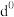 或
或 排布时,无颜色;为
排布时,无颜色;为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
___________ 颜色(填“无”或“有”)。
 ,d元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;e与d的最高能层数相同,但其价电子层电子数等于其电子层数;f元素原子最外层只有1个电子,次外层内的所有轨道的电子均成对。请回答下列问题(答题时涉及a~f元素,要用元素符号表示):
,d元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;e与d的最高能层数相同,但其价电子层电子数等于其电子层数;f元素原子最外层只有1个电子,次外层内的所有轨道的电子均成对。请回答下列问题(答题时涉及a~f元素,要用元素符号表示):(1)d其原子核外电子共有
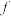 属于
属于(2)b、c、d、e四种元素第一电离能由大到小的顺序为
(3)与e元素处于对角线位置的第二周期元素的氢氧化物与
 元素的最高价氧化物对应水化物反应的离子方程式为
元素的最高价氧化物对应水化物反应的离子方程式为(4)
 能与
能与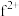 形成
形成 配离子,而
配离子,而 不能形成
不能形成 配离子,其原因是
配离子,其原因是(5)过渡金属离子与水分子形成的配合物是否有颜色,与其
 轨道电子排布有关。一般而言,为
轨道电子排布有关。一般而言,为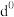 或
或 排布时,无颜色;为
排布时,无颜色;为 排布时,有颜色,如
排布时,有颜色,如 显粉红色。据此判断,
显粉红色。据此判断,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】如图中A、B、C、D是同周期或同主族的相邻元素:
(1)已知:A元素的最低价为-3价,它的最高价氧化物含氧56.34%,原子核内中子数比质子数多1个,则A元素原子的质量数为_____ 。
(2)写出元素符号:A_____ ,C_____ ,D____ 。
(3)A、B、C三种元素最高价氧化物的水化物中酸性最强的是____ (填化学式)。
(4)B、D两种元素和氢组成的气态氢化物中稳定性最强的是___ ,还原性最强的____ (填化学式)。
| D | ||
| A | B | C |
(1)已知:A元素的最低价为-3价,它的最高价氧化物含氧56.34%,原子核内中子数比质子数多1个,则A元素原子的质量数为
(2)写出元素符号:A
(3)A、B、C三种元素最高价氧化物的水化物中酸性最强的是
(4)B、D两种元素和氢组成的气态氢化物中稳定性最强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E都是短周期元素,原子半径D>C>A>E>B,其中A、B处在同一周期,A、C处在同一主族。C原子核内质子数等于A、B原子核内质子数之和,C原子最外层上的电子数是D原子最外层电子数的4倍,且D为金属。试回答:
(1)C的元素名称为_________ 。
(2)在五种元素中,能形成的最简单的液态或气态氢化物的稳定性由大到小的顺序是(用具体的分子式表示)______________ 。
(3)A与B形成的三原子分子的结构式是______ ,B与D形成的原子个数比为1∶1的化合物的电子式是______ 。
(4)请写出一个由以上5种元素中部分元素形成的物质,发生置换反应方程式______________
(1)C的元素名称为
(2)在五种元素中,能形成的最简单的液态或气态氢化物的稳定性由大到小的顺序是(用具体的分子式表示)
(3)A与B形成的三原子分子的结构式是
(4)请写出一个由以上5种元素中部分元素形成的物质,发生置换反应方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去):
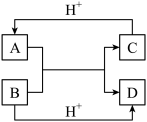
(1)若A、B、C、D均是10电子粒子,请写出A、D的化学式:A___ ;D___ 。
(2)若A和C均是18电子粒子,且A为阴离子,B和D均是10电子粒子,则A与B在溶液中反应的离子方程式为___ 。

(1)若A、B、C、D均是10电子粒子,请写出A、D的化学式:A
(2)若A和C均是18电子粒子,且A为阴离子,B和D均是10电子粒子,则A与B在溶液中反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F是原子序数依次增大的六种常见元素,其中A原子最外层电子数比次外层电子数多2个电子;B的阴离子与C的阳离子电子数之和为20,质子数相差3;E2、EB2均是生活生产中常见的杀菌消毒剂;气体DB2中D的质量分数为50%;A与F形成一种化合物M可与水反应生成一种可燃性的直线型分子N。根据以上信息回答下列问题:
(1)用一个反应方程式说明D与E的非金属性强弱关系___________________________ 。
(2)M的电子式___________________________________________________ 。
(3)汽车安全气囊中的叠氮化钠NaN3可用次氯酸钠溶液销毁,写出反应的化学方程式:______________________ ,每生成1molN2,转移的电子数为_____________________________ 。
(4)自来水厂常用EB2对饮用水进行杀菌消毒,处理后的水中要求EB2的残留的浓度为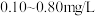 ,一般可用碘量法对其进行检测,现操作步骤如下:
,一般可用碘量法对其进行检测,现操作步骤如下:
Ⅰ、取1L水样加硫酸酸化,向其中加入足量的KI溶液,充分反应后,用NaOH溶液调节溶液至中性,加入淀粉溶液。
Ⅱ、用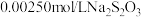 溶液滴定Ⅰ所得溶液,测得所用体积为
溶液滴定Ⅰ所得溶液,测得所用体积为
①步骤Ⅰ中EB2与碘化钾溶液反应的离子方程式为___________________________________ 。
②滴定终点的现象_________________________________________________________ 。
③步骤Ⅰ中调节溶液至中性的原因是________________________________________ 。
④该水样中EB2的浓度为______________________________ mg/L。(保留到小数点后两位)
(1)用一个反应方程式说明D与E的非金属性强弱关系
(2)M的电子式
(3)汽车安全气囊中的叠氮化钠NaN3可用次氯酸钠溶液销毁,写出反应的化学方程式:
(4)自来水厂常用EB2对饮用水进行杀菌消毒,处理后的水中要求EB2的残留的浓度为
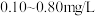 ,一般可用碘量法对其进行检测,现操作步骤如下:
,一般可用碘量法对其进行检测,现操作步骤如下:Ⅰ、取1L水样加硫酸酸化,向其中加入足量的KI溶液,充分反应后,用NaOH溶液调节溶液至中性,加入淀粉溶液。
Ⅱ、用
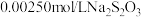 溶液滴定Ⅰ所得溶液,测得所用体积为
溶液滴定Ⅰ所得溶液,测得所用体积为
①步骤Ⅰ中EB2与碘化钾溶液反应的离子方程式为
②滴定终点的现象
③步骤Ⅰ中调节溶液至中性的原因是
④该水样中EB2的浓度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
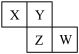
【推荐1】X、Y、Z、W、Q、E、R是7种短周期元素。已知X、Y、Z、W在周期表中相对位置如图所示,且W原子最外层电子数是其内层电子数的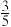 ,Q元素组成的单质是最理想的气体燃料,E的原子最外层电子数是次外层电子数的3倍,R的单质通常用于自来水的消毒。
,Q元素组成的单质是最理想的气体燃料,E的原子最外层电子数是次外层电子数的3倍,R的单质通常用于自来水的消毒。
请回答下列问题:
(1)E在周期表中的位置是______ ;R的单质与镁形成的化合物电子式为____ 。
(2)由X和Q组成的一种气体,其密度与相同条件下的Y单质密度相同,则该气体使溴水褪色的化学方程式为__________ ;该反应类型为_______ 。
(3)关于以上元素说法正确的是_______ (填字母)。
a.Y的最简单氢化物分解比Z的难
b.X元素是自然界中能形成化合物种类最多的元素,是因为X在自然界含量最丰富
c.R的单质通常用于自来水的消毒是因为该单质有毒性,可以“以毒攻毒”
d.Z的一种单质可用于制火柴
(4)可利用如图装置(烧瓶B下面的加热装置未画出)验证元素非金属性的强弱关系。

现用药品Na2S溶液、浓盐酸、MnO2来设计实验验证R的非金属性强于W,则:实验中能够说明R的非金属性强于W的主要现象是__________ ;B中反应离子方程式为________ 。
 ,Q元素组成的单质是最理想的气体燃料,E的原子最外层电子数是次外层电子数的3倍,R的单质通常用于自来水的消毒。
,Q元素组成的单质是最理想的气体燃料,E的原子最外层电子数是次外层电子数的3倍,R的单质通常用于自来水的消毒。
请回答下列问题:
(1)E在周期表中的位置是
(2)由X和Q组成的一种气体,其密度与相同条件下的Y单质密度相同,则该气体使溴水褪色的化学方程式为
(3)关于以上元素说法正确的是
a.Y的最简单氢化物分解比Z的难
b.X元素是自然界中能形成化合物种类最多的元素,是因为X在自然界含量最丰富
c.R的单质通常用于自来水的消毒是因为该单质有毒性,可以“以毒攻毒”
d.Z的一种单质可用于制火柴
(4)可利用如图装置(烧瓶B下面的加热装置未画出)验证元素非金属性的强弱关系。

现用药品Na2S溶液、浓盐酸、MnO2来设计实验验证R的非金属性强于W,则:实验中能够说明R的非金属性强于W的主要现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,表中的一个序号代表一种元素。某种融雪剂在机场、高速公路等地被广泛使用,该融雪剂的主要成分是由下表中部分元素(①~①)组成的化合物A(化学式为 )。Y、X、Z、M的原子序数依次递增,Y与M位于同一主族,X的最外层电子数是电子层数的2倍,Z是地壳中含量最多的元素,含元素M的物质在酒精灯外焰上灼烧呈紫色火焰。请结合信息回答下列问题。
)。Y、X、Z、M的原子序数依次递增,Y与M位于同一主族,X的最外层电子数是电子层数的2倍,Z是地壳中含量最多的元素,含元素M的物质在酒精灯外焰上灼烧呈紫色火焰。请结合信息回答下列问题。
(1)A的化学式为___________ ,该化合物中存在的化学键类型有___________ ;元素M在周期表中位置为___________ 。
(2)X、Z和③的原子半径由大到小的顺序为___________ (用元素符号表示)。
(3)⑥的单质在④的单质中燃烧的现象为___________ ,生成物的电子式为___________ 。
(4)⑥⑦①三种元素的氢氧化物,碱性由强到弱的顺序为___________ (填化学式)。
(5)元素⑨的单质和元素⑩的最高价氧化物的水化物反应的离子方程式为___________ 。
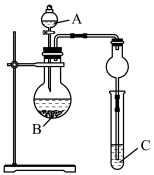
(6)我们可以利用如图装置通过实验比较元素②和⑧的非金属性强弱;从下列选项中选出实验所需的物质(已知: 不溶于水):
不溶于水):
a.稀盐酸 b.稀硫酸
c.碳酸钙 d. 溶液
溶液
试剂A为___________ (填字母,下同);试剂C为___________ 。请指出该装置存在的一个缺陷:___________ 。
 )。Y、X、Z、M的原子序数依次递增,Y与M位于同一主族,X的最外层电子数是电子层数的2倍,Z是地壳中含量最多的元素,含元素M的物质在酒精灯外焰上灼烧呈紫色火焰。请结合信息回答下列问题。
)。Y、X、Z、M的原子序数依次递增,Y与M位于同一主族,X的最外层电子数是电子层数的2倍,Z是地壳中含量最多的元素,含元素M的物质在酒精灯外焰上灼烧呈紫色火焰。请结合信息回答下列问题。| 族 周期 | Ⅰ A | 0 | |||||||
| 1 | ① | Ⅱ A | Ⅲ A | Ⅳ A | Ⅴ A | Ⅵ A | Ⅶ A | ||
| 2 | ② | ③ | ④ | ⑤ | |||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | |||||
| 4 | ⑩ | ||||||||
(2)X、Z和③的原子半径由大到小的顺序为
(3)⑥的单质在④的单质中燃烧的现象为
(4)⑥⑦①三种元素的氢氧化物,碱性由强到弱的顺序为
(5)元素⑨的单质和元素⑩的最高价氧化物的水化物反应的离子方程式为
(6)我们可以利用如图装置通过实验比较元素②和⑧的非金属性强弱;从下列选项中选出实验所需的物质(已知:
 不溶于水):
不溶于水):
a.稀盐酸 b.稀硫酸
c.碳酸钙 d.
 溶液
溶液试剂A为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】元素周期表是化学发展史上的重要里程碑之一。“价-类”二维图有助于认识物质之间的转化,更有利于提升对元素周期表的认识。
(1)元素周期表共有_______ 个周期。其中氮元素在周期表中的位置是_______ 。
(2)在放电或高温下,空气中的N2会转化为HNO3,过程如下图。
N2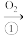 NO
NO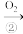 NO2
NO2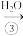 HNO3
HNO3
其中属于固氮的转化是_______ 。(选填上图中编号)写出③的化学方程式_______ 。
(3)检验硝酸铵固体中铵根离子的方法为_______ 。
(4)对“N”“P”元素及其化合物相关性质进行比较,下列说法不正确的是_______。
下图是某元素的“价-类”二维图:
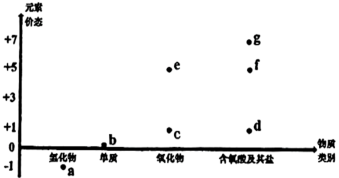
(5)已知该元素是第3周期元素,此元素是_______ (填写元素符号),画出该元素的原子结构示意图_______ 。
(6)有同学猜测向含d的含氧酸根离子的溶液中加入含a的浓溶液,能产生_______(选填编号)。
(7)从元素化合价角度分析能发生上述反应的原因_______ 。
(1)元素周期表共有
(2)在放电或高温下,空气中的N2会转化为HNO3,过程如下图。
N2
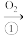 NO
NO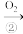 NO2
NO2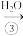 HNO3
HNO3其中属于固氮的转化是
(3)检验硝酸铵固体中铵根离子的方法为
(4)对“N”“P”元素及其化合物相关性质进行比较,下列说法不正确的是_______。
| A.原子半径大小:P<N |
| B.原子得电子的能力:P<N |
| C.气态氢化物的热稳定性:PH3<NH3 |
| D.最高价氧化物对应水化物的酸性:H3PO4<HNO3 |
下图是某元素的“价-类”二维图:

(5)已知该元素是第3周期元素,此元素是
(6)有同学猜测向含d的含氧酸根离子的溶液中加入含a的浓溶液,能产生_______(选填编号)。
| A.b | B.e | C.f | D.g |
您最近一年使用:0次



