以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如右图所示:
回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为________________ 。
(2)当25℃时,Kw=1.0×10-14,Kb(NH3·H2O)=1.75×105。(NH4)2SO4溶液呈酸性,其原因是(用力方程式解释):__________ ;该离子方程式的平衡常数K约为______ (填具体数字)。
(3)如何检验中和液中的杂质离子已完全除尽_________ 。
(4)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为__________ 。
(5)综上分析,流程图中M的主要成分的化学式为________ ,M可用一种物质吸收以实现循环利用,该物质的名称是_________ 。
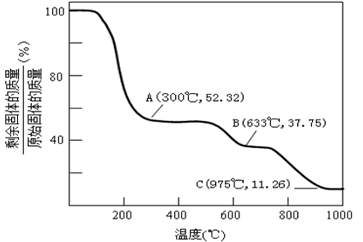
(6)固体NH4Al(SO4)2.12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体成分的化学式为_____________ 。

回答下列问题:
(1)氧化步骤中发生的主要反应的离子方程式为
(2)当25℃时,Kw=1.0×10-14,Kb(NH3·H2O)=1.75×105。(NH4)2SO4溶液呈酸性,其原因是(用力方程式解释):
(3)如何检验中和液中的杂质离子已完全除尽
(4)NH4Al(SO4)2溶液与过量NaOH溶液混合加热,反应的化学方程式为
(5)综上分析,流程图中M的主要成分的化学式为
(6)固体NH4Al(SO4)2.12H2O在加热时,固体残留率随温度的变化如图所示。633℃时剩余固体成分的化学式为
更新时间:2017-03-20 16:56:45
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按下列要求填空
①向碳酸氢钙溶液中加入少量氢氧化钠溶液的离子方程式:________________________ 。
氯化铝溶液与NaHCO3溶液混合的离子方程式:_____________________________________ 。
②在KClO3+ 6HCl =" KCl" + 3Cl2↑ + 3H2O的反应中,被氧化的氯原子与被还原的氯原子的物质的量之比是_______________ 。
③强酸性的未知无色溶液中可能含有大量的Cl-、S2-、NO3-、CO32-、NH4+、Cu2+、Fe3+、Ag+等,现已检出有Ag+,你认为其中____________ 离子还需要鉴定是否存在,请写出检验该离子的离子方程式_____________________ 。
④某化合物的相对分子质量为m,在t℃时AmL该化合物的饱和溶液为Bg,将其蒸干后得到固体Cg。该化合物在t℃时的溶解度为____________ g,该饱和溶液中溶质的物质的量浓度为___________ mol/L。
①向碳酸氢钙溶液中加入少量氢氧化钠溶液的离子方程式:
氯化铝溶液与NaHCO3溶液混合的离子方程式:
②在KClO3+ 6HCl =" KCl" + 3Cl2↑ + 3H2O的反应中,被氧化的氯原子与被还原的氯原子的物质的量之比是
③强酸性的未知无色溶液中可能含有大量的Cl-、S2-、NO3-、CO32-、NH4+、Cu2+、Fe3+、Ag+等,现已检出有Ag+,你认为其中
④某化合物的相对分子质量为m,在t℃时AmL该化合物的饱和溶液为Bg,将其蒸干后得到固体Cg。该化合物在t℃时的溶解度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】向盛有CuSO4溶液的试管中加入少量氨水,现象是_______ ;继续添加氨水,得到深蓝色透明溶液,该步骤的离子方程式为_______ ;若要得到深蓝色晶体,需进行的操作是_______ ,所得晶体的化学式为_______ 。AgCl沉淀也能溶解在氨水中,生成的配合物中配体的空间结构名称为_______ ,Ag+的配位数是_______ ,继续向溶液中加入足量HNO3溶液,观察到的现象是_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
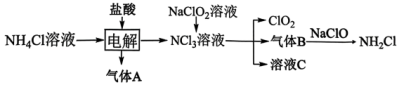
【推荐1】二氧化氯(黄绿色易溶于水的气体)是绿色消毒剂,实验室用如图方法制备 :
:
(1) 与
与 在溶液中恰好反应生成
在溶液中恰好反应生成 的离子方程式为
的离子方程式为_______ 。
(2)下列说法正确的是_______。
(3)写出 与水反应的化学方程式
与水反应的化学方程式_______ 。
(4) 、
、 、
、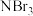 的沸点由高到低的顺序是
的沸点由高到低的顺序是_______ ,你的理由是_______ 。
(5)假设 恰好完全反应,气体全部逸出,设计实验检验溶液C中所有阴离子
恰好完全反应,气体全部逸出,设计实验检验溶液C中所有阴离子_______ 。
 :
:
(1)
 与
与 在溶液中恰好反应生成
在溶液中恰好反应生成 的离子方程式为
的离子方程式为(2)下列说法正确的是_______。
A.气体A是 |
B. 消毒是通过缓慢释放的HClO作用的,其消毒的持久力强 消毒是通过缓慢释放的HClO作用的,其消毒的持久力强 |
C.电解的阳极方程式为: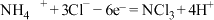 |
D.除去 中的气体B可用碱石灰,也能用无水氯化钙 中的气体B可用碱石灰,也能用无水氯化钙 |
 与水反应的化学方程式
与水反应的化学方程式(4)
 、
、 、
、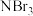 的沸点由高到低的顺序是
的沸点由高到低的顺序是(5)假设
 恰好完全反应,气体全部逸出,设计实验检验溶液C中所有阴离子
恰好完全反应,气体全部逸出,设计实验检验溶液C中所有阴离子
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解。
(1)已知Na2S2O5中O元素的化合价为-2,则S元素的化合价为_______ 。Na2S2O5在酸性条件下会放出SO2,其反应的离子方程式为_______ 。
(2)Na2S2O5是一种食品添加剂、Na2S2O5晶体中常含有 。
。
①Na2S2O5作脱氧剂时的反应原理为 ,用单线桥法标出该反应中电子转移的数目和方向:
,用单线桥法标出该反应中电子转移的数目和方向:_______ 。
②检验其中含有 的方法是
的方法是_______ 。
(3)葡萄酒中常加入Na2S2O5作抗氧化剂。测定某葡萄酒中Na2S2O5残留量的实验方法如下:取20.00mL葡萄酒样品,慢慢滴加5.00mL0.010mol/LI2标准液恰好反应(以淀粉溶液作指示剂)。已知实验过程中发生的反应为 。计算该葡萄酒中Na2S2O5的残留量为
。计算该葡萄酒中Na2S2O5的残留量为_______ mol/L。
(1)已知Na2S2O5中O元素的化合价为-2,则S元素的化合价为
(2)Na2S2O5是一种食品添加剂、Na2S2O5晶体中常含有
 。
。①Na2S2O5作脱氧剂时的反应原理为
 ,用单线桥法标出该反应中电子转移的数目和方向:
,用单线桥法标出该反应中电子转移的数目和方向:②检验其中含有
 的方法是
的方法是(3)葡萄酒中常加入Na2S2O5作抗氧化剂。测定某葡萄酒中Na2S2O5残留量的实验方法如下:取20.00mL葡萄酒样品,慢慢滴加5.00mL0.010mol/LI2标准液恰好反应(以淀粉溶液作指示剂)。已知实验过程中发生的反应为
 。计算该葡萄酒中Na2S2O5的残留量为
。计算该葡萄酒中Na2S2O5的残留量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有失去标签的四瓶无色溶液分别为Na2CO3溶液、稀盐酸、Ba(OH)2溶液、NaHSO4溶液,为确定四瓶溶液分别是什么,将其随意标号为A、B、C、D,分别取少量溶液两两混合,产生的现象如下表所示。
已知:NaHSO4属于酸式盐,在水溶液中的电离方程式为:NaHSO4 = Na+ + H+ + SO42- 。
根据实验现象,回答下列问题:
(1)A为 ,C为 。
(2)写出下列反应的离子方程式
A + B ,A + D ,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为 ,反应后得到的溶液中含有的阴离子有 。
(4)上述没有明显变化的实验④、⑥,其中 发生了离子反应,离子方程式为 。请设计实验证明其发生了反应 。(试剂任选)
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A + B | 生成白色沉淀 |
| ② | A + C | 放出无色气体 |
| ③ | A + D | 放出无色气体 |
| ④ | B + C | 无明显变化 |
| ⑤ | B + D | 生成白色沉淀 |
| ⑥ | C + D | 无明显变化 |
已知:NaHSO4属于酸式盐,在水溶液中的电离方程式为:NaHSO4 = Na+ + H+ + SO42- 。
根据实验现象,回答下列问题:
(1)A为 ,C为 。
(2)写出下列反应的离子方程式
A + B ,A + D ,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为 ,反应后得到的溶液中含有的阴离子有 。
(4)上述没有明显变化的实验④、⑥,其中 发生了离子反应,离子方程式为 。请设计实验证明其发生了反应 。(试剂任选)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】研究性学习小组用化学方法测量一个不规则容器的体积,测量过程如下:
称取7.5gCuSO4·5H2O晶体放入500mL烧杯中,加入150mL蒸馏水。待晶体完全溶解、冷却后,将溶液全部转移到容器中,用蒸馏水稀释到完全充满容器,从中取出溶液l00mL ,该溶液恰好与20mL 0.1mol/L BaCl2溶液完全反应。
(1)求100mL CuSO4 溶液的物质的量浓度_______ ;
(2)试计算该容器的体积__________ 。
称取7.5gCuSO4·5H2O晶体放入500mL烧杯中,加入150mL蒸馏水。待晶体完全溶解、冷却后,将溶液全部转移到容器中,用蒸馏水稀释到完全充满容器,从中取出溶液l00mL ,该溶液恰好与20mL 0.1mol/L BaCl2溶液完全反应。
(1)求100mL CuSO4 溶液的物质的量浓度
(2)试计算该容器的体积
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】为测试一铁片中铁元素的含量,某课外活动小组提出下面两种方案并进行了实验(以下数据为多次平行实验测定结果的平均值):
方案一:将ag铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580 mL(标准状况);
方案二:将a/10g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.020 00 mol·L-1的KMnO4溶液滴定,达到终点时消耗了25.00 mL KMnO4溶液。
请回答下列问题:
(1)配平下面的化学方程式:__________________________
 KMnO4+
KMnO4+ FeSO4+
FeSO4+ H2SO4===
H2SO4=== Fe2(SO4)3+
Fe2(SO4)3+ MnSO4+
MnSO4+ K2SO4+
K2SO4+ H2O
H2O
(2)在滴定实验中不能选择________ 式滴定管,理由是______________ ;
(3)根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为________ 和________ ;
(4)若排除实验仪器和操作的影响因素,试对上述两种方案测定结果的准确性做出判断和分析。
①方案一________ (填“准确”、“不准确”或“不一定准确”),理由是____________ ;
②方案二________ (填“准确”、“不准确”或“不一定准确”),理由是_____________ 。
方案一:将ag铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580 mL(标准状况);
方案二:将a/10g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.020 00 mol·L-1的KMnO4溶液滴定,达到终点时消耗了25.00 mL KMnO4溶液。
请回答下列问题:
(1)配平下面的化学方程式:
 KMnO4+
KMnO4+ FeSO4+
FeSO4+ H2SO4===
H2SO4=== Fe2(SO4)3+
Fe2(SO4)3+ MnSO4+
MnSO4+ K2SO4+
K2SO4+ H2O
H2O(2)在滴定实验中不能选择
(3)根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为
(4)若排除实验仪器和操作的影响因素,试对上述两种方案测定结果的准确性做出判断和分析。
①方案一
②方案二
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】十九大报告提出要对环境问题进行全面、系统的可持续治理。回答下列问题:
Ⅰ.浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的装置如下图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。
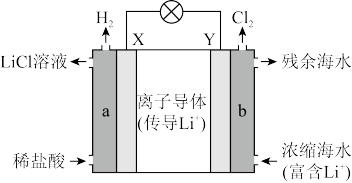
(1)X极为_______ 极,Y极电极反应式:_______ 。
(2)Y极生成1mol 时,
时,_______ mol 移向
移向_______ (填“X”或“Y”)极。
Ⅱ.汽车普遍使用的铅酸蓄电池放电时总反应式为 。
。
(3)当外电路通过1 mol电子时,理论上负极板的质量比正极板的质量多增加_______ g,电池中消耗的硫酸物质的量为_______ mol。
Ⅲ.标准状况下,1.68L某气态烃在足量氧气中完全燃烧。若将产物通入足量澄清石灰水中,得到白色沉淀质量为15g;若用足量碱石灰吸收燃烧产物,增重9.3g。
(4)燃烧产物中水的质量为_______ g。
(5)若原气体是单一气体,则其电子式为_______ ,若将该气体设计成碱性(KOH)燃料电池,请写出负极电极反应式_______ 。
Ⅰ.浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的装置如下图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

(1)X极为
(2)Y极生成1mol
 时,
时, 移向
移向Ⅱ.汽车普遍使用的铅酸蓄电池放电时总反应式为
 。
。(3)当外电路通过1 mol电子时,理论上负极板的质量比正极板的质量多增加
Ⅲ.标准状况下,1.68L某气态烃在足量氧气中完全燃烧。若将产物通入足量澄清石灰水中,得到白色沉淀质量为15g;若用足量碱石灰吸收燃烧产物,增重9.3g。
(4)燃烧产物中水的质量为
(5)若原气体是单一气体,则其电子式为
您最近一年使用:0次



