下表是元素周期表的一部分元素,用元素符号或化学式回答下列问题:
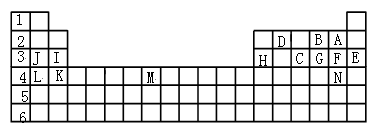
① 表中用字母标出的14种元素中,化学性质最不活泼的是________ ,主族元素中金属性最强的是_______ ,常温下单质为液态的非金属元素是_______ ;属于过渡元素的是_________ 。
②C、G、F气态氢化物的稳定性顺序是______________________ 。
③第三周期中原子半径最小的元素是_______ 。

① 表中用字母标出的14种元素中,化学性质最不活泼的是
②C、G、F气态氢化物的稳定性顺序是
③第三周期中原子半径最小的元素是
更新时间:2017-03-29 12:36:06
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
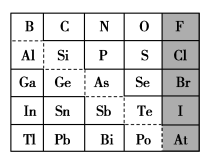
(1)Si的最高化合价为_______ ,Cl的最高价氧化物对应的水化物的化学式为_______ ,Bi的最高价氧化物的化学式为_______ 。
(2)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是_______ 元素(填元素符号)。
②酸性:
_______ (填“>”“<”或“=”,下同) 。
。
③氢化物的还原性:
_______  。
。
(3)N的氢化物和它的最高价含氧酸反应的化学方程式_______ 。

(1)Si的最高化合价为
(2)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是
②酸性:

 。
。③氢化物的还原性:

 。
。(3)N的氢化物和它的最高价含氧酸反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】结合元素周期表回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界______ 。
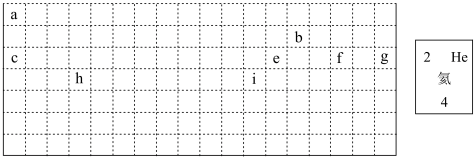
(2)表中所列元素,属于短周期元素的有______ (用元素符号回答),属于主族元素的有______ (用元素符号回答)。
(3)g元素位于第______ 周期第______ 族;i元素位于第______ 周期第______ 族。
(4)元素f是第______ 周期第______ 族元素,请按氦元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量_________ 。
(5)写出b元素的基态原子的电子排布式______ ,写出h元素的符号______ ,该原子的价层电子排布图______ 。
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界

(2)表中所列元素,属于短周期元素的有
(3)g元素位于第
(4)元素f是第
(5)写出b元素的基态原子的电子排布式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】元素周期表是指导我们系统学习化学的重要工具。(答案都填写化学式)
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图__ ,自然界中存在的54Fe和56Fe,它们互称为___ 。将铁片放入冷浓硫酸中,片刻后将铁片移入硫酸铜溶液中,发现铁片表面无明显变化,原因是__ 。通常证明某溶液中含Fe2+的化学方法是___ 。
下表是元素周期表的一部分:

(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的__ 相同。处于同一列的N和P位于元素周期表的__ 族。
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为_ ,其气态氢化物的结构式为__ 。
②与硅元素处于同一周期,两性金属元素是__ ,并写出其在元素周期表中的位置:第__ 周期,__ 族,该元素的最高价氧化物对应水化物的电离方程式为__ 。
③第三周期半径最大的金属元素__ ,该元素形成氢氧化物的电子式_ ,检验物质中是否含有该元素的方法是:__ 。
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是__ (写化学式)。该元素与硫元素相比,非金属性较强的元素是__ (填元素符号),请写出证明该结论的一个实验事实:__ 。
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是___ 。

a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第__ 族,又有人提议可将它放在周期表中第IVA族,这样建议的原因是__ 。
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的__ (选填序号)。
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
(1)如图是铁元素在元素周期表中的有关信息。

写出Fe的原子结构示意图
下表是元素周期表的一部分:

(2)从原子结构角度分析,C、N、O、F四种元素处于同一行,是由于它们的
(3)通过元素周期表,我们可以知道:
①氮元素的最低化合价为
②与硅元素处于同一周期,两性金属元素是
③第三周期半径最大的金属元素
④在上表所列元素的最高价氧化物对应水化物中酸性最强的是
⑤如图,将潮湿的Cl2单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是

a.浓硫酸 b.NaOH溶液 c.KI溶液 d.饱和食盐水
⑥由于氢元素的化合价,有人提议还可以将其放在第
⑦科学家通过对某些元素的化合价进行研究,寻找高效农药。这些元素往往位于元素周期表的
a.左下角区域 b.右上角区域 c.左上角区域 d.右下角区域
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求作答:
(1)写出下列微粒的电子式
Na+:___ ;S2-:___ ;NH3:___ ;Na2O2:___ ;HClO:___ 。
(2)用电子式表示下列化合物的形成过程
NaCl:___ ;HF:___ 。
(3)同主族从上到下:原子半径逐渐____ (填“增大”或“减小”);金属性逐渐____ (填“增强”或“减弱”,下同);最高价氧化物对应水化物碱性___ 。同周期从左到右:原子半径逐渐___ (填“增大”或“减小”);非属性逐渐___ (填“增强”或“减弱”,下同);最高价氧化物对应水化物酸性___ ;简单氢化物稳定性逐渐___ 。
(1)写出下列微粒的电子式
Na+:
(2)用电子式表示下列化合物的形成过程
NaCl:
(3)同主族从上到下:原子半径逐渐
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素在周期表中的位置反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。回答下列问题:
(1)N在元素周期表中的位置为第__________ 周期__________ 族。根据元素周期律,预测酸性强弱:
______ (填“>”或“<”) 。
。
(2)S的最高化合价和最低化合价的代数和为_______ ,Se与 的反应比S与
的反应比S与 的反应
的反应______ (填“难”或“易”)。
(3) 具有较强的氧化性,
具有较强的氧化性, 具有较强的还原性,将
具有较强的还原性,将 气体通入溴水后,溶液中主要存在的离子是
气体通入溴水后,溶液中主要存在的离子是________ (填离子符号)。
(4)下列说法错误的是___________ (填序号)。
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③由元素周期律可直接推断出酸性:
④HF、HCl、HBr、HI的稳定性逐渐减弱
| C | N | O | F | ||
| Si | P | S | Cl | ||
| Ge | As | Se | Br | ||
| Sn | Sb | Te | I | ||
| Pb | Bi | Po | At |

 。
。(2)S的最高化合价和最低化合价的代数和为
 的反应比S与
的反应比S与 的反应
的反应(3)
 具有较强的氧化性,
具有较强的氧化性, 具有较强的还原性,将
具有较强的还原性,将 气体通入溴水后,溶液中主要存在的离子是
气体通入溴水后,溶液中主要存在的离子是(4)下列说法错误的是
①C、N、O、F的原子半径随着原子序数的增大而减小
②Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
③由元素周期律可直接推断出酸性:

④HF、HCl、HBr、HI的稳定性逐渐减弱
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。如图是元素周期表的一部分,回答下列问题。
(1)周期表呈现的短周期元素中,次外层电子数等于其他电子层电子数之和的元素是_______ (写原子结构示意图);上述周期表呈现的元素中,金属性最强的元素在周期表中处于第_______ 周期第_______ 族。
(2)Sn的最高正价为_______ ,写出Cl的最高价氧化物对应水化物的化学式_______ 。
(3)比较微粒半径大小:Al_______ F;
_______  (选填“>”或“<”)。
(选填“>”或“<”)。
(4)元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。
①以下关于碱金属,说法不正确的是_______ 。
A.随电子层数增多,原子半径逐渐增大
B.随着核电荷数的增加,离子的氧化性逐渐增强
C.钾与氧气或水反应比钠的反应剧烈,也比铷、铯的反应更剧烈
D.原子易失去电子,呈现+1价
②原子数相同、价电子总数相同的粒子互称为等电子体。Y、Q是上述周期表中短周期元素,元素相关信息见下表。
硼元素与Y、Q形成互为等电子体负离子: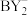 、
、 ,则m值为
,则m值为_______ 。
| B | C | N | O | F |
| Al | Si | P | S | Cl |
| Ga | Ge | As | Se | Br |
| In | Sn | Sb | Te | I |
(2)Sn的最高正价为
(3)比较微粒半径大小:Al

 (选填“>”或“<”)。
(选填“>”或“<”)。(4)元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。
①以下关于碱金属,说法不正确的是
A.随电子层数增多,原子半径逐渐增大
B.随着核电荷数的增加,离子的氧化性逐渐增强
C.钾与氧气或水反应比钠的反应剧烈,也比铷、铯的反应更剧烈
D.原子易失去电子,呈现+1价
②原子数相同、价电子总数相同的粒子互称为等电子体。Y、Q是上述周期表中短周期元素,元素相关信息见下表。
| Q | 与H可形成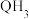 的10电子结构分子 的10电子结构分子 |
| Y | 带两个负电荷的负离子与氖原子结构相同 |
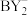 、
、 ,则m值为
,则m值为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表是ⅥA族部分元素的相关性质。
请回答下列问题:
(1)硒的熔点范围可能是______________________ 。
(2)碲的化合价可能有______________________ 。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是________ (填化学式)。
(4)氢硒酸有较强的________ (填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生的化学方程式为_______________________________________ 。
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
________ Al2Te3+( ) ===2Al(OH)3↓+________ H2Te↑
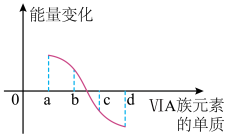
(6)氧族元素单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表________ ,d代表________ (均写单质名称)。
元素 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1 390 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热 化合 | 加热 难化合 | 不能直 接化合 |
请回答下列问题:
(1)硒的熔点范围可能是
(2)碲的化合价可能有
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是
(4)氢硒酸有较强的
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
(6)氧族元素单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示氧族中某一元素的单质。则b代表

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)原子序数11-17的元素,自钠到氯,电子层数相同,最外层电子数从_______ 增加到_______ ,随着核电荷数依次递增,原子半径依次_______ ,核对外层电子的引力逐渐_______ ,失电子能力逐渐_______ ,得电子能力逐渐_______ ,因此,金属性逐渐_______ ,非金属性逐渐_______ 。
(2)元素金属性的强弱,可以从它的单质及水或酸反应置换氢的_______ 程度,以及它的最高价氧化物的水化物的_______ 强弱来判断。元素非金属性的强弱,可以从它的最高价氧化物的水化物的_______ 强弱,或它的单质跟H2生成气态氢化物的_______ 及氢化物的_______ 来判断。
(2)元素金属性的强弱,可以从它的单质及水或酸反应置换氢的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】钠、铝等金属及其材料在人类文明进步和社会发展中发挥了重要的作用。
(1)请用一个离子方程式说明钠与铝的金属性强弱___________ 。
(2)叠氮化钠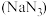 是一种无色结晶,其固体中正负离子的个数比为
是一种无色结晶,其固体中正负离子的个数比为 ,则该固体中含有的化学键是
,则该固体中含有的化学键是___________ (填化学键名称)。叠氮化钠受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32L(标准状况下)氮气,至少需要叠氮化钠___________ g。
(3)在含0.1molNaOH的溶液中不断地通入 ,得到溶质的质量为8.35g,则烧杯中生产的溶质是
,得到溶质的质量为8.35g,则烧杯中生产的溶质是___________ 。溶质的物质的量是___________ 。
(4)高锰酸根离子 水对人体危害极大,可用过碳酸钠
水对人体危害极大,可用过碳酸钠 改性赤泥进行处理,反应如下:
改性赤泥进行处理,反应如下:
___________ ___________
___________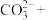 ___________
___________ ___________
___________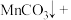 ___________
___________ ___________
___________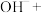 ___________H2O
___________H2O
补全并配平上述化学反应过程式___________ ;反应中,过碳酸钠起沉淀剂和___________ 剂作用;若将1L含Mn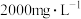 的含高锰酸根离子的废水处理至含Mn
的含高锰酸根离子的废水处理至含Mn ,则转移电子数为
,则转移电子数为___________ mol(保留2位小数)。
(1)请用一个离子方程式说明钠与铝的金属性强弱
(2)叠氮化钠
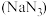 是一种无色结晶,其固体中正负离子的个数比为
是一种无色结晶,其固体中正负离子的个数比为 ,则该固体中含有的化学键是
,则该固体中含有的化学键是(3)在含0.1molNaOH的溶液中不断地通入
 ,得到溶质的质量为8.35g,则烧杯中生产的溶质是
,得到溶质的质量为8.35g,则烧杯中生产的溶质是(4)高锰酸根离子
 水对人体危害极大,可用过碳酸钠
水对人体危害极大,可用过碳酸钠 改性赤泥进行处理,反应如下:
改性赤泥进行处理,反应如下:___________
 ___________
___________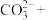 ___________
___________ ___________
___________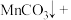 ___________
___________ ___________
___________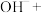 ___________H2O
___________H2O补全并配平上述化学反应过程式
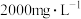 的含高锰酸根离子的废水处理至含Mn
的含高锰酸根离子的废水处理至含Mn ,则转移电子数为
,则转移电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。
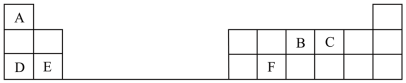
请填写下列空白:
(1)A与B形成 的电子式为
的电子式为________ ;C的原子结构示意图为________ 。
(2)B的最高价氧化物对应的水化物的化学式为_______ ;D、E的最高价氧化物对应的水化物中碱性较弱的是_______  用化学式表示
用化学式表示 ;
;
(3)F的氧化物与氢氧化钠溶液反应的离子方程式为______________ 。

请填写下列空白:
(1)A与B形成
 的电子式为
的电子式为(2)B的最高价氧化物对应的水化物的化学式为
 用化学式表示
用化学式表示 ;
; (3)F的氧化物与氢氧化钠溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期律反映了元素性质的周期性变化规律。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最弱的是_____ (填化学式)。
(2)氮氧化铝(AlON)是一种高硬度、耐高温的防弹材料,Al、O、N三种元素的简单离子半径由大到小的排列顺序是_____ 。
(3)锡为主族元素,其原子结构示意图: 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是_____ ,SnO2能与NaOH溶液反应生成钠盐(Na2SnO3)和水,写出发生反应的化学方程式:_____ 。
(4)硒(34Sn)是与人类的健康密切相关的一种元素,工业上用浓H2SO4焙烧CuSe的方法提取硒(其中Cu转化为CuSO4),且有SO2、H2O和SeO2(固体)生成,写出发生反应的化学方程式:_____ 。理论上该反应每转移1mol电子,可得到的SeO2的质量为_____ g。
(1)元素的性质,特别是化学性质取决于元素的原子结构。钠、镁、铝元素形成的最高价氧化物对应的水化物中,碱性最弱的是
(2)氮氧化铝(AlON)是一种高硬度、耐高温的防弹材料,Al、O、N三种元素的简单离子半径由大到小的排列顺序是
(3)锡为主族元素,其原子结构示意图:
 。锡在元素周期表中的位置是
。锡在元素周期表中的位置是(4)硒(34Sn)是与人类的健康密切相关的一种元素,工业上用浓H2SO4焙烧CuSe的方法提取硒(其中Cu转化为CuSO4),且有SO2、H2O和SeO2(固体)生成,写出发生反应的化学方程式:
您最近一年使用:0次



