A、B、C、D、E、F、G为原子序数依次增大的短周期主族元素。B、C、D均能与A形成10电子分子,E单质可用于焊接钢轨,F与D同主族,F与G同周期。
(1)F的离子结构示意图为___________ 。
(2)D、E、F的离子半径由大到小的顺序为__________________ (填离子符号)。
(3)写出能证明G比F非金属性强的一个化学方程式______________________ 。
(4)F和G的一种化合物甲中所有原子均为8电子稳定结构,该化合物与水反应生成F单质、F的最高价含氧酸和G的氢化物,三种产物的物质的量之比为2:1:6,甲的电子式为_________ ,该反应的化学方程式为__________________ 。
(5)C能分别与A和D按原子个数比1:2形成化合物乙和丙,乙的结构式为_________________ 。常温下,液体乙与气体丙反应生成两种无污染的物质,若共生成1mol产物时放热QkJ,该反应的热化学方程式为__________________ 。
(6)现取100mL 1mol/L的E的氯化物溶液,向其中加入1mol/L氢氧化钠溶液产生了3.9g沉淀,则加入的氢氧化钠溶液体积可能为________________ mL。
(1)F的离子结构示意图为
(2)D、E、F的离子半径由大到小的顺序为
(3)写出能证明G比F非金属性强的一个化学方程式
(4)F和G的一种化合物甲中所有原子均为8电子稳定结构,该化合物与水反应生成F单质、F的最高价含氧酸和G的氢化物,三种产物的物质的量之比为2:1:6,甲的电子式为
(5)C能分别与A和D按原子个数比1:2形成化合物乙和丙,乙的结构式为
(6)现取100mL 1mol/L的E的氯化物溶液,向其中加入1mol/L氢氧化钠溶液产生了3.9g沉淀,则加入的氢氧化钠溶液体积可能为
更新时间:2017-03-28 22:13:39
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
【推荐1】CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,.发生反应2S2(g)+CH4(g) CS2(g)+2H2S(g)。回答下列问题:
CS2(g)+2H2S(g)。回答下列问题:
(1)CH4的电子式为___ 。
(2)某温度下,若S8完全分解成气态S2。在恒温密闭容器中,S2与CH4物质的量比为2:1时开始反应。
①当CS2的体积分数为10%时,CH4的转化率为___ 。
②当以下数值不变时.能说明该反应达到平衡的是___ (填字母标号)。
a.气体密度 b.气体总压 c.CH4与S2体积比 d.CS2的体积分数
(3)一定条件下,CH4与S2反应中CH4的平衡转化率、S8分解产生S2的体积分数随温度的变化曲线如图所示。据图分析,生成CS2的反应为___ (填“放热”或“吸热”)反应。工业上通常采用在600~650℃的条件下进行此反应,不采用低于600℃的原因是___ 。

(4)用燃煤废气(含N2、O2、SO2、CO2、H2O、NOx等)使尾气中的H2S转化为单质硫S,可实现废物利用,保护环境,写出其中一个反应的化学方程式___ 。
 CS2(g)+2H2S(g)。回答下列问题:
CS2(g)+2H2S(g)。回答下列问题:(1)CH4的电子式为
(2)某温度下,若S8完全分解成气态S2。在恒温密闭容器中,S2与CH4物质的量比为2:1时开始反应。
①当CS2的体积分数为10%时,CH4的转化率为
②当以下数值不变时.能说明该反应达到平衡的是
a.气体密度 b.气体总压 c.CH4与S2体积比 d.CS2的体积分数
(3)一定条件下,CH4与S2反应中CH4的平衡转化率、S8分解产生S2的体积分数随温度的变化曲线如图所示。据图分析,生成CS2的反应为

(4)用燃煤废气(含N2、O2、SO2、CO2、H2O、NOx等)使尾气中的H2S转化为单质硫S,可实现废物利用,保护环境,写出其中一个反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】研究小组为探究固体X(含五种元素的盐)的性质,设计并完成如下实验。
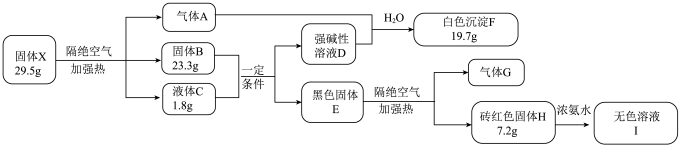
已知:固体B是纯净物,溶液I呈强碱性,溶质的阳离子为二配位的配离子。
请回答:
(1)A的电子式为_______ ,E中所含金属的元素符号是_______ ,X的化学式是_______ 。
(2)写出固体B与液体C反应的化学方程式_______ 。
(3)写出H和浓氨水反应转化为I的离子反应方程式_______ 。
(4)设计实验检验D中的离子_______ 。

已知:固体B是纯净物,溶液I呈强碱性,溶质的阳离子为二配位的配离子。
请回答:
(1)A的电子式为
(2)写出固体B与液体C反应的化学方程式
(3)写出H和浓氨水反应转化为I的离子反应方程式
(4)设计实验检验D中的离子
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】肼(N2H4)是一种可燃性液体,可用作火箭燃料。
(1)N2H4分子中氮原子均达到8电子稳定结构,写出N2H4的电子式____ ;H2O2是一种绿色氧化剂,当它与肼反应时生成两种无污染物质,该反应的化学方程式为___ 。
(2)以Cl2、NaOH和尿素[(NH2)2CO]为原料可制备水合肼(N2H4•H2O),其主要实验流程如图:
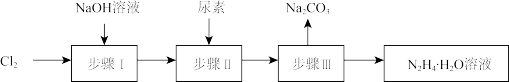
①步骤I制备NaClO溶液,写出该反应的离子方程式____ ;反应中放出大量的热,若温度超过 ,Cl2会与NaOH溶液反应生成NaClO3。为防止NaClO3的生成,实验中可采取的措施是
,Cl2会与NaOH溶液反应生成NaClO3。为防止NaClO3的生成,实验中可采取的措施是___ 。
②步骤III分离得到N2H4•H2O溶液样品.为测定所得样品中N2H4•H2O的含量,采用以下实验步骤。
I.取5.00mL样品配制成250mL溶液,取该溶液10.00mL于锥形瓶内,加20mL蒸馏水、1mL1mol·L-1硫酸、NaHCO3约1g15.00mL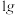 0.1000mol·L-1碘标准溶液,振荡。
0.1000mol·L-1碘标准溶液,振荡。
II.向锥形瓶内加入适量___ 作指示剂,用0.05000mol·L-1的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液12.00mL。
已知:N2H4•H2O+2I2+H2SO4+6NaHCO3=N2↑+6CO2↑+Na2SO4+4NaI+7H2O
I2+2Na2S2O3=Na2S2O4+2NaI
计算试样中N2H4•H2O的物质的量浓度____ (写出计算过程)。
(1)N2H4分子中氮原子均达到8电子稳定结构,写出N2H4的电子式
(2)以Cl2、NaOH和尿素[(NH2)2CO]为原料可制备水合肼(N2H4•H2O),其主要实验流程如图:

①步骤I制备NaClO溶液,写出该反应的离子方程式
 ,Cl2会与NaOH溶液反应生成NaClO3。为防止NaClO3的生成,实验中可采取的措施是
,Cl2会与NaOH溶液反应生成NaClO3。为防止NaClO3的生成,实验中可采取的措施是②步骤III分离得到N2H4•H2O溶液样品.为测定所得样品中N2H4•H2O的含量,采用以下实验步骤。
I.取5.00mL样品配制成250mL溶液,取该溶液10.00mL于锥形瓶内,加20mL蒸馏水、1mL1mol·L-1硫酸、NaHCO3约1g15.00mL
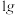 0.1000mol·L-1碘标准溶液,振荡。
0.1000mol·L-1碘标准溶液,振荡。II.向锥形瓶内加入适量
已知:N2H4•H2O+2I2+H2SO4+6NaHCO3=N2↑+6CO2↑+Na2SO4+4NaI+7H2O
I2+2Na2S2O3=Na2S2O4+2NaI
计算试样中N2H4•H2O的物质的量浓度
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐1】下表标出的是元素周期表的一部分元素,回答下列问题:

(1)第三周期中原子半径最小的是___________ 。(用元素符号表示)
(2)表中用字母标出的15种元素中,化学性质最不活泼的是___________ (用元素符号表示),金属性最强的是___________ ,(用元素符号表示)非金属性最强的是___________ ,(用元素符号表示)属于过渡元素的是___________ (用字母表示)。
(3)d,e,f气态氢化物最稳定的为___________ , 最不稳定的为___________ 。(填化学式)
(4)钛被称为继铁、铝之后的第三金属,钛元素在元素周期表中的位置为___________ ,其价电子排布式为___________ 。
(5)请画出26号元素其价电子排布图:___________ 。
(6)d与a反应的产物的分子中心原子的杂化形式为___________ ,该分子是___________ (填“极性”或“非极性”)分子。
(7)写出铜元素在周期表中的位置___________ ,它位于___________ 区。并写出Cu+ 基态电子排布式___________ 。
(8)o、p两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态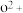 再失去一个电子比气态
再失去一个电子比气态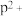 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是___________
(9)元素X的某价态阴离子Xn-中所有电子正好充满K和L电子层,CnX的晶体结构如图所示。
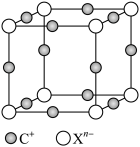
该晶体中阳离子和阴离子个数比为___________ ,晶体中每个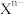 被
被___________ 个等距离的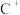 包围。
包围。

(1)第三周期中原子半径最小的是
(2)表中用字母标出的15种元素中,化学性质最不活泼的是
(3)d,e,f气态氢化物最稳定的为
(4)钛被称为继铁、铝之后的第三金属,钛元素在元素周期表中的位置为
(5)请画出26号元素其价电子排布图:
(6)d与a反应的产物的分子中心原子的杂化形式为
(7)写出铜元素在周期表中的位置
(8)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p | |
| 电离能/kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 |
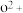 再失去一个电子比气态
再失去一个电子比气态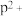 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是(9)元素X的某价态阴离子Xn-中所有电子正好充满K和L电子层,CnX的晶体结构如图所示。

该晶体中阳离子和阴离子个数比为
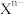 被
被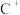 包围。
包围。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】A、B、C、D、E、F、G七种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成分子X,X的水溶液呈碱性;A、D同主族,D的焰色反应为黄色;E的简单阳离子与X具有相同电子数,且E是同周期中简单离子半径最小的元素;F元素的原子最外层比次外层少两个电子,C、G两种元素的原子最外层共有13个电子。则
(1)F在元素周期表中的位置为_______________ 。
(2)在2 L的密闭容器中,充入2 mol B2和3 mol A2,在一定条件下发生反应,5 s后测得A2为1.8 mol,则以B2的表示的反应速率v(B2)为__________________________ 。
(3)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为_______________ 。
(4)D2F溶液在空气中长期放置发生反应,生成一种强碱与D2F2。D2F2与过氧化钠的结构和化学性质相似,其溶液显黄色。D2F2的电子式为_______ ,写出D2F在空气中长期放置生成D2F2的化学反应方程式为:_____________ 。D2F2的溶液与稀硫酸反应产生的现象为_____________ 。
(5)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol A4B4熔融电离生成两种离子各1mol,则该物质熔融时的电离方程式为____________ 。
(6)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。
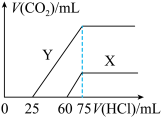
则曲线Y表明M中的溶质为________ ;原NaOH溶液的物质的量浓度为_______ ;由曲线X、Y可知,两次实验通入的CO2的体积比为_________ 。
(1)F在元素周期表中的位置为
(2)在2 L的密闭容器中,充入2 mol B2和3 mol A2,在一定条件下发生反应,5 s后测得A2为1.8 mol,则以B2的表示的反应速率v(B2)为
(3)常温下,液态的B2A4与气态的BC2两者发生反应生成无毒物质,16g B2A4发生反应放热akJ,该反应的热化学方程式为
(4)D2F溶液在空气中长期放置发生反应,生成一种强碱与D2F2。D2F2与过氧化钠的结构和化学性质相似,其溶液显黄色。D2F2的电子式为
(5)化学家发现一种化学式为A4B4的离子化合物,一定条件下1mol A4B4熔融电离生成两种离子各1mol,则该物质熔融时的电离方程式为
(6)向30mL某浓度由A、B、C、D中三种元素形成一元强碱溶液通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体V(CO2)与加入盐酸的体积V[HCl(aq)]的关系有下列图示两种情况(不计CO2的溶解)。

则曲线Y表明M中的溶质为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】短周期元素X、Y、Z、W、R原子序数依次增大,W原子次外层电子数比最外层电子数多2个,X与R同主族,其中部分元素的原子半径和主要化合价如下表所示:
请回答下列问题:
(1)W元素在元素周期表中的位置为___________ 。
(2)Y元素最高价氧化物水化物的溶液与Z的氧化物反应的离子方程式为___________ 。
(3)W、R元素最高价氧化物水化物的酸性较强的为___________ (用化学式表示),从原子结构角度解释原因___________ 。
(4)化合物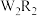 、
、 (所有原子均满足8电子结构)在工业生产中有广泛用途,
(所有原子均满足8电子结构)在工业生产中有广泛用途,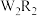 的电子式为
的电子式为___________ ;在一定条件下, 与
与 反应生成
反应生成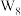 、
、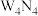 和一种仅由非金属元素组成的离子化合物,该离子化合物为
和一种仅由非金属元素组成的离子化合物,该离子化合物为___________ (填化学式)。
(5)化合物 可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。
可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。 与
与 反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为
反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为___________ 。
| N | X | Y | Z | |
| 原子半径/pm | 75 | 71 | 186 | 143 |
| 主要化合价 | / | —1 | +1 | +3 |
(1)W元素在元素周期表中的位置为
(2)Y元素最高价氧化物水化物的溶液与Z的氧化物反应的离子方程式为
(3)W、R元素最高价氧化物水化物的酸性较强的为
(4)化合物
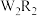 、
、 (所有原子均满足8电子结构)在工业生产中有广泛用途,
(所有原子均满足8电子结构)在工业生产中有广泛用途,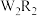 的电子式为
的电子式为 与
与 反应生成
反应生成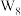 、
、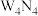 和一种仅由非金属元素组成的离子化合物,该离子化合物为
和一种仅由非金属元素组成的离子化合物,该离子化合物为(5)化合物
 可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。
可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。 与
与 反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为
反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】几种短周期元素的原子半径及化合价见下表:
分析上表中有关数据,结合已学过的知识,回答以下问题。
涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中的位置是___________ 。
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)____________ 。
(3)用电子式表示A与I所形成化合物的形成过程__________________ 。
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为__________________ ;
(5)用B与D所形成的化合物的化学式为__________________ ,属于___________ 晶体。
元素代号 | A | B | D | E | G | H | I | J |
化合价 | -1 | -2 | +4、-4 | +6、-2 | +5、-3 | +3 | +2 | +1 |
原子半径/nm | 0.071 | 0.074 | 0.130 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中的位置是
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)
(3)用电子式表示A与I所形成化合物的形成过程
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为
(5)用B与D所形成的化合物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】已知X、Y、Z、W四种元素分别是元素周期表中三个连续短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z 原子的最外层电子数之和。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)上述元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为___________ ,含有离子键和非极性共价键的化合物的电子式为_______________________ ;含有极性共价键和非极性共价键的化合物的电子式为____________________ 。
(2)由X、Y、Z所形成的常见离子化合物是_________________________ (写化学式),该化合物与[W的最高价氧化物对应水化物的浓溶液加热时反应的离子方程式为_________ 。
(1)上述元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为
(2)由X、Y、Z所形成的常见离子化合物是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】现有部分元素的性质或原子结构信息如表,据此回答下列问题:
(1)元素X的基态原子核外共有________ 种空间运动状态不同的电子,元素X与H元素形成的化合物是当今重要的能源,该化合物的电子式为________ 。
(2)元素Y的价电子排布图为________________ ,元素Y与元素T相比,电负性较大的是________ (用元素符号表示)。
(3)元素Z与元素T相比,非金属性强的是________ (用元素符号表示),下列表述中能证明这一事实的是________ 。
a.常温下Z的单质和T的单质状态不同
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
b.Z的氢化物比T的氢化物稳定
d.最高价氧化物对应水化物的酸性Z的比T的酸性强
(4)W的价电子排布式为________ ,稳定性比较:W3+________ W2+(填“>”或“<”),原因是__________________________________________________________________________ 。
元素编号 | 元素性质或原子结构 |
T | M层上有2对成对电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物的水溶液显碱性 |
Z | 短周期元素最高正化合价是+7价 |
W | 3d能级电子数是最外层电子数的3倍 |
(1)元素X的基态原子核外共有
(2)元素Y的价电子排布图为
(3)元素Z与元素T相比,非金属性强的是
a.常温下Z的单质和T的单质状态不同
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
b.Z的氢化物比T的氢化物稳定
d.最高价氧化物对应水化物的酸性Z的比T的酸性强
(4)W的价电子排布式为
您最近一年使用:0次



