现有部分元素的性质或原子结构信息如表,据此回答下列问题:
(1)元素X的基态原子核外共有________ 种空间运动状态不同的电子,元素X与H元素形成的化合物是当今重要的能源,该化合物的电子式为________ 。
(2)元素Y的价电子排布图为________________ ,元素Y与元素T相比,电负性较大的是________ (用元素符号表示)。
(3)元素Z与元素T相比,非金属性强的是________ (用元素符号表示),下列表述中能证明这一事实的是________ 。
a.常温下Z的单质和T的单质状态不同
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
b.Z的氢化物比T的氢化物稳定
d.最高价氧化物对应水化物的酸性Z的比T的酸性强
(4)W的价电子排布式为________ ,稳定性比较:W3+________ W2+(填“>”或“<”),原因是__________________________________________________________________________ 。
元素编号 | 元素性质或原子结构 |
T | M层上有2对成对电子 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物的水溶液显碱性 |
Z | 短周期元素最高正化合价是+7价 |
W | 3d能级电子数是最外层电子数的3倍 |
(1)元素X的基态原子核外共有
(2)元素Y的价电子排布图为
(3)元素Z与元素T相比,非金属性强的是
a.常温下Z的单质和T的单质状态不同
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
b.Z的氢化物比T的氢化物稳定
d.最高价氧化物对应水化物的酸性Z的比T的酸性强
(4)W的价电子排布式为
更新时间:2017-03-29 12:55:07
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】前36号元素中的A、B、C、D、E、F的原子序数依次增大,只有前四种为短周期元素。A、B的原子核外s电子总数与p电子总数相等: C原子核外所有p轨道全满或半满: D元素的族序数与周期数的差为4;E是前四周期中电负性最小的元素:F在周期表的第七列。请根据以上相关信息,回答下列问题.
(1)A离子的电子共占据_____ 个轨道,A元素在自然界中的存在形态_____ (a 只有化合态、b只有游离态、c都可能)。
(2)某人画的B的电子排布图如图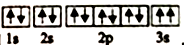 ,违背了
,违背了________ 原理。
(3)F位于______ 族,其基态原子的电子有_____ 种运动状态。
(4)CD3中心原子的杂化方式为____ ,用价层电子对互斥理论推测其分子空间构型为____ ,检验E元素的方法是___________ 。
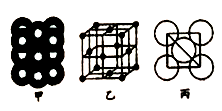
(5)若某金属单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.则晶胞中该原子的配位数为______ ,该单质晶体中原子的堆积方式为四种基本堆积方式中的________ ,若已知该金属的原子半径为dcm,NA代表阿伏伽德罗常数,金属的相对原子质量为M,则该晶体的密度为________ g/cm3(用字母表示)。
(1)A离子的电子共占据
(2)某人画的B的电子排布图如图
 ,违背了
,违背了(3)F位于
(4)CD3中心原子的杂化方式为
(5)若某金属单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.则晶胞中该原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】铁及其化合物是日常生活生产中应用广泛的材料。
(1)铁元素常见的离子有 和
和 ,稳定性
,稳定性
___________  (填“大于”“等于”或“小于”),
(填“大于”“等于”或“小于”), 的基态核外价电子排布式为
的基态核外价电子排布式为___________ 。
(2)某金属原子簇类配位化合物结构如图
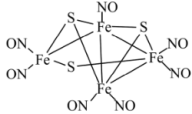
上述化合物中含有三种非金属元素,三种元素原子第一电离能由大到小顺序为___________ (用元素符号表示),中心原子铁的配位原子是___________ 。
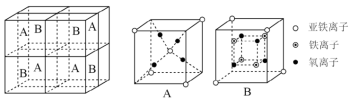
(3)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。该氧化物中 、
、 、
、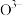 的个数比为
的个数比为___________ (填最简整数比)。
(4)铁有δ、γ、α三种同素异形体,如下图所示。
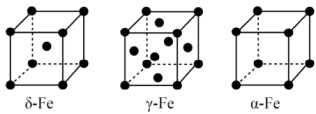
γ-Fe晶体的一个晶胞中所含有的铁原子数为___________ ,α-Fe、δ-Fe两种晶胞中铁原子的配位数之比为___________ 。
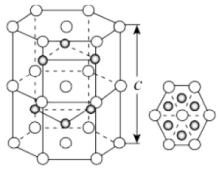
(5)Fe与S形成的一种化合物晶体的晶胞结构及其纵向投影如图所示,已知:晶体密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞六棱柱底面边长为
,晶胞六棱柱底面边长为 ,该晶胞的高c=
,该晶胞的高c=___________ pm(列出计算式)。
(1)铁元素常见的离子有
 和
和 ,稳定性
,稳定性
 (填“大于”“等于”或“小于”),
(填“大于”“等于”或“小于”), 的基态核外价电子排布式为
的基态核外价电子排布式为(2)某金属原子簇类配位化合物结构如图

上述化合物中含有三种非金属元素,三种元素原子第一电离能由大到小顺序为
(3)某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。该氧化物中
 、
、 、
、 的个数比为
的个数比为
(4)铁有δ、γ、α三种同素异形体,如下图所示。

γ-Fe晶体的一个晶胞中所含有的铁原子数为
(5)Fe与S形成的一种化合物晶体的晶胞结构及其纵向投影如图所示,已知:晶体密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞六棱柱底面边长为
,晶胞六棱柱底面边长为 ,该晶胞的高c=
,该晶胞的高c=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】已知A、B、C、D和E是原子序数依次增大前20号元素。A原子价电子层p轨道中只有1个电子;B、C、D元素的基态原子具有相同的能层数,B、D元素原子的p能级上都有1个未成对电子,D原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子;E是同周期第一电离能最小的元素。回答下列问题:
(1)B3+的结构示意图为______ ,C的最高价氧化物对应水化物与E的最高价氧化物对应水化物按物质的量1:1反应的离子方程式为__________ 。
(2)上述五种元素中碱性最强物质的电子式为_________ ; D所在周期第一电离能最大的元素是________ ;AD3是_________ 分子(填“极性”或“非极性”)
(3)B单质为面心立方晶体,晶胞中B原子的配位数为_________ .
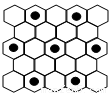
(4)石墨具有平面层状结构,同一层中的原子构成许许多多的正六边形,它与熔融的E单质相互作用,形成某种青铜色的物质(其中的元素E用“●”表示),原子分布如图所示,该物质的化学式为_________________ 。
(1)B3+的结构示意图为
(2)上述五种元素中碱性最强物质的电子式为
(3)B单质为面心立方晶体,晶胞中B原子的配位数为
(4)石墨具有平面层状结构,同一层中的原子构成许许多多的正六边形,它与熔融的E单质相互作用,形成某种青铜色的物质(其中的元素E用“●”表示),原子分布如图所示,该物质的化学式为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】A、B、C、D、E、F为短周期元素,非金属元素 最外层电子数与其周期数相同,
最外层电子数与其周期数相同, 的最外层电子数是其所在周期数的2倍。
的最外层电子数是其所在周期数的2倍。 在D中充分燃烧能生成其最高价化合物
在D中充分燃烧能生成其最高价化合物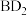 。
。 与
与 具有相同的电子数。
具有相同的电子数。 在
在 中燃烧,产物溶于水得到一种强酸。回答下列问题:
中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)写出一种实验室制备单质 的化学方程式
的化学方程式_______ 。
(2)B、D、E组成的一种盐中, 的质量分数为
的质量分数为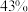 ,其俗名为
,其俗名为_______ ,其水溶液与少量 单质反应的化学方程式为
单质反应的化学方程式为_______ 。
(3)由这些元素组成的物质,其组成和结构信息如下表:
 的化学为
的化学为_______ ; 的化学式为
的化学式为_______  的电子式为
的电子式为_______ 。
(4)由A和B、D元素组成的两种二元化合物(含有两种不同元素)形成一类新能源物质。一种化合物分子通过_______ 构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为_______ 。
 最外层电子数与其周期数相同,
最外层电子数与其周期数相同, 的最外层电子数是其所在周期数的2倍。
的最外层电子数是其所在周期数的2倍。 在D中充分燃烧能生成其最高价化合物
在D中充分燃烧能生成其最高价化合物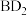 。
。 与
与 具有相同的电子数。
具有相同的电子数。 在
在 中燃烧,产物溶于水得到一种强酸。回答下列问题:
中燃烧,产物溶于水得到一种强酸。回答下列问题:(1)写出一种实验室制备单质
 的化学方程式
的化学方程式(2)B、D、E组成的一种盐中,
 的质量分数为
的质量分数为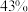 ,其俗名为
,其俗名为 单质反应的化学方程式为
单质反应的化学方程式为(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物 | 组成和结构信息 |
| a | 含有 的由两种元素形成的离子化合物 的由两种元素形成的离子化合物 |
| b | 含有非极性共价键的由两种元素形成的离子化合物,且原子数之比为 |
| c | 化学组成为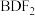 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
 的化学为
的化学为 的化学式为
的化学式为 的电子式为
的电子式为(4)由A和B、D元素组成的两种二元化合物(含有两种不同元素)形成一类新能源物质。一种化合物分子通过
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】甲是一种含结晶水的盐,由A、B、C、D、E五种原子序数依次增大的短周期元素组成。甲溶于水后可电离出三种离子,其中含有由A、B形成的10电子阳离子。B元素原子核内质子数比C的少1,C、E处于同主族。用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中,向其中加入稀盐酸,无现象。再加入BaCl2溶液,出现白色沉淀。
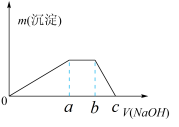
③取少量甲溶液于试管中逐滴滴入NaOH溶液,生成沉淀的质量与滴入NaOH溶液的体积关系如图所示。
(1)D的元素符号是___________ E在周期表中的位置是___________ 。
(2)B、C、E的简单气态氢化物的沸点高低顺序为___________ (用化学式表示,下同);相同条件下,等物质的量浓度的B和E的最高价氧化物对应的水化物的水溶液,pH较小的是___________ 。
(3)经测定甲晶体的摩尔质量为453 g/mol,其中阳离子和阴离子物质的量之比为 ,则甲晶体的化学式为
,则甲晶体的化学式为___________ 。
(4)实验③中根据图象得V(Oa):V(ab):V(bc)=___________ 。
(5)B的最高价氧化物对应的水化物的极稀的溶液,与D的单质反应时,还原产物可用作化肥,该物质溶于水时会吸热。写出该反应的离子方程式___________ 。
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中,向其中加入稀盐酸,无现象。再加入BaCl2溶液,出现白色沉淀。
③取少量甲溶液于试管中逐滴滴入NaOH溶液,生成沉淀的质量与滴入NaOH溶液的体积关系如图所示。

(1)D的元素符号是
(2)B、C、E的简单气态氢化物的沸点高低顺序为
(3)经测定甲晶体的摩尔质量为453 g/mol,其中阳离子和阴离子物质的量之比为
 ,则甲晶体的化学式为
,则甲晶体的化学式为(4)实验③中根据图象得V(Oa):V(ab):V(bc)=
(5)B的最高价氧化物对应的水化物的极稀的溶液,与D的单质反应时,还原产物可用作化肥,该物质溶于水时会吸热。写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】现有部分元素的性质与原子(或分子)结构如下表:
(1)写出这四种元素的元素符号:T_______ ;X_______ ;Y_______ ;Z_______ 。
(2)写出元素T的原子结构示意图_____________________________
(3)元素Y与元素Z相比,金属性较强的是________ (用元素符号表示),下列表述中能证明这一事实的是__________ (填序号)。
①Y单质的熔点比Z单质低 ②Y的化合价比Z低
③Y单质与水反应比Z单质剧烈 ④Y最高价氧化物的水化物的碱性比Z强
(4)X元素的气态氢化物与其最高价含氧酸反应的方程式为______________________
(5)元素T和氢元素以原子个数比1∶1化合形成化合物Q,元素X与氢元素以原子个数比1∶2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式________________________________________
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第三周期元素的简单离子中半径最小 |
(2)写出元素T的原子结构示意图
(3)元素Y与元素Z相比,金属性较强的是
①Y单质的熔点比Z单质低 ②Y的化合价比Z低
③Y单质与水反应比Z单质剧烈 ④Y最高价氧化物的水化物的碱性比Z强
(4)X元素的气态氢化物与其最高价含氧酸反应的方程式为
(5)元素T和氢元素以原子个数比1∶1化合形成化合物Q,元素X与氢元素以原子个数比1∶2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】随原子序数递增,x、y、z、……等八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示(已知:一般情况下当微粒电子层数相同时,核电荷数越大微粒半径越小;如半径: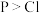 ,
, )
)

(1)g的离子结构示意图为_______ 。
(2)d、e、f、g、h的离子半径由大到小的顺序为_______ (填离子符号)。
(3)元素g位于周期表的第_______ 族,其非金属性比h弱,用原子结构的知识解释原因:_______ 。请写出能证明h比g非金属性强的一个化学方程式:_______ 。
(4)g的一种氧化物是形成酸雨的主要原因之一,工业上用z的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:_______ 。
(5)f和z组成的化合物fz,被大量用于制造电子元件。工业上用f的氧化物、y单质和z单质在高温下制备fz,其中f的氧化物和y单质的物质的量之比为1:3,则该反应的化学方程式为_______ 。
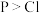 ,
, )
)
(1)g的离子结构示意图为
(2)d、e、f、g、h的离子半径由大到小的顺序为
(3)元素g位于周期表的第
(4)g的一种氧化物是形成酸雨的主要原因之一,工业上用z的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:
(5)f和z组成的化合物fz,被大量用于制造电子元件。工业上用f的氧化物、y单质和z单质在高温下制备fz,其中f的氧化物和y单质的物质的量之比为1:3,则该反应的化学方程式为
您最近一年使用:0次
【推荐2】现有部分元素的原子结构特点如表:
(1)画出W原子结构示意图________ 。
(2)元素X与元素Z相比,非金属性较强的是________ (填元素符号),写出一个能表示X、Z非金属性强弱关系的化学反应方程式_______________________ 。
(3)X、Y、Z、W四种元素形成的一种化合物,其水溶液显强酸性,该化合物的化学式为________ ,写出其在水溶液中的电离方程式____________________ 。
(4)元素X和元素Y以原子个数比1∶1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式__________________________ 。
| X | L层电子数是K层电子数的3倍 |
| Y | 核外电子层数等于原子序数 |
| Z | L层电子数是K层和M层电子数之和 |
| W | 共用三对电子形成双原子分子,常温下为气体单质 |
(2)元素X与元素Z相比,非金属性较强的是
(3)X、Y、Z、W四种元素形成的一种化合物,其水溶液显强酸性,该化合物的化学式为
(4)元素X和元素Y以原子个数比1∶1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C、D是中学常见的四种元素,原子序数依次增大,A的原子最外层电子数是次外层的2倍,B的氧化物属于两性氧化物,B、C位于同周期,A、B、C的原子最外层电子数之和为14,D是人体必需的微量元素,缺乏D会导致贫血症状。
(1)A在元素周期表中的位置是___________ 。
(2)下列事实能用元素周期律解释的是(填字母序号)___________ 。
a.B的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b.C的气态氢化物的稳定性小于HF
c.DC3的溶液可用于刻蚀铜制的印刷电路板
(3)画出B和C形成化合物的电子式___________ ,属于___________ 化合物(填“离子”或“共价”)
(4)工业上用电解法制备B的单质,反应的化学方程式为___________ 。
(5)D的单质可用于处理酸性废水中的NO ,使其转换为NH
,使其转换为NH ,同时生成有磁性的D的氧化物X,再进行后续处理。
,同时生成有磁性的D的氧化物X,再进行后续处理。
①上述反应的离子方程式为___________ ;
②B的单质与X在高温下反应的化学方程式为___________ 。
(1)A在元素周期表中的位置是
(2)下列事实能用元素周期律解释的是(填字母序号)
a.B的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b.C的气态氢化物的稳定性小于HF
c.DC3的溶液可用于刻蚀铜制的印刷电路板
(3)画出B和C形成化合物的电子式
(4)工业上用电解法制备B的单质,反应的化学方程式为
(5)D的单质可用于处理酸性废水中的NO
 ,使其转换为NH
,使其转换为NH ,同时生成有磁性的D的氧化物X,再进行后续处理。
,同时生成有磁性的D的氧化物X,再进行后续处理。①上述反应的离子方程式为
②B的单质与X在高温下反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相对位置如图,A元素最外层与次外层的电子数之差为3,B为地壳中含量最多的金属元素。

(1)D原子结构示意图为_______ 。
(2)将C的低价态氧化物甲中通入到D单质的水溶液会使之褪色,体现了甲的_______ 性,写出该反应的离子方程式_______ 。
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到100mL8.0mol/L乙的浓溶液中,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是_______ ,还原剂失电子数为_______ 。
(4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,充分反应生成气体的体积比为_______ ,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为_______ ;B单质表面的氧化膜可用NaOH溶液除去,写出该反应的化学方程式_______ 。

(1)D原子结构示意图为
(2)将C的低价态氧化物甲中通入到D单质的水溶液会使之褪色,体现了甲的
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到100mL8.0mol/L乙的浓溶液中,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是
(4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,充分反应生成气体的体积比为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】A、B、C、D、E五种主族元素分属三个短周期,且原子序数依次增大。B、D的原子序数之差为8,B原子最外层电子数是其次外层电子数的3倍,C原子在同周期主族元素中原子半径最大。
回答下列问题:
(1)B在周期表中的位置为__________ ;A、E形成的化合物中存在的化学键的类型是_______________ 。
(2)B、C、D原子的半径从大到小的顺序是________ (用元素符号表示);C单质与A的氧化物反应的化学方程式是__________________________ 。
(3)设计实验证明E的非金属性比D的非金属性强_______________________ (写出操作步骤及现象)。
回答下列问题:
(1)B在周期表中的位置为
(2)B、C、D原子的半径从大到小的顺序是
(3)设计实验证明E的非金属性比D的非金属性强
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】有A、B、C、D、E五种常见的短周期主族元素,它们的核电荷数依次增大,A元素原子的最外层只有一个电子;B和D元素原子的最外层电子数相同,且B元素原子L层电子数是K层电子数的3倍;C元素原子的最外层电子数是D元素原子最外层电子数的一半。
(1)D在元素周期表中的位置___ 。
(2)A与B形成原子个数比为1:1的液体物质甲,甲的电子式___ ;A与B形成原子个数比为2:1的液体物质乙,液态物质乙中存在的作用力有___ (填序号):
①共价键 ②离子键 ③氢键 ④范德华力
(3)B、C、D、E离子半径由大到小的顺序是___ (用离子符号表示)。
(4)化合物丙由E和F两种元素组成,常大量用于面粉的消毒与漂白,常温下呈液态,极易分解得两种气体单质X和Y。现有12.05g化合物丙,将完全分解后所得混合气体通过足量NaOH溶液,最后只余标准状况下1.12L气体单质X共1.40g。
请回答:
①丙的化学式是___ 。
②丙遇水蒸气可形成一种常见的漂白性物质M同时放出气体N,该反应为非氧化还原反应,写出丙与水反应的化学方程式为___ 。
(1)D在元素周期表中的位置
(2)A与B形成原子个数比为1:1的液体物质甲,甲的电子式
①共价键 ②离子键 ③氢键 ④范德华力
(3)B、C、D、E离子半径由大到小的顺序是
(4)化合物丙由E和F两种元素组成,常大量用于面粉的消毒与漂白,常温下呈液态,极易分解得两种气体单质X和Y。现有12.05g化合物丙,将完全分解后所得混合气体通过足量NaOH溶液,最后只余标准状况下1.12L气体单质X共1.40g。
请回答:
①丙的化学式是
②丙遇水蒸气可形成一种常见的漂白性物质M同时放出气体N,该反应为非氧化还原反应,写出丙与水反应的化学方程式为
您最近一年使用:0次



