A、B、C、D、E、F是元素周期表前四周期中原子序数依次增大的六种常见元素,其相关信息如下表:
回答下列问题:
(1)元素E在元素周期表中的位于第四周期第__ 族,其高价态离子核外有__ 个未成对电子。
(2)B、C、D三种元素的离子半径由小到大的顺序是______ (用离子符号表示)。
(3)A、D两元素的简单氢化物发生反应生成的化合物的电子式为_______ 。
(4)常温下AD3是一种淡黄色液体。以下关于AD3的说法中,正确的是___________
A.AD3分子中只有非极性键 B.AD3分子中各原子均达8e-稳定结构
C.AD3的晶体属于分子晶体 D.AD3液体气化时化学键被破坏
(5)金属C与E的黑色磁性晶体氧化物在高温下反应,该反应的化学方程式为____________________
(6)向F的硫酸盐溶液中通入AH3气体至过量,观察到的现象是__________ ;该过程总的离子反应式为________________ 向反应后的溶液中加入适量乙醇,析出深蓝色晶体,该晶体中不含有的化学键类型是________ 。
A.配位键 B.极性共价键 C.非极性共价键 D.离子键
元素 | 相 关 信 息 |
A | 原子核外有7种运动状态不同的电子 |
B | 外围电子排布式为nsnnpn+2 |
C | 常见的金属,在周期表中周期序数与族序数相等 |
D | 气态氢化物及最高价氧化物对应的水化物均为强酸 |
E | 一种核素的质量数为56,中子数为30 |
F | 单质紫红色,电缆材料,常见氧化物为黑色 |
(1)元素E在元素周期表中的位于第四周期第
(2)B、C、D三种元素的离子半径由小到大的顺序是
(3)A、D两元素的简单氢化物发生反应生成的化合物的电子式为
(4)常温下AD3是一种淡黄色液体。以下关于AD3的说法中,正确的是
A.AD3分子中只有非极性键 B.AD3分子中各原子均达8e-稳定结构
C.AD3的晶体属于分子晶体 D.AD3液体气化时化学键被破坏
(5)金属C与E的黑色磁性晶体氧化物在高温下反应,该反应的化学方程式为
(6)向F的硫酸盐溶液中通入AH3气体至过量,观察到的现象是
A.配位键 B.极性共价键 C.非极性共价键 D.离子键
更新时间:2017-03-22 12:37:51
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】X、Y、Z、M、W是原子序数由小到大排列的五种短周期主族元素,其中X、Z、M、W四种元素的原子序数之和为32,在元素周期表中X是原子半径最小的元素,Y原子的最外层电子数是其电子层数的2倍,Z、M左右相邻,M、W位于同主族。回答下列问题:
(1)Y在周期表中的位置是________ , W的阴离子符号是_____ 。
(2) Z的单质的结构式为________ 。标准状况下,试管中收集满Z的简单氢化物后倒立于水中(假设溶质不向试管外扩散),一段时间后,试管内溶液中溶质的物质的量浓度为_______ 。
(3)由X、Z、M三种元素组成的化合物是酸、碱、盐的化学式分别为________ (各举一例)。
(4)写出加热时Y的单质与W的最高价氧化物的水化物的浓溶液发生反应的化学方程式:_______ 。
(5)化合物甲由X、Z、M、W和Fe五种元素组成,甲的摩尔质量为392g·mol-1, 1 mol甲中含有6 mol结晶水。对化合物甲进行如下实验:
a.取甲的水溶液少许,加入过量的浓NaOH溶液,加热,产生白色絮状沉淀和无色、有刺激性气味的气体;白色絮状沉淀迅速变成灰绿色,最后变成红褐色。
b.另取甲的水溶液少许,加入过量的BaCl2溶液,产生白色沉淀;再加盐酸,白色沉淀不溶解。
① 甲的化学式为________ 。
② 已知100 mL 1 mol·L-1的甲溶液能与20 mL 1 mol·L-1的酸性KMnO4溶液恰好反应,写出反应的离子方程式:____________ 。
(1)Y在周期表中的位置是
(2) Z的单质的结构式为
(3)由X、Z、M三种元素组成的化合物是酸、碱、盐的化学式分别为
(4)写出加热时Y的单质与W的最高价氧化物的水化物的浓溶液发生反应的化学方程式:
(5)化合物甲由X、Z、M、W和Fe五种元素组成,甲的摩尔质量为392g·mol-1, 1 mol甲中含有6 mol结晶水。对化合物甲进行如下实验:
a.取甲的水溶液少许,加入过量的浓NaOH溶液,加热,产生白色絮状沉淀和无色、有刺激性气味的气体;白色絮状沉淀迅速变成灰绿色,最后变成红褐色。
b.另取甲的水溶液少许,加入过量的BaCl2溶液,产生白色沉淀;再加盐酸,白色沉淀不溶解。
① 甲的化学式为
② 已知100 mL 1 mol·L-1的甲溶液能与20 mL 1 mol·L-1的酸性KMnO4溶液恰好反应,写出反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】A~E是周期表中1~36号的元素,它们的原子序数递增,对它们的性质及结构的描述如下:A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之邻的所有元素;D在周期表中位于C的下一周期,其电负性在同周期主族元素中最大;E的基态原子在前四周期中未成对电子数最多。
(1)基态B原子的价电子中,两种自旋状态的电子数之比为___________ 。 中C原子的杂化方式为
中C原子的杂化方式为___________ 。
(2)已知元素的电负性:C>D,则C与D形成的化合物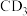 的空间构型为
的空间构型为___________ ,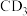 与水发生水解反应的化学方程式为
与水发生水解反应的化学方程式为___________ 。
(3)E位于元素周期表的___________ 区。
(4)已知常温下 的水解常数
的水解常数 。
。
常温下,含等物质的量浓度的HBC与NaBC的混合溶液显___________ (填“酸”“碱”或“中”)性,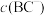
___________ (填“>”“<”或“=”)c(HBC)。常温下,若将 盐酸与
盐酸与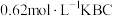 溶液等体积混合后恰好得到中性溶液,则c=
溶液等体积混合后恰好得到中性溶液,则c=___________ (小数点后保留4位数字)。
(1)基态B原子的价电子中,两种自旋状态的电子数之比为
 中C原子的杂化方式为
中C原子的杂化方式为(2)已知元素的电负性:C>D,则C与D形成的化合物
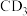 的空间构型为
的空间构型为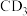 与水发生水解反应的化学方程式为
与水发生水解反应的化学方程式为(3)E位于元素周期表的
(4)已知常温下
 的水解常数
的水解常数 。
。常温下,含等物质的量浓度的HBC与NaBC的混合溶液显
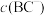
 盐酸与
盐酸与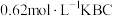 溶液等体积混合后恰好得到中性溶液,则c=
溶液等体积混合后恰好得到中性溶液,则c=
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】前四周期的A、B、C、D、E、F六种元素,原子序数依次增大。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上未成对的电子数最多;C元素为最活泼的非金属元素;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
(1)E元素在周期表中位置为_______ ,E3+价电子轨道表示式为_______ 。
(2)B、C、F三种元素电负性由大到小的顺序为_______ (用元素符号表示),第一电离能D_______ (填“>”、“<”或“=”)Al,其原因是_______ 。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)F元素可能的性质_______ (填标号)。
 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。(1)E元素在周期表中位置为
(2)B、C、F三种元素电负性由大到小的顺序为
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)F元素可能的性质
| A.其单质可作半导体材料 |
| B.存在-3、+3、+5等多种化合价 |
| C.最高价氧化物对应的水化物是强酸 |
| D.单质还原性弱于磷单质 |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】硼族元素可形成许多结构和性质特殊的化合物。回答下列问题
(1)基态Ga原子的电子排布式为___________ 。
(2)常温下,F2与硼单质反应生成BF3,BF3为缺电子结构,通入水中产生三种酸分别为HBF4、HF和___________ (填化学式)。NF3和NF3BF3中F-N-F的键角大小是NF3___________ NF3BF3(填“>”、“<”或“=”)。
(3)一定条件下,NH4F、NaF和NaAlO2反应生成NH3、H2O和化合物X。X晶胞及晶胞中某一原子的俯视投影如图所示。___________ 。
②X晶体内含有的作用力有___________ (填字母)。
a.配位键 b.离子键 c.氢键 d.金属键
(4)解释H2N-NH2,HO-OH,H3C-CH3中,N-N,O-O,C-C的键能O-O<N-N<C-C___________ 。
(1)基态Ga原子的电子排布式为
(2)常温下,F2与硼单质反应生成BF3,BF3为缺电子结构,通入水中产生三种酸分别为HBF4、HF和
(3)一定条件下,NH4F、NaF和NaAlO2反应生成NH3、H2O和化合物X。X晶胞及晶胞中某一原子的俯视投影如图所示。
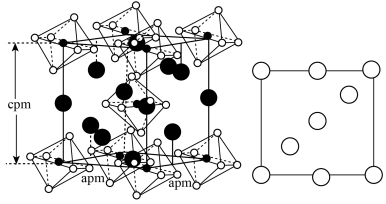
②X晶体内含有的作用力有
a.配位键 b.离子键 c.氢键 d.金属键
(4)解释H2N-NH2,HO-OH,H3C-CH3中,N-N,O-O,C-C的键能O-O<N-N<C-C
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】甲基叔戊基醚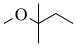 (TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇
(TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇 (简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应(
(简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应( 为2-甲基-1-丁烯的简写,不考虑其他副反应):
为2-甲基-1-丁烯的简写,不考虑其他副反应):
反应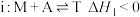
反应ii: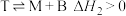
反应iii:
(1)磷钼酸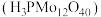 可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第VIB族,核外电子排布与
可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第VIB族,核外电子排布与 相似。
相似。
①基态钼原子的价层电子排布式为_______ 。
②完成化学方程式: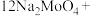
_______ 
(2)比较
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)我国学者团队对制备TAME反应的催化剂进行了研究。研究衣明:用不同浓度(13%)的磷钼酸浸渍催化剂,浓度越大催化剂催化活性越好。用浓度分别为 的磷钼酸浸渍催化剂进行了三组实验,得到
的磷钼酸浸渍催化剂进行了三组实验,得到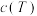 随时间
随时间 的变化曲线如图所示。
的变化曲线如图所示。
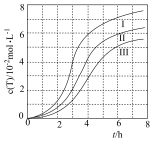
①用 的磷钼酸浸渍时,在
的磷钼酸浸渍时,在 内,
内, 的平均生成速率为
的平均生成速率为_______ 。
②下列仿关说法正确的有_______ 。
A.三组实验中,反应速率都随反应进程一直增大
B.平衡后加入惰性溶剂四氢呋喃稀释, 减小
减小
C.催化剂可加快化学反应速率,提高甲醇的平衡转化率
D.降低温度,反应 和ii的正、逆反应速率都减小
和ii的正、逆反应速率都减小
E.达到平衡后,加入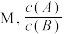 不变
不变
(4)研究团队继续研究其他条件不变时,不同醇烯比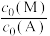 (甲醇
(甲醇 与烯烃
与烯烃 的起始物质的量浓度之比)对平衡的影响,当
的起始物质的量浓度之比)对平衡的影响,当 起始浓度
起始浓度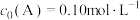 时,测得平衡时
时,测得平衡时 和
和 的
的 随
随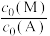 的变化曲线如图。
的变化曲线如图。
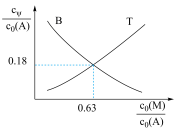
①曲线 呈现如图所示变化的原因是
呈现如图所示变化的原因是_______ 。
②当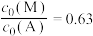 时,计算反应I的平衡常数
时,计算反应I的平衡常数_______ (写出计算过程)。
 (TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇
(TAME,简写为T)常用作汽油添加剂。在催化剂作用下,通过甲醇 (简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应(
(简写为M)与2-甲基-2-丁烯(简写为A)的液相反应制得。通过控制条件,体系中主要发生如下反应( 为2-甲基-1-丁烯的简写,不考虑其他副反应):
为2-甲基-1-丁烯的简写,不考虑其他副反应):反应
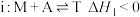
反应ii:
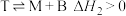
反应iii:

(1)磷钼酸
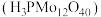 可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第VIB族,核外电子排布与
可作为制备TAME反应催化剂的浸渍试剂。已知钼元素位于第五周期第VIB族,核外电子排布与 相似。
相似。①基态钼原子的价层电子排布式为
②完成化学方程式:
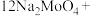

(2)比较

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)我国学者团队对制备TAME反应的催化剂进行了研究。研究衣明:用不同浓度(13%)的磷钼酸浸渍催化剂,浓度越大催化剂催化活性越好。用浓度分别为
 的磷钼酸浸渍催化剂进行了三组实验,得到
的磷钼酸浸渍催化剂进行了三组实验,得到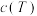 随时间
随时间 的变化曲线如图所示。
的变化曲线如图所示。
①用
 的磷钼酸浸渍时,在
的磷钼酸浸渍时,在 内,
内, 的平均生成速率为
的平均生成速率为②下列仿关说法正确的有
A.三组实验中,反应速率都随反应进程一直增大
B.平衡后加入惰性溶剂四氢呋喃稀释,
 减小
减小C.催化剂可加快化学反应速率,提高甲醇的平衡转化率
D.降低温度,反应
 和ii的正、逆反应速率都减小
和ii的正、逆反应速率都减小E.达到平衡后,加入
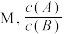 不变
不变(4)研究团队继续研究其他条件不变时,不同醇烯比
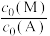 (甲醇
(甲醇 与烯烃
与烯烃 的起始物质的量浓度之比)对平衡的影响,当
的起始物质的量浓度之比)对平衡的影响,当 起始浓度
起始浓度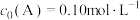 时,测得平衡时
时,测得平衡时 和
和 的
的 随
随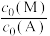 的变化曲线如图。
的变化曲线如图。
①曲线
 呈现如图所示变化的原因是
呈现如图所示变化的原因是②当
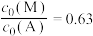 时,计算反应I的平衡常数
时,计算反应I的平衡常数
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】自然界中存在大量的金属元素,在工农业生产中有着广泛的应用。回答下列问题:
(1)焰色反应的光谱属于发射光谱,铜和含铜离子化合物的焰色为___________ 色。
(2)基态Ni原子中,核外电子占据的最高能层符号是___________ ,其核外电子排布式中未成对电子数为___________ 个。
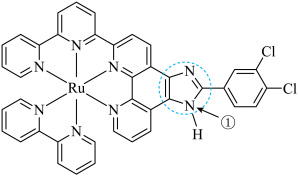
(3)钌-多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(Ⅱ)的配位数是___________ ,已知虚线框内五个原子共平面,则①号N原子的杂化类型为___________ 。
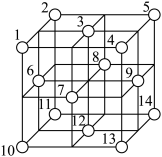
(4)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着如由1、3、6、7的O2-围成的正四面体空隙和3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和全部Fe2+填充在正八面体空隙中,则Fe3O4晶体中,正八面体空隙数与O2-数之比为___________ 。正四面体空隙填充率与正八面体空隙填充率之比为___________ 。Fe3O4晶胞中有8个图示结构单元,该晶胞参数为apm,则晶体密度为___________ g/cm3(写出含a和NA的计算表达式)。
(1)焰色反应的光谱属于发射光谱,铜和含铜离子化合物的焰色为
(2)基态Ni原子中,核外电子占据的最高能层符号是
(3)钌-多吡啶配合物具有丰富的光化学和光物理信息,结构简式如图所示。钌(Ⅱ)的配位数是

(4)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着如由1、3、6、7的O2-围成的正四面体空隙和3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和全部Fe2+填充在正八面体空隙中,则Fe3O4晶体中,正八面体空隙数与O2-数之比为

您最近一年使用:0次



