有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E的顺序增大。C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2反应生成C2A与气态物质EB4;E的M层电子数是K层电子数的2倍。
(1)写出下列元素的名称:B:________ E:________ 。
(2)写出EB4的化学式:__________ 。
(3)D2A2中含有的化学键类型为____________ 。
(4)由A、C、D三种元素组成的化合物M属于________ (填“离子”或“共价”)化合物,M溶于水后________ (填“能”或“不能”)发生化学变化,原因是(从化学键变化的角度解释):___________________________________ 。
(1)写出下列元素的名称:B:
(2)写出EB4的化学式:
(3)D2A2中含有的化学键类型为
(4)由A、C、D三种元素组成的化合物M属于
更新时间:2017-05-05 13:45:07
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知X、Y、Z、W四种元素分别是元素周期表中三个连续短周期的元素,且原子序数依次增大。X、W同主族, Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键。 原子的最外层电子数是次外层电子数的3倍,试推断:
原子的最外层电子数是次外层电子数的3倍,试推断:
(1)X、Z两种元素的元素符号: X__________ 、Z__________ 。
(2)由以上元素中两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为__________ ,它的共价键属于__________ (填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为__________ ;含有极性共价键和非极性共价键的化合物的电子式为_______ 。
(3)由X、Y、Z所形成的常见离子化合物是__________ (写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为__________ ;W的单质与水反应时,水作__________ (填“氧化剂”或“还原剂”)。
(4)用电子式表示W与Z形成W2Z化合物的过程:__________ 。
 原子的最外层电子数是次外层电子数的3倍,试推断:
原子的最外层电子数是次外层电子数的3倍,试推断:(1)X、Z两种元素的元素符号: X
(2)由以上元素中两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为
(3)由X、Y、Z所形成的常见离子化合物是
(4)用电子式表示W与Z形成W2Z化合物的过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下列是元素周期表的一部分,表中所列字母分别代表某一化学元素。
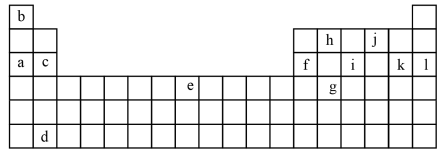
(1)e元素在周期表中的位置是___ ;表中所列元素的单质能用作半导体材料的是___ (填名称)。
(2)写出h与b元素组成的最简单分子的电子式:___ ;i、k元素的最高价氧化物对应水化物的酸性强弱为:____>___(用化学式表示)___ 。
(3)将表中短周期字母元素挑出四种,另用W、X、Y、Z表示,其原子序数X>W>Z>Y,X原子最外层电子数与最内层电子数相等,Y原子最外层电子数是内层电子数的2倍,W原子和Z原子可形成2∶1和1∶1两种化合物,Z原子最外层电子数是核外电子层数的3倍。
①写出Y、Z的元素符号:Y___ ,Z___ 。
②W、X元素的最高价氧化物对应水化物的碱性强弱为:____<____(用化学式表示)___ 。
③这四种元素原子半径的大小为___>____>____>____(填元素符号)___ 。

(1)e元素在周期表中的位置是
(2)写出h与b元素组成的最简单分子的电子式:
(3)将表中短周期字母元素挑出四种,另用W、X、Y、Z表示,其原子序数X>W>Z>Y,X原子最外层电子数与最内层电子数相等,Y原子最外层电子数是内层电子数的2倍,W原子和Z原子可形成2∶1和1∶1两种化合物,Z原子最外层电子数是核外电子层数的3倍。
①写出Y、Z的元素符号:Y
②W、X元素的最高价氧化物对应水化物的碱性强弱为:____<____(用化学式表示)
③这四种元素原子半径的大小为___>____>____>____(填元素符号)
您最近一年使用:0次
【推荐3】W、X、Y、Z四种短周期元素的原子序数W>X>Z>Y。X原子的最外层没有p电子,Y原子最外层s电子与p电子数之比为1∶1,W与Z原子核外s电子与p电子数之比均为1∶1。则:
(1)写出各元素的元素符号:W:________ 、X:________ 、Y:________ 、Z:________ 。
(2)四种元素原子半径大小顺序依次为____________________________________ 。
(3)W、X元素最高价氧化物对应水化物的碱性强弱为________________________ (用化学式表示)。
(1)写出各元素的元素符号:W:
(2)四种元素原子半径大小顺序依次为
(3)W、X元素最高价氧化物对应水化物的碱性强弱为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、F、G均为短周期主族元素,其原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成化合物X,X的水溶液呈碱性;A、D同主族,C的原子序数等于A、B原子序数之和;E是地壳中含量最高的金属元素,F元素的原子最外层比次外层少两个电子。回答下列问题:
(1)F和G的最高价氧化物对应的水化物的酸性较强的是______ (写最高价氧化物对应的水化物的化学式)。
(2)A和C按照原子个数1:1形成的化合物的结构式为______ 。
(3)都由A、C、D、F四种元素形成的两种化合物的水溶液反应的离子方程式为____________________
(4)常温下,液态化合物B2A4与气态化合物BC2反应生成无毒物质,写出其反应的化学方程式为___________________________
(5)FC2通入BaCl2溶液中无明显现象,但与G的单质一起通入则有白色沉淀出现,请用离子方程式表示沉淀形成的过程____________________________________________ 。
(1)F和G的最高价氧化物对应的水化物的酸性较强的是
(2)A和C按照原子个数1:1形成的化合物的结构式为
(3)都由A、C、D、F四种元素形成的两种化合物的水溶液反应的离子方程式为
(4)常温下,液态化合物B2A4与气态化合物BC2反应生成无毒物质,写出其反应的化学方程式为
(5)FC2通入BaCl2溶液中无明显现象,但与G的单质一起通入则有白色沉淀出现,请用离子方程式表示沉淀形成的过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】以下是元素周期表的一部分,回答下列有关问题:
⑴写出⑥的元素符号:___ ,⑧的离子结构示意图____ ,②的单质的电子式_____ ,①的氢化物结构式___ 。
⑵在这些元素中,最不活泼的元素是____________ (用元素符号作答)。
⑶在这些元素的最高价氧化物对应的水化物中,酸性最强的是_________ ;(用化学式作答,下同)碱性最强的是_________ ;呈两性的氢氧化物的是_________ 。
⑷在这些元素中,原子半径最大的是________ (用元素符号作答)。
⑸这些元素中形成的碱性最强的碱与呈两性的氢氧化物恰好反应的离子方程式是
_________________________________________________________________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑾ | ⑿ |
⑴写出⑥的元素符号:
⑵在这些元素中,最不活泼的元素是
⑶在这些元素的最高价氧化物对应的水化物中,酸性最强的是
⑷在这些元素中,原子半径最大的是
⑸这些元素中形成的碱性最强的碱与呈两性的氢氧化物恰好反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、D、E、G 是原子序数依次增大的五种短周期元素,A与E同主族,A、B和E的原子最外层电子数之和为19,B与G 的单质都能与 H2反应生成“HX”(X代表B或G)型氢化物,D 为同周期主族元素中原子半径最大的元素。
(1)B 在元素周期表中的位置是______ 。
(2)D 的两种常见氧化物中均含有____________ (填“离子键”或“共价键”)。
(3)E的最高价氧化物对应水化物的浓溶液和木炭共热,反应的化学方程式为____________ 。
(4)D 的最高价氧化物对应水化物的溶液与G的单质反应,反应的离子方程式为___________ 。
(5)用原子结构解释“B、G 单质都能与H2反应生成HX型氢化物”的原因:________ 。
(1)B 在元素周期表中的位置是
(2)D 的两种常见氧化物中均含有
(3)E的最高价氧化物对应水化物的浓溶液和木炭共热,反应的化学方程式为
(4)D 的最高价氧化物对应水化物的溶液与G的单质反应,反应的离子方程式为
(5)用原子结构解释“B、G 单质都能与H2反应生成HX型氢化物”的原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表是元素周期表的前三周期及其中的部分元素,请回答相关问题
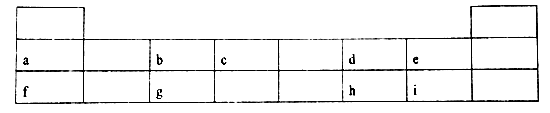
(1) a、f、g 元素最高价氧化物的水化物碱性由强到弱的顺序是__________ (用化学式表示)。表中所给元素中金属性最强的与非金属性最强的形成的化合物溶液显______ (填“中性“酸性”或“碱性” )。
(2) 氢元素可与其它元素形成_________ (填选项序号)等化学键。
A.极性共价键 B.非极性共价键 C.氢键 D.离子键
(3)d、f、h三种元素可形成一种有强还原性的化合物,该化合物中含有非极性键,其化学式为____ ,向该化合物的水溶液中加入盐酸发生反应的离子方程式为______________ 。
(4)表中所给的某两种元素可形成一种常见的有机溶剂,可用于萃取碘水中的碘单质,萃取后有机层的颜色为___________ ,分液时有机层应从________ (填“下口流出“或“上口倒出”)。该有机溶剂的电子式是_______ 。

(1) a、f、g 元素最高价氧化物的水化物碱性由强到弱的顺序是
(2) 氢元素可与其它元素形成
A.极性共价键 B.非极性共价键 C.氢键 D.离子键
(3)d、f、h三种元素可形成一种有强还原性的化合物,该化合物中含有非极性键,其化学式为
(4)表中所给的某两种元素可形成一种常见的有机溶剂,可用于萃取碘水中的碘单质,萃取后有机层的颜色为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
真题
解题方法
【推荐2】A是自然界存在最广泛的ⅡA族元素,常以化合物F存在。从单质A起始发生的一系列化学反应可由下图表示:
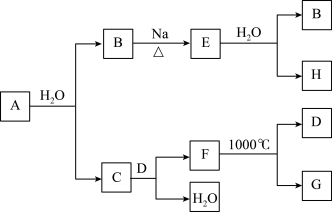
请回答下列问题:
(1) A与水反应的化学方程式为_______________ ,E与水反应的化学方程式为_____________ ;
(2)F的化学式为_____________ ,G和D的电子式分别为_______________ 和______________ ;
(3)D与H反应可能生成的盐有_____________ (填化学式);
(4)实际生产中,可由F为原料制备单质A,简述一种制备方法_________________ 。

请回答下列问题:
(1) A与水反应的化学方程式为
(2)F的化学式为
(3)D与H反应可能生成的盐有
(4)实际生产中,可由F为原料制备单质A,简述一种制备方法
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。①A元素最外层电子数是次外层电子数的2倍。②B的阴离子和C的阳离子与氖原子的电子层结构相同。③在通常状况下,B的单质是气体,0.1molB的气体与足量的氢气完全反应共有0.4mol电子转移。④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应可生成B的单质。⑤D与B同主族。请回答下列问题:
(1)写出各元素的元素符号A:___ ;B:___ ;C:___ ;D:___ 。
(2)B元素在周期表中的位置为___ 。
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有___ ,___ 。
(4)④中淡黄色固体能与AB2反应可生成B的单质的化学反应方程式为___ 。
(5)C与D能形成2:1的化合物,用电子式表示该化合物的形成过程___ 。
(6)元素D与元素E相比,能证明这两种元素非金属性谁更强的事实是___ (填字母)。
a.常温下D的单质和E的单质状态不同
b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
(1)写出各元素的元素符号A:
(2)B元素在周期表中的位置为
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有
(4)④中淡黄色固体能与AB2反应可生成B的单质的化学反应方程式为
(5)C与D能形成2:1的化合物,用电子式表示该化合物的形成过程
(6)元素D与元素E相比,能证明这两种元素非金属性谁更强的事实是
a.常温下D的单质和E的单质状态不同
b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1)CaC2中 与
与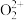 互为等电子体,
互为等电子体,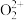 的电子式可表示为
的电子式可表示为___________ ;1 mol 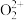 中含有的π键数目为
中含有的π键数目为___________ 。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为___________ 。
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是___________ ;分子中处于同一直线上的原子数目最多为___________ 。
(1)CaC2中
 与
与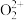 互为等电子体,
互为等电子体,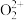 的电子式可表示为
的电子式可表示为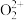 中含有的π键数目为
中含有的π键数目为(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】观察下面的元素周期表,并回答下列问题
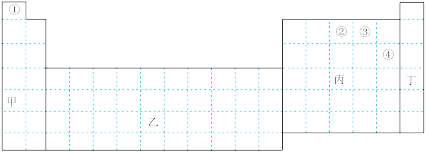
(1)在上面元素周期表中,全部是金属元素的区域为_______
甲 乙 丙 丁
(2)用实线画出金属与非金属的分界线。(在答题卷图上完成)_______ 。
(3)请问:仅用①②④三种元素_______ (填“能”或“不能”)形成离子化合物;若能,请写出该物质的名称_______ (若不能,此格不填)若用球棍模型表示①和③形成的化合物的分子结构,应该是_______ 。


(1)在上面元素周期表中,全部是金属元素的区域为
甲 乙 丙 丁
(2)用实线画出金属与非金属的分界线。(在答题卷图上完成)
(3)请问:仅用①②④三种元素

您最近一年使用:0次



