FeCl3的用途广泛。
(1)实验室利用FeCl3制备Fe(OH)3胶体:
①Fe(OH)3胶体制备反应的化学方程式为___________________________________________ 。
②利用所制得的Fe(OH)3胶体进行实验:将其装入U形管内,用石墨作电极,通电一段时间后发现
___________ 极区附近的红褐色逐渐变深,这表明_________________________________
③向Fe(OH)3胶体中加H2SO4溶液,产生的现象是_______________________________ 。
(2)FeCl3溶液常用于腐蚀铜印刷电路板,该反应的离子方程式为_________________________ 。
(3)FeCl3常用于净水,用离子方程式表示其原理____________________________________ 。
(4)FeCl3溶液中若混有FeCl2,检验FeCl2的试剂为________________________ 。
(5)将FeCl3溶液蒸干并灼烧得到的固体成分为__________________ 。
(6)已知Fe(OH)3的Ksp=8×10-38,某溶液中c(FeCl3)=0.05mol/L,如果要使Fe(OH)3沉淀完全,pH至少为______________________ 。
(溶液中离子浓度小于10-5mol/L认为沉淀已完全,已知lg2=0.3 lg5=0.7)
(1)实验室利用FeCl3制备Fe(OH)3胶体:
①Fe(OH)3胶体制备反应的化学方程式为
②利用所制得的Fe(OH)3胶体进行实验:将其装入U形管内,用石墨作电极,通电一段时间后发现
③向Fe(OH)3胶体中加H2SO4溶液,产生的现象是
(2)FeCl3溶液常用于腐蚀铜印刷电路板,该反应的离子方程式为
(3)FeCl3常用于净水,用离子方程式表示其原理
(4)FeCl3溶液中若混有FeCl2,检验FeCl2的试剂为
(5)将FeCl3溶液蒸干并灼烧得到的固体成分为
(6)已知Fe(OH)3的Ksp=8×10-38,某溶液中c(FeCl3)=0.05mol/L,如果要使Fe(OH)3沉淀完全,pH至少为
(溶液中离子浓度小于10-5mol/L认为沉淀已完全,已知lg2=0.3 lg5=0.7)
更新时间:2017-05-08 20:43:02
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】I.学习化学离不开化学实验,请结合下图回答问题。
资料:碳酸钠与二氧化碳、水反应生成可溶于水的碳酸氢钠。
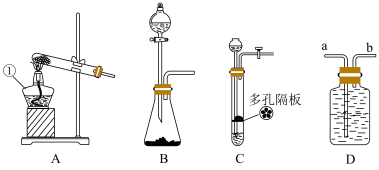
(1)写出图B中装固体和液体仪器的名称分别为______ 、______ 。
(2)若用D装置收集氧气,则气体应该从_____ (填“a”或“b”)进入。
(3)实验室用锌粒与稀硫酸制取H2,其反应的离子方程式为___________ 。装置C与B相比较,其优点是________ 。
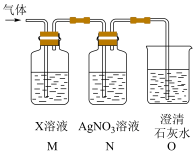
(4)实验室用石灰石与盐酸制取的CO2通入到澄清石灰水,石灰水并未变浑浊。将气体依次通过装置M、N、O后,发现N中溶液不变浑浊,O中溶液变浑浊。则装置M中X溶液为_____ (填字母)。
A.饱和Na2CO3溶液 B.饱和NaHCO3溶液 C.饱和NaOH溶液
II.通过分散系的学习,我们认识了胶体,下面就胶体的制备以及相关性质做了相应探究。根据所学回答下列问题:
(5)取少量 粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为
粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为_________ ,反应后得到的溶液记为A。
(6)在小烧杯中加入 蒸馏水,加热至沸腾后,向沸水中滴入饱和A,继续煮沸至溶液呈红褐色,停止加热,即制得
蒸馏水,加热至沸腾后,向沸水中滴入饱和A,继续煮沸至溶液呈红褐色,停止加热,即制得 胶体(记为C)。制备C的化学反应方程式为:
胶体(记为C)。制备C的化学反应方程式为:_________ 。
(7)另取一只小烧杯也加入 蒸馏水,接着向烧杯中加入少量
蒸馏水,接着向烧杯中加入少量 溶液,振荡均匀后的液体记为D,将C与D一起放置于暗处,分别用激光笔照射,可以看到
溶液,振荡均匀后的液体记为D,将C与D一起放置于暗处,分别用激光笔照射,可以看到_________ 。(填现象)。
资料:碳酸钠与二氧化碳、水反应生成可溶于水的碳酸氢钠。

(1)写出图B中装固体和液体仪器的名称分别为
(2)若用D装置收集氧气,则气体应该从
(3)实验室用锌粒与稀硫酸制取H2,其反应的离子方程式为
(4)实验室用石灰石与盐酸制取的CO2通入到澄清石灰水,石灰水并未变浑浊。将气体依次通过装置M、N、O后,发现N中溶液不变浑浊,O中溶液变浑浊。则装置M中X溶液为

A.饱和Na2CO3溶液 B.饱和NaHCO3溶液 C.饱和NaOH溶液
II.通过分散系的学习,我们认识了胶体,下面就胶体的制备以及相关性质做了相应探究。根据所学回答下列问题:
(5)取少量
 粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为
粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为(6)在小烧杯中加入
 蒸馏水,加热至沸腾后,向沸水中滴入饱和A,继续煮沸至溶液呈红褐色,停止加热,即制得
蒸馏水,加热至沸腾后,向沸水中滴入饱和A,继续煮沸至溶液呈红褐色,停止加热,即制得 胶体(记为C)。制备C的化学反应方程式为:
胶体(记为C)。制备C的化学反应方程式为:(7)另取一只小烧杯也加入
 蒸馏水,接着向烧杯中加入少量
蒸馏水,接着向烧杯中加入少量 溶液,振荡均匀后的液体记为D,将C与D一起放置于暗处,分别用激光笔照射,可以看到
溶液,振荡均匀后的液体记为D,将C与D一起放置于暗处,分别用激光笔照射,可以看到
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验兴趣小组同学用如图所示装置制备氢氧化铁胶体(部分夹持装置已略去)。根据所学知识回答下列问题:
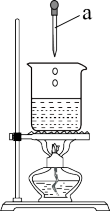
已知:淀粉溶液遇到碘水会变蓝。
(1)仪器a的名称为_______ 。
(2)氢氧化铁胶体的制备:
①制备方法为_______ 。
②烧杯中发生反应的化学方程式为 ,该反应的反应类型为
,该反应的反应类型为_______ (填基本反应类型)。
③下列关于氢氧化铁胶体的说法正确的是_______ (填标号)。
A.具有吸附性
B.单个氢氧化铁分子的直径大于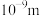
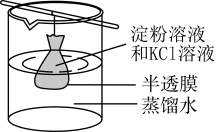
(3)通常采用透析法(使离子或分子从胶体里分离出去的操作)净化胶体。将淀粉溶液和KCl溶液的混合液加入由半透膜(胶体不能透过半透膜)制成的袋中,并将此袋浸入装有蒸馏水的烧杯中。几分钟后,烧杯中的液体_______ (填“有”或“无”)淀粉溶液。取烧杯中的少许液体加入试管中,向试管中滴加少量 溶液,试管中出现
溶液,试管中出现_______ (填颜色)沉淀,且该沉淀为_______ (填化学式)。

已知:淀粉溶液遇到碘水会变蓝。
(1)仪器a的名称为
(2)氢氧化铁胶体的制备:
①制备方法为
②烧杯中发生反应的化学方程式为
 ,该反应的反应类型为
,该反应的反应类型为③下列关于氢氧化铁胶体的说法正确的是
A.具有吸附性
B.单个氢氧化铁分子的直径大于
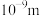
(3)通常采用透析法(使离子或分子从胶体里分离出去的操作)净化胶体。将淀粉溶液和KCl溶液的混合液加入由半透膜(胶体不能透过半透膜)制成的袋中,并将此袋浸入装有蒸馏水的烧杯中。几分钟后,烧杯中的液体
 溶液,试管中出现
溶液,试管中出现
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某课外兴趣小组的同学向Na2SiO3溶液中滴加盐酸,预计会生成H2SiO3胶体,用激光笔照射会出现“丁达尔效应”。但令人意想不到的是,试管中在出现硅酸胶体的同时也出现了大量气泡,为什么会出现这种现象呢?甲乙两同学进行了大胆的推测。
甲同学推测是生成了硅酸胶体,造成HCl在溶液中的溶解度变小,最终从溶液中逸出;
乙同学咨询了实验员得知这瓶Na2SiO3溶液已经放置了很长一段时间,他推测溶液可能已经变质,故导致以上现象的出现。
(1)请设计一个最简单的实验验证甲同学的推测是否正确:____________________ ;
(2)乙同学取这瓶久置的硅酸钠溶液,用激光笔照射,发现有光柱出现,说明在这瓶硅酸钠溶液中已经有______________ 胶体生成。推测产生的气体可能是__________ ,然后乙同学又做了两个实验进行验证:
Ⅰ.取少量该瓶溶液,向其中滴加__________ ,并检验产生的气体。请写出检验该气体的常用方法:__________________________ ;
Ⅱ.取硅酸钠固体,配成饱和溶液,现配现用,滴入盐酸,观察现象;
(3)通过以上实验,证明了乙同学观点正确,请写出所对应的化学反应方程式:_______________________ 、_______________________ 。
甲同学推测是生成了硅酸胶体,造成HCl在溶液中的溶解度变小,最终从溶液中逸出;
乙同学咨询了实验员得知这瓶Na2SiO3溶液已经放置了很长一段时间,他推测溶液可能已经变质,故导致以上现象的出现。
(1)请设计一个最简单的实验验证甲同学的推测是否正确:
(2)乙同学取这瓶久置的硅酸钠溶液,用激光笔照射,发现有光柱出现,说明在这瓶硅酸钠溶液中已经有
Ⅰ.取少量该瓶溶液,向其中滴加
Ⅱ.取硅酸钠固体,配成饱和溶液,现配现用,滴入盐酸,观察现象;
(3)通过以上实验,证明了乙同学观点正确,请写出所对应的化学反应方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学:向饱和FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
回答下列问题:
(1)其中操作正确的同学是_______ (填“甲”“乙”或“丙”),该正确操作的化学方程式为_______ 。
(2)证明有Fe(OH)3胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是_______ 。
(3)丙同学在做实验时加热时间过长,结果形成了悬浊液,原因是_______ 。
(4)丁同学取适量的Fe(OH)3胶体注入试管,然后用胶头滴管逐滴向试管中加入过量稀硫酸,观察到现象为_______ 。
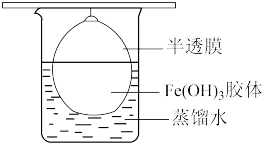
(5)戊同学认为制备的Fe(OH)3胶体中混有FeCl3杂质,采用如图所示装置进行提纯,该操作名称为_______ ,放置2 min后,取少量半透膜外的液体于试管中,向试管中加入用稀硝酸酸化的AgNO3溶液,可观察到的现象为_______ 。
甲同学:向饱和FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
回答下列问题:
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是
(3)丙同学在做实验时加热时间过长,结果形成了悬浊液,原因是
(4)丁同学取适量的Fe(OH)3胶体注入试管,然后用胶头滴管逐滴向试管中加入过量稀硫酸,观察到现象为
(5)戊同学认为制备的Fe(OH)3胶体中混有FeCl3杂质,采用如图所示装置进行提纯,该操作名称为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】我国规定饮用水质量标准如表所示:
如图是源水处理成自来水的工艺流程示意图,请回答:
源水 曝气池
曝气池 一级沉降池
一级沉降池 二级沉降池
二级沉降池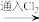 过滤池
过滤池 自来水
自来水
(1)源水中含 、
、 、
、 、
、 等,加入过量生石灰后生成
等,加入过量生石灰后生成 ,进而发生若干化学反应,在一级沉降池中所得沉淀的主要成分为
,进而发生若干化学反应,在一级沉降池中所得沉淀的主要成分为_______ (填化学式)。
(2) 是常用的絮凝剂,加入后最终生成红褐色
是常用的絮凝剂,加入后最终生成红褐色 胶状物,写出实验室制备
胶状物,写出实验室制备 胶体的化学方程式
胶体的化学方程式_______ 。
(3) 的作用是杀菌、消毒,写出氯气与水反应的离子方程式
的作用是杀菌、消毒,写出氯气与水反应的离子方程式_________ 。下列物质可替代 的是
的是_______ (填序号)。
①NaCl ② ③
③
(4)水中 和
和 的含量可用Y溶液进行测定,Y与
的含量可用Y溶液进行测定,Y与 和
和 均以等物质的量完全反应。现取某水厂样品100mL,测得完全反应时消耗
均以等物质的量完全反应。现取某水厂样品100mL,测得完全反应时消耗 溶液,则该水厂样品中
溶液,则该水厂样品中 、
、 总浓度是
总浓度是______ mol/L,说明已达到饮用水标准。
| 项目 | pH |  、 、 总浓度 总浓度 | 细菌个数 |
| 相关值 | 6.5~8.5 |  | 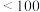 个 个 |
源水
 曝气池
曝气池 一级沉降池
一级沉降池 二级沉降池
二级沉降池 过滤池
过滤池 自来水
自来水(1)源水中含
 、
、 、
、 、
、 等,加入过量生石灰后生成
等,加入过量生石灰后生成 ,进而发生若干化学反应,在一级沉降池中所得沉淀的主要成分为
,进而发生若干化学反应,在一级沉降池中所得沉淀的主要成分为(2)
 是常用的絮凝剂,加入后最终生成红褐色
是常用的絮凝剂,加入后最终生成红褐色 胶状物,写出实验室制备
胶状物,写出实验室制备 胶体的化学方程式
胶体的化学方程式(3)
 的作用是杀菌、消毒,写出氯气与水反应的离子方程式
的作用是杀菌、消毒,写出氯气与水反应的离子方程式 的是
的是①NaCl ②
 ③
③
(4)水中
 和
和 的含量可用Y溶液进行测定,Y与
的含量可用Y溶液进行测定,Y与 和
和 均以等物质的量完全反应。现取某水厂样品100mL,测得完全反应时消耗
均以等物质的量完全反应。现取某水厂样品100mL,测得完全反应时消耗 溶液,则该水厂样品中
溶液,则该水厂样品中 、
、 总浓度是
总浓度是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氯化铁溶液和氢氧化铁胶体颜色相近,某同学按照以下操作步骤进行实验探究二者的性质。
(1)向少量红棕色的Fe2O3粉末,加入适量盐酸,发生反应的化学方程式为____ ,反应后得到的溶液呈____ 色。
(2)取少量上述溶液于试管中,滴入几滴NaOH溶液,可观察到____ 的现象,反应的化学方程式为____ 。
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈____ 色,即制得Fe(OH)3胶体。该实验不能用自来水的原因是____ 。
(4)取另一只盛有20mL蒸馏水的小烧杯,向其中加入1mLFeCl3溶液,振荡均匀后,与制得的Fe(OH)3胶体一起放置于暗处,分别用激光笔照射烧杯中的液体,可以观察到____ 。该实验可用来区别____ 。
(5)取(3)中制得的Fe(OH)3胶体进行以下实验:
①将其装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,说明____ ,这种现象称为____ 。
②向Fe(OH)3胶体中逐滴滴加过量稀硫酸,边滴边振荡,观察到____ ,其原因是____ 。
(1)向少量红棕色的Fe2O3粉末,加入适量盐酸,发生反应的化学方程式为
(2)取少量上述溶液于试管中,滴入几滴NaOH溶液,可观察到
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈
(4)取另一只盛有20mL蒸馏水的小烧杯,向其中加入1mLFeCl3溶液,振荡均匀后,与制得的Fe(OH)3胶体一起放置于暗处,分别用激光笔照射烧杯中的液体,可以观察到
(5)取(3)中制得的Fe(OH)3胶体进行以下实验:
①将其装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,说明
②向Fe(OH)3胶体中逐滴滴加过量稀硫酸,边滴边振荡,观察到
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学为了检验家中的一瓶补铁药(成分为FeSO4)是否变质,设计了如下实验:将药片除去糖衣研细后,溶解过滤,取滤液分别加入两支试管中,再进行如下图所示操作。 请填出该同学实验中出现以下现象时所应得到的结论:
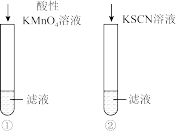
现象 | 结论 |
| ①中酸性KMnO4溶液褪色 ②中KSCN溶液不变色 | |
| ①中酸性KMnO4溶液不褪色 ②中KSCN溶液变红 | |
| ①中酸性KMnO4溶液褪色 ②中KSCN溶液变红 |

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某小组研究铁与水蒸气的反应,两位同学分别进行了如下实验。
请回答:
(1)实验Ⅰ中湿棉花的作用是______ ,实验Ⅰ反应的化学方程式是__________________ 。
(2)甲同学观察到实验Ⅰ中持续产生肥皂泡,用火柴点燃肥皂泡,目的是_______ 。
(3)乙同学观察到实验Ⅰ中持续产生肥皂泡,实验Ⅱ中溶液B未呈现红色。说明溶液A中含有_____ 。
(4)丙同学观察到实验室Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色。丙同学分析原因并进行实验验证:
①结合化学用语和必要文字说明溶液B未呈现红色的原因___________ 。
②取未呈现红色的溶液B少许于试管中,通入少量氯气,观察到_______ ,证明分析原因正确。
③通入少量氯气发生反应的离子方程式为_______________ 。
| 实验Ⅰ | 实验Ⅱ |
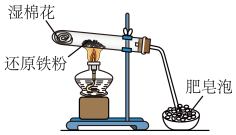 | 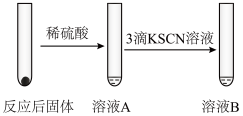 |
(1)实验Ⅰ中湿棉花的作用是
(2)甲同学观察到实验Ⅰ中持续产生肥皂泡,用火柴点燃肥皂泡,目的是
(3)乙同学观察到实验Ⅰ中持续产生肥皂泡,实验Ⅱ中溶液B未呈现红色。说明溶液A中含有
(4)丙同学观察到实验室Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色。丙同学分析原因并进行实验验证:
①结合化学用语和必要文字说明溶液B未呈现红色的原因
②取未呈现红色的溶液B少许于试管中,通入少量氯气,观察到
③通入少量氯气发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】现有未知固体粉末,含有K+、Fe3+、Ba2+、 、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:
、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:
(1)取少量固体粉末溶于水中,固体完全溶解且溶液无色透明,证明该固体粉末中无___________ (填离子符号);
(2)有同学提出质疑,直接观察溶液颜色并不能作为判断的标准,可能含量太少观察不出来,取(1)中少量溶液于试管中加入___________ 溶液,发现溶液变为红色。
(3)另取(1)中少量溶液于试管中,滴加少量的稀硫酸,发现有白色沉淀产生,证明该固体粉末中有___________ (填离子符号),并写出离子方程式___________ 。
(4)另取(1)中少量溶液进行焰色试验,透过蓝色钴玻璃观察,火焰呈紫色,证明该固体粉末中有___________ (填离子符号);
(5)取(1)中少量溶液,加入硝酸银溶液,发现无明显现象,证明该固体粉末中无___________ (填离子符号),该固体粉末中一定有 ,原因是
,原因是___________ 。
 、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:
、Cl—中的几种。化学兴趣小组的同学进行了如下实验,回答下列问题:(1)取少量固体粉末溶于水中,固体完全溶解且溶液无色透明,证明该固体粉末中无
(2)有同学提出质疑,直接观察溶液颜色并不能作为判断的标准,可能含量太少观察不出来,取(1)中少量溶液于试管中加入
(3)另取(1)中少量溶液于试管中,滴加少量的稀硫酸,发现有白色沉淀产生,证明该固体粉末中有
(4)另取(1)中少量溶液进行焰色试验,透过蓝色钴玻璃观察,火焰呈紫色,证明该固体粉末中有
(5)取(1)中少量溶液,加入硝酸银溶液,发现无明显现象,证明该固体粉末中无
 ,原因是
,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】锰是重要的合金材料和催化剂,在工农业生产和科技领域有广泛的用途。请回答下列问题:
(1)溶液中的Mn2+可被酸性 溶液氧化为MnO4-,该方法可用于检验Mn2+。
溶液氧化为MnO4-,该方法可用于检验Mn2+。
①检验时的实验现象为_________ 。
②该反应的离子方程式为___________ 。
③ 可看成两分子硫酸偶合所得,若硫酸的结构式为
可看成两分子硫酸偶合所得,若硫酸的结构式为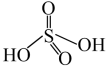 ,则
,则 的结构式为
的结构式为_________ 。
(2)实验室用含锰废料(主要成分 ,含有少量
,含有少量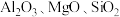 )制备Mn的流程如下:
)制备Mn的流程如下:
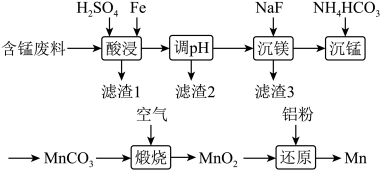
已知:Ⅰ.难溶物的溶度积常数如下表所示:
Ⅱ.溶液中离子浓度≤10-5 mol·L-1时,认为该离子沉淀完全。
①“酸浸”时, 将Fe氧化为Fe3+。该反应的离子方程式为
将Fe氧化为Fe3+。该反应的离子方程式为________ ;该过程中时间和液固比对锰浸出率的影响分别如图1、图2所示:
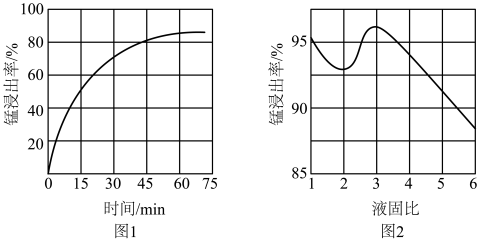
则适宜的浸出时间和液固比分别为___________ 、___________ 。
②若“酸浸”后所得滤液中c(Mn2+)=0.18 mol·L-1,则“调pH”的范围为___________ 。
③“煅烧”反应中氧化剂和还原剂的物质的量之比为_______ 。“还原”时所发生的反应在化学上又叫做_________ 。
(1)溶液中的Mn2+可被酸性
 溶液氧化为MnO4-,该方法可用于检验Mn2+。
溶液氧化为MnO4-,该方法可用于检验Mn2+。①检验时的实验现象为
②该反应的离子方程式为
③
 可看成两分子硫酸偶合所得,若硫酸的结构式为
可看成两分子硫酸偶合所得,若硫酸的结构式为 ,则
,则 的结构式为
的结构式为(2)实验室用含锰废料(主要成分
 ,含有少量
,含有少量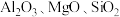 )制备Mn的流程如下:
)制备Mn的流程如下:
已知:Ⅰ.难溶物的溶度积常数如下表所示:
| 难溶物 |  |  |  |  |
溶度积常数( ) ) | 4.0×10-38 | 1.0×10-33 | 1.8×10-11 | 1.8×10-13 |
①“酸浸”时,
 将Fe氧化为Fe3+。该反应的离子方程式为
将Fe氧化为Fe3+。该反应的离子方程式为
则适宜的浸出时间和液固比分别为
②若“酸浸”后所得滤液中c(Mn2+)=0.18 mol·L-1,则“调pH”的范围为
③“煅烧”反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)向 溶液中加入
溶液中加入 固体,则溶液中c(S2-)
固体,则溶液中c(S2-)__________ (填“增大”或“减小”)。
(2)25℃,在 溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与
溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与 关系如图(忽略溶液体积的变化、
关系如图(忽略溶液体积的变化、 的挥发)。
的挥发)。
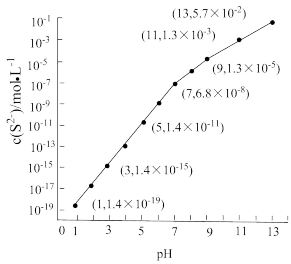
①pH=13时,溶液中的
_______ 
②某溶液含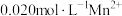 、
、 ,当溶液pH=
,当溶液pH=_______ 时, 开始沉淀[已知:
开始沉淀[已知: ]。
]。
(3)25℃,两种酸的电离平衡常数如下表。
① 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为_______ 。
②向 溶液中通入少量二氧化硫时反应的离子方程式为
溶液中通入少量二氧化硫时反应的离子方程式为_______ 。
(4)银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。已知 ,若向
,若向  的
的  溶液中加入
溶液中加入 的盐酸,混合后溶液中的
的盐酸,混合后溶液中的 的浓度为
的浓度为_______  。
。
(1)向
 溶液中加入
溶液中加入 固体,则溶液中c(S2-)
固体,则溶液中c(S2-)(2)25℃,在
 溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与
溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与 关系如图(忽略溶液体积的变化、
关系如图(忽略溶液体积的变化、 的挥发)。
的挥发)。
①pH=13时,溶液中的


②某溶液含
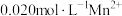 、
、 ,当溶液pH=
,当溶液pH= 开始沉淀[已知:
开始沉淀[已知: ]。
]。(3)25℃,两种酸的电离平衡常数如下表。
| Ka1/mol/L | Ka2/mol/L | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
①
 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为②向
 溶液中通入少量二氧化硫时反应的离子方程式为
溶液中通入少量二氧化硫时反应的离子方程式为(4)银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。已知
 ,若向
,若向  的
的  溶液中加入
溶液中加入 的盐酸,混合后溶液中的
的盐酸,混合后溶液中的 的浓度为
的浓度为 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某工厂以重晶石(主要含BaSO4)为原料,生产“电子陶瓷工业支柱”——钛酸钡(BaTiO3)的工艺流程如图:
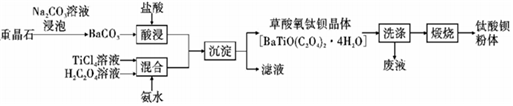
回答下列问题:
(1)为提高BaCO3的酸浸速率,可采取的措施为____ (写出一条即可)。常温下,TiCl4为液体且易水解,配制一定浓度的TiCl4溶液的方法是___ 。
(2)用Na2CO3溶液浸泡重晶石(假设杂质不与Na2CO3反应),能将BaSO4转化为BaCO3,此反应的平衡常数K=____ (填写计算结果)。若不考虑CO 的水解,要使2.33gBaSO4恰好完全转化为BaCO3,则至少需要浓度为1.0mol•L-1Na2CO3溶液
的水解,要使2.33gBaSO4恰好完全转化为BaCO3,则至少需要浓度为1.0mol•L-1Na2CO3溶液___ mL(已知:Ksp(BaSO4)=1.0×10-10、Ksp(BaCO3)=5.0×10-9)。
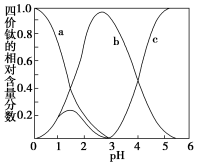
(3)流程中“混合”溶液的钛元素以TiO(OH)+、TiOC2O4、TiO(C2O4) 三种形式存在,其分布随pH发生变化.在制备过程中,先用氨水调节混合溶液的pH,再进行“沉淀”.请写出“沉淀”过程的离子方程式
三种形式存在,其分布随pH发生变化.在制备过程中,先用氨水调节混合溶液的pH,再进行“沉淀”.请写出“沉淀”过程的离子方程式____ 。
(4)流程中“滤液”的主要成分为___ (写化学式)。

回答下列问题:
(1)为提高BaCO3的酸浸速率,可采取的措施为
(2)用Na2CO3溶液浸泡重晶石(假设杂质不与Na2CO3反应),能将BaSO4转化为BaCO3,此反应的平衡常数K=
 的水解,要使2.33gBaSO4恰好完全转化为BaCO3,则至少需要浓度为1.0mol•L-1Na2CO3溶液
的水解,要使2.33gBaSO4恰好完全转化为BaCO3,则至少需要浓度为1.0mol•L-1Na2CO3溶液(3)流程中“混合”溶液的钛元素以TiO(OH)+、TiOC2O4、TiO(C2O4)
 三种形式存在,其分布随pH发生变化.在制备过程中,先用氨水调节混合溶液的pH,再进行“沉淀”.请写出“沉淀”过程的离子方程式
三种形式存在,其分布随pH发生变化.在制备过程中,先用氨水调节混合溶液的pH,再进行“沉淀”.请写出“沉淀”过程的离子方程式
(4)流程中“滤液”的主要成分为
您最近一年使用:0次



