有A 、B 、C 、D四种元素都为短周期元素,原子序数依次增大,A元素原子最外层电子数是其内层电子数的3倍, B 元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质,C为原子核内有14个中子的金属,当1.8克C与足量B的最高价氧化物对应水化物反应时,在标准状况下放出气体2.24L ,D的M层上7个电子。
(1)写出各元素名称:A____ ,B_____ ,C_____ ,D_____ ;
其中D在周期表中的位置:___________________ 。
(2)B的离子结构示意图:______________ 。
(3)分别写出B和D的最高价氧化物的水化物的化学式______ ,_______ .
(4)比较D的气态氢化物与H2S和HF的稳定性:___________________ (由强到弱排列)。
(5)写出B与C 的最高价氧化物对应水化物之间发生反应的离子方程式:______________ 。
(1)写出各元素名称:A
其中D在周期表中的位置:
(2)B的离子结构示意图:
(3)分别写出B和D的最高价氧化物的水化物的化学式
(4)比较D的气态氢化物与H2S和HF的稳定性:
(5)写出B与C 的最高价氧化物对应水化物之间发生反应的离子方程式:
更新时间:2017-05-20 20:09:11
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】短周期主族元素A、B、C、D、E、F、G的原子序数依次增大,在元素周期表中A的原子半径最小,B与C相邻且 的最外层电子数是次外层的3倍,D为同周期中金属性最强的元素,C、F同主族,E是地壳中含量最多的金属元素。回答下列问题:
的最外层电子数是次外层的3倍,D为同周期中金属性最强的元素,C、F同主族,E是地壳中含量最多的金属元素。回答下列问题:
(1)C在元素周期表中的位置为第_______ 周期_______ 族,G的元素符号是_______ 。
(2)B的原子结构示意图为_______
(3)比较 和
和 离子半径大小:
离子半径大小:_______ (用离子符号表示);
(4)比较 和
和 简单氢化物的热稳定性强弱:
简单氢化物的热稳定性强弱:_______ (用化学式表示)。
(5) 和
和 的最高价氧化物的水化物酸性较强的是
的最高价氧化物的水化物酸性较强的是_______ (用化学式表示)。
(6) 的氧化物与
的氧化物与 的最高价氧化物对应水化物的溶液反应的离子方程式为
的最高价氧化物对应水化物的溶液反应的离子方程式为_______ 。
 的最外层电子数是次外层的3倍,D为同周期中金属性最强的元素,C、F同主族,E是地壳中含量最多的金属元素。回答下列问题:
的最外层电子数是次外层的3倍,D为同周期中金属性最强的元素,C、F同主族,E是地壳中含量最多的金属元素。回答下列问题:(1)C在元素周期表中的位置为第
(2)B的原子结构示意图为
(3)比较
 和
和 离子半径大小:
离子半径大小:(4)比较
 和
和 简单氢化物的热稳定性强弱:
简单氢化物的热稳定性强弱:(5)
 和
和 的最高价氧化物的水化物酸性较强的是
的最高价氧化物的水化物酸性较强的是(6)
 的氧化物与
的氧化物与 的最高价氧化物对应水化物的溶液反应的离子方程式为
的最高价氧化物对应水化物的溶液反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知X、Y、Z、R、W、Q六种元素中,X的原子序数为1;Y元素原子最外层电子数是内层电子总数的2倍;Z元素原子次外层电子数比其最外层电子数少4个;R元素原子最外层有1个电子,其阳离子与Z的阴离子原子核外电子总数相同;W元素原子K层和M层电子总数等于其L层电子数。请要求填空:
(1)Z元素形成的原子的结构示意图为___________ ;
(2)从前五种元素中选出三种元素组成化合物,其中属于碱的是___________ (填化学式);属于非电解质的是___________ (填一种物质的名称即可);
(3)现有标准状况下YZ和 混合气体8.96L,其质量为16g,则该气体中,YZ和
混合气体8.96L,其质量为16g,则该气体中,YZ和 的物质的量之比为
的物质的量之比为___________ ;
(4)55.0g化合物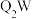 中含有
中含有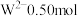 ,则Q的相对原子质量为
,则Q的相对原子质量为___________ ;
(5)将4.00gRZX溶于一定量水,所得溶液的体积为100mL,该溶液中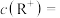
___________ ;
(6)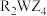 溶于水的电离方程式
溶于水的电离方程式___________ ;
(7)化合物 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
(1)Z元素形成的原子的结构示意图为
(2)从前五种元素中选出三种元素组成化合物,其中属于碱的是
(3)现有标准状况下YZ和
 混合气体8.96L,其质量为16g,则该气体中,YZ和
混合气体8.96L,其质量为16g,则该气体中,YZ和 的物质的量之比为
的物质的量之比为(4)55.0g化合物
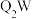 中含有
中含有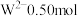 ,则Q的相对原子质量为
,则Q的相对原子质量为(5)将4.00gRZX溶于一定量水,所得溶液的体积为100mL,该溶液中
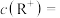
(6)
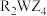 溶于水的电离方程式
溶于水的电离方程式(7)化合物
 与
与 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D四种元素原子序数依次增大;A元素最内层与最外层的电子数相同;B元素L层比K层电子数多5个;C元素的+3价阳离子和氖原子具有相同的电子数;D元素的原子核外有4个电子层,K层和L层电子数之和等于M层与N层电子数之和。写出:
(1)元素符号:A_____________ B____________ C___________ D__________________
(2)A的原子结构示意图____________ ,B离子的电子式____________ ,C的离子结构示意图________________ ,D原子的电子式____________________ 。
(1)元素符号:A
(2)A的原子结构示意图
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】短周期元素X、Y、Z在周期表中位置关系如图所示。

(1)X元素的单质分子式是___ 。若X核内中子数与质子数相等,X单质的摩尔质量是___ 。
(2)Y单质的电子式是___ 。
Y单质与水反应的化学方程式:___ 。
Z与钠形成的化合物的电子式是:___ 。

(1)X元素的单质分子式是
(2)Y单质的电子式是
Y单质与水反应的化学方程式:
Z与钠形成的化合物的电子式是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】元素周期表是我们学习化学,研究物质性质的重要工具。根据元素周期表和元素周期律的相应内容,完成下列3个小题。
(1)图中是7×8的格子,用红笔 画出周期表的轮廓_____

(2)如图是金字塔式元素周期表的一部分,请回答下列问题:

①铁元素位于元素周期表中第4周期_______ 族。
②关于金字塔周期表的上述元素,下列叙述正确的是_______ 。
A.h的最高价氧化物对应的水化物是一种强碱
B.硒化氢的稳定性强于f的氢化物的稳定性
C.c的氢化物的水溶液是强酸
D.原子半径:h>e>f
E.氢化物的酸性:f强于g
③与b同族的短周期元素与b的非金属性强弱关系是_______ (填元素符号)。
④写出元素e,d的最高价氧化物对应水化物之间的反应的离子反应方程式_______ 。
(3)五种短周期元素A、B、C、D、E的主要化合价和原子半径如表所示。
已知:A是非金属元素且C,D同周期。回答下列问题:
①B、D元素组成的化合物的化学式为_______ 。
②写出C和E元素组成化合物的电子式:_______ 。
(1)图中是7×8的格子,用

(2)如图是金字塔式元素周期表的一部分,请回答下列问题:

①铁元素位于元素周期表中第4周期
②关于金字塔周期表的上述元素,下列叙述正确的是
A.h的最高价氧化物对应的水化物是一种强碱
B.硒化氢的稳定性强于f的氢化物的稳定性
C.c的氢化物的水溶液是强酸
D.原子半径:h>e>f
E.氢化物的酸性:f强于g
③与b同族的短周期元素与b的非金属性强弱关系是
④写出元素e,d的最高价氧化物对应水化物之间的反应的离子反应方程式
(3)五种短周期元素A、B、C、D、E的主要化合价和原子半径如表所示。
| 元素代号 | A | B | C | D | E |
| 主要化合价 |  |  |  |   |  |
| 原子半径/nm | 0.082 | 0.037 | 0.160 | 0.110 | 0.071 |
①B、D元素组成的化合物的化学式为
②写出C和E元素组成化合物的电子式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】阅读下面信息,推断元素,按要求回答问题:
| 信息 | 问题 |
| ①短周期元素X、Y、Z、W,原子序数依次增大,最外层电子数均不少于最内层电子数,且四种元素组成的单质常温下均为固体。 | (1)X一定不是 A 氢 B 碳 C 氧 D 硫 |
| ②一定条件下,上述四种元素的单质均能与足量的氧气反应,生成的氧化物有两种能溶于稀硫酸,三种能溶于浓NaOH溶液,氧化物的相对分子质量都大于26 | (2)这四种元素中有铝元素吗? |
| ③向上述四种元素的单质的混合物中,加入足量的盐酸,固体部分溶解,过滤,向滤液中加入过量的烧碱溶液,最终溶液中有白色沉淀 | (3)白色沉淀的化学式为 |
| ④向上述四种元素的单质的混合物中,加入足量的烧碱溶液,固体部分溶解,过滤,向滤液中加入过量的盐酸,最终溶液中有白色沉淀 | (4)生成白色沉淀的离子方程式为 |
| ⑤X与W同主族 | (5)X的单质与W的最高价氧化物反应的化学方程式为 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表为元素周期表的一部分,请回答有关问题:
根据上表回答下列问题:
(1)④元素的原子结构示意图为_______ ,②该元素在周期表中的位置是第二周期第_______ 族。
(2)表中非金属性最强的是_______ (用元素符号表示)。
(3)由⑤⑧元素的形成的化合物的电子式是_______ 。
(4)以下事实能说明⑧非金属性比⑩元素强的是 。
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1)④元素的原子结构示意图为
(2)表中非金属性最强的是
(3)由⑤⑧元素的形成的化合物的电子式是
(4)以下事实能说明⑧非金属性比⑩元素强的是 。
| A.⑧的氢化物比⑩的氢化物稳定 |
| B.⑧的氢化物酸性比⑩的氢化物酸性弱 |
| C.⑧的单质能将⑩从其钠盐溶液中置换出来 |
| D.⑧最高价氧化物对应的水化物的酸性强于⑩最高价氧化物对应的水化物的酸性 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如图为周期表的一小部分,A、B、C、D的位置关系如图所示。且它们均为短周期元素,其中C元素的最外层电子数是电子层数的2倍,回答下列问题:
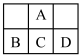
(1)在B、C、D最高价氧化物对应水化物中,酸性最强的是__ (写分子式)。
(2)在A、B、C所形成氢化物中,A的电子式:___ ,其中最稳定的是__ (写分子式)。
(3)写D的单质与C的氢化物反应的化学方程式__ 。
(4)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是__ (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000kg该溶液需消耗氯气的质量为___ kg(保留整数)。

(1)在B、C、D最高价氧化物对应水化物中,酸性最强的是
(2)在A、B、C所形成氢化物中,A的电子式:
(3)写D的单质与C的氢化物反应的化学方程式
(4)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】钛(22Ti)由于其特殊的性能被誉为“未来世纪的金属”。钛铁矿主要成分为FeTiO3(含有少量MgO、SiO2等杂质),Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿来制备,工艺流程如下:
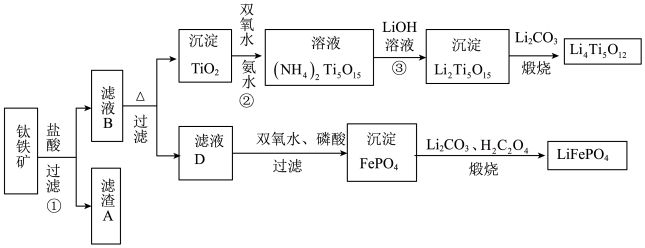
(1)Ti位于元素周期表中的位置为________ 。钛铁矿在预处理时需要进行粉碎,其原因是_______ 。
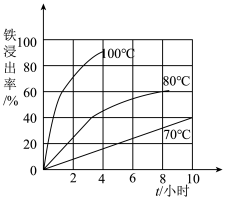
(2)过程①中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为80%时,所采用的实验条件是_________ 。
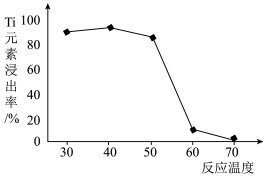
(3)过程②中固体TiO2与双氧水、氨水反应转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示,反应温度过高时,Ti元素浸出率下降的原因是___________ 。
(4)写出由滤液D生成FePO4的离子方程式____________________________________ 。
(5)由流程图可知FePO4制备LiFePO4的化学方程式是_________________________ 。

(1)Ti位于元素周期表中的位置为
(2)过程①中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为80%时,所采用的实验条件是

(3)过程②中固体TiO2与双氧水、氨水反应转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示,反应温度过高时,Ti元素浸出率下降的原因是

(4)写出由滤液D生成FePO4的离子方程式
(5)由流程图可知FePO4制备LiFePO4的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1)L的元素符号为________ ;M在元素周期表中的位置为________________ ;五种元素的原子半径从大到小的顺序是____________________ (用元素符号表示)。
(2) Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为___ ,B的分子式为____________ 。
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______ ,其最高价氧化物对应的水化物化学式为_______ 。
回答下列问题:
(1)L的元素符号为
(2) Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如图是部分短周期元素(用字母x等表示)化合价与原子序数的关系图。

根据判断出的元素回答问题:
(1)h在周期表中的位置是__________ 。
(2)比较z、f、g、r常见离子的半径大小(用化学式表示,下同):______ >______ >______ >______ ;比较r、m的最高价氧化物对应水化物的酸性强弱:______ >______ >;比较d、m的氢化物的沸点:______ >______ 。
(3)x与氢元素能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式)______ ,实验室制取该物质的化学方程式为:____________________________________ 。
(4)由y、m和氢元素组成一种离子化合物,写出其电子式:___________________________ 。
(5)用铅蓄电池作电源,惰性电极电解饱和em溶液,则电解反应的生成物为(写化学式)___________________________ 。铅蓄电池放电时正极反应式为式)___________________________ 。

根据判断出的元素回答问题:
(1)h在周期表中的位置是
(2)比较z、f、g、r常见离子的半径大小(用化学式表示,下同):
(3)x与氢元素能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式)
(4)由y、m和氢元素组成一种离子化合物,写出其电子式:
(5)用铅蓄电池作电源,惰性电极电解饱和em溶液,则电解反应的生成物为(写化学式)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A、B、C、D、E是原子序数依次增大的五种短周期元素,A与C同主族,A与B、A与E形成共价化合物,A与B形成的最简单化合物的水溶液呈碱性,E的最高正化合价与最低负化合价的代数和为6,D是同周期中简单离子半径最小的元素。
(1)五种元素中,E在元素周期表中的位置是______ ,画出C的原子结构示意图:________ 。
(2)B的气态氢化物与其最高价氧化物对应的水化物反应生成的化合物中存在的化学键类型为_____ 。
(3)C的最高价氧化物对应的水化物与D的最高价氧化物反应的化学方程式为__________________ 。
(4)已知X、Y、Z三种物质中均含有上述元素中的某一种元素,它们之间存在如图所示的转化关系:
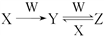
①X、Y、Z均含有同一种金属元素,若W固体俗称干冰,则反应Y→Z的离子方程式为______ ;若W是强碱,且Y是白色难溶固体,则反应Y →Z的离子方程式为__________________ 。
②X、Y、Z是均含有同一种非金属元素的化合物,W是一种常见金属单质,且上述转化均在常温条件下完成,则反应Z→Y的离子方程式为_____________________ 。
(1)五种元素中,E在元素周期表中的位置是
(2)B的气态氢化物与其最高价氧化物对应的水化物反应生成的化合物中存在的化学键类型为
(3)C的最高价氧化物对应的水化物与D的最高价氧化物反应的化学方程式为
(4)已知X、Y、Z三种物质中均含有上述元素中的某一种元素,它们之间存在如图所示的转化关系:
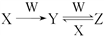
①X、Y、Z均含有同一种金属元素,若W固体俗称干冰,则反应Y→Z的离子方程式为
②X、Y、Z是均含有同一种非金属元素的化合物,W是一种常见金属单质,且上述转化均在常温条件下完成,则反应Z→Y的离子方程式为
您最近一年使用:0次



