设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.常温常压下6.0g乙酸所含σ键数目为0.8NA |
| B.2.0gH218O与D2O的混合物中所含中子数为NA |
| C.标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA |
| D.50mll2mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
更新时间:2017/06/07 09:47:24
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】阿伏加 德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.标准状况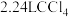 含有共价键数为 含有共价键数为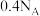 |
B.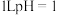 的 的 溶液中 溶液中 的数目为 的数目为 |
C. 与 与 反应生成的 反应生成的 分子数为 分子数为 |
D.钾与水反应生成 时转移电子数为 时转移电子数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为 |
B.常温常压下,7.8g过氧化钠中含有阴离子的数目为 |
C. 为非电解质 为非电解质 |
D.标准状况下,22.4L 与足量的铁充分反应,转移的电子数为 与足量的铁充分反应,转移的电子数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A.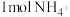 所含电子数目为11 所含电子数目为11 |
B.标准状况下, 含有的分子数为0.5 含有的分子数为0.5 |
C.分子数相等的 和 和 ,所含氧原子数均为2 ,所含氧原子数均为2 |
D.常温常压下,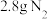 和 和 的混合气体中含有的原子数为0.2 的混合气体中含有的原子数为0.2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA是阿伏加德罗常数的值。下列叙述正确的是
| A.1 L 0.1 mol·L–1氢硫酸中含有的H+数目为0.2NA |
| B.标准状况下,2.24 L丙烷含有的共价键数为0.8NA |
| C.常温下,将2.8 g铁片投入到浓硝酸中,反应转移的电子数为0.15NA |
D.向1 L 0.1 mol·L–1盐酸中滴加氨水至中性,溶液中含有的 数目为0.1NA 数目为0.1NA |
您最近一年使用:0次
【推荐1】关于反应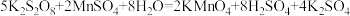 的说法
的说法不正确 的是
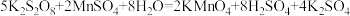 的说法
的说法| A.K2S2O8发生还原反应 |
| B.若设计成原电池,KMnO4为负极产物 |
C.氧化剂和还原剂物质的量之比是 |
D.消耗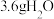 时,转移0.5mol电子 时,转移0.5mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知S元素的最低化合价是–2价,最高化合价是+6价,那么下列物质中的S元素只具有氧化性的是( )
| A.H2S | B.S | C.SO2 | D.H2SO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】如图是一种综合处理含SO2尾气的工艺流程:
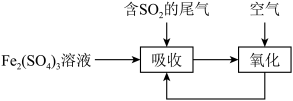
已知“吸收”步骤和“氧化”步骤发生的反应分别为:①2H2O+SO2+Fe2(SO4)3=2FeSO4+2H2SO4;②4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O。若每步反应都完全,下列说法正确的是

已知“吸收”步骤和“氧化”步骤发生的反应分别为:①2H2O+SO2+Fe2(SO4)3=2FeSO4+2H2SO4;②4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O。若每步反应都完全,下列说法正确的是
A.由反应过程中可推知氧化性的强弱顺序: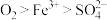 |
| B.“吸收”步骤中Fe2(SO4)3为还原剂,SO2为酸性氧化物 |
| C.处理含1个SO2的尾气,反应①中转移电子数为1个 |
| D.Fe2(SO4)3溶液在上述流程中不可以循环使用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关实验装置进行的相应实验,能达到实验目的的是
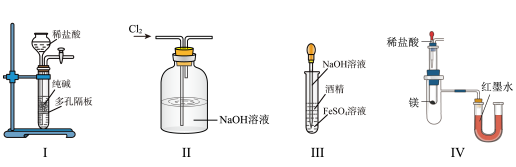

| A.图I:制取少量纯净的CO2气体 |
| B.图II:除去Cl2中含有少量的HCl |
| C.图III:制备Fe(OH)2并能保证较长时间观察到白色 |
| D.图IV:验证镁和稀盐酸反应放热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据如图的转化关系判断下列说法正确的是(反应条件已略去)
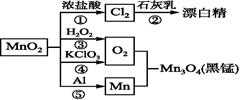

| A.反应①②③④⑤均属于氧化还原反应,反应③还属于置换反应 |
| B.反应⑤说明该条件下铝可用于制熔点较高的金属 |
| C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶1 |
| D.反应①中氧化剂与还原剂的物质的量之比为1∶4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在给定条件下,下列横线上的物质在化学反应中能被完全消耗的是
| A.用10mL10mol/L浓盐酸与10g二氧化锰(式量为87)共热制取氯气 |
| B.通常状况下,将1g铝片投入10L1mol/L的稀硫酸中 |
| C.大量含CO2的CO在电火花作用下与少量Na2O2反应 |
| D.在5×107Pa、500℃和铁触媒催化的条件下,用过量的氮气和氢气合成氨 |
您最近一年使用:0次

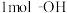 (羟基)与
(羟基)与 中所含的电子数均为
中所含的电子数均为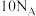 ;
; 苯与足量的
苯与足量的 反应时,参与反应的碳碳双键数为
反应时,参与反应的碳碳双键数为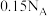
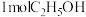 被
被 溶液氧化放出
溶液氧化放出
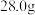 乙烯和丙烯的混合气体中含有的氢原子数为
乙烯和丙烯的混合气体中含有的氢原子数为


