(1)已知反应2H2 + O2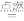 2H2O为放热反应,破坏1mol的化学键消耗的能量称为化学键的键能。有关物质中化学键的键能如下表,则生成1mol水可以放出热量
2H2O为放热反应,破坏1mol的化学键消耗的能量称为化学键的键能。有关物质中化学键的键能如下表,则生成1mol水可以放出热量 __________ kJ
(2)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如下图所示,A、B两个电极均由多孔的碳块组成。
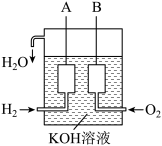
①B作_____ 极材料(填“正”或“负”),电解质溶液中SO42- 移向_____ 极(填“A”或“B”)。
②写出A极的电极反应式_______ ,一段时间后,溶液的PH______ (填“升高”“降低”“不变”),
③如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电池装置,当有标准状况下11.2L CH4完全反应时,导线中通过的电子的数目__________ 。
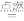 2H2O为放热反应,破坏1mol的化学键消耗的能量称为化学键的键能。有关物质中化学键的键能如下表,则生成1mol水可以放出热量
2H2O为放热反应,破坏1mol的化学键消耗的能量称为化学键的键能。有关物质中化学键的键能如下表,则生成1mol水可以放出热量 | 化学键 | H—H | O=O | H—O |
| 键能kJ/mol | 436 | 496 | 463 |

①B作
②写出A极的电极反应式
③如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电池装置,当有标准状况下11.2L CH4完全反应时,导线中通过的电子的数目
更新时间:2017-06-13 21:37:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能。下表是某些共价键的键能:根据右图中能量变化图,回答下列问题:
(1)图中:a=___________ 。
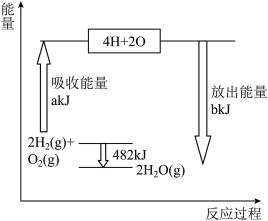
(2)表格中:X=__________ 。
Ⅱ.如图,A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
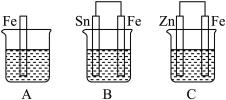
(1)A中反应的离子方程式为_____________________________ 。
(2)B中Sn极的电极反应式为____________________________ 。
(3)C中被腐蚀的金属是________ ,总反应的化学方程式为_________________________ ,
比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为__________ (填序号)。
(1)图中:a=

(2)表格中:X=
| 共价键 | H-H | O=O | H-O |
| 键能/kJ ·mol-1 | 436 | 498 | X |
Ⅱ.如图,A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

(1)A中反应的离子方程式为
(2)B中Sn极的电极反应式为
(3)C中被腐蚀的金属是
比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】能源是人类赖以生存和发展的重要物质基础,常规能源的合理利用和新能源的合理开发是当今社会面临的严峻课题,回答下列问题:
(1)乙醇(C2H5OH)是未来内燃机的首选环保型液体燃料。1 g乙醇完全燃烧生成液态水放出a kJ的热量,则乙醇燃烧的热化学方程式为__________ 。
(2)由于C3H8(g)= C3H6(g)+H2(g) H=+bkJmol(b>0)的反应中,反应物具有的总能量________ (填“大于”“等于”或“小于”)生成物具有的总能量,那么在化学反应时,反应物就需要________ (填“放出”或“吸收”)能量才能转化为生成物。
(3)关于用水制取二次能源氢气,以下研究方向不正确的是________ 。
A 组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B 设法将太阳光聚焦,产生高温,使水分解产生氢气
C 寻找高效催化剂,使水分解产生氢气,同时释放能量
D 寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(4)已知下列两个热化学方程式,
A 2H2(g)+O2(g)=2H2O(l) H = -571.6kJ∙mol-1
B C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) H= -2220kJ∙mol-1
能表示燃烧热的热化学方程式为________ (填A或B)。将标况下22.4L的C3H8和H2混合气体(其中H2的体积分数为1/2),在上述条件下完全燃烧,则放出的热量为________ kJ。
(1)乙醇(C2H5OH)是未来内燃机的首选环保型液体燃料。1 g乙醇完全燃烧生成液态水放出a kJ的热量,则乙醇燃烧的热化学方程式为
(2)由于C3H8(g)= C3H6(g)+H2(g) H=+bkJmol(b>0)的反应中,反应物具有的总能量
(3)关于用水制取二次能源氢气,以下研究方向不正确的是
A 组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B 设法将太阳光聚焦,产生高温,使水分解产生氢气
C 寻找高效催化剂,使水分解产生氢气,同时释放能量
D 寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
(4)已知下列两个热化学方程式,
A 2H2(g)+O2(g)=2H2O(l) H = -571.6kJ∙mol-1
B C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) H= -2220kJ∙mol-1
能表示燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮是地球上含量丰富的一种元素,氮及其化合物对我们的生产、生活有重要的影响。回答下列问题:
(1)机动车发动机工作时会引发 与
与 的反应,该反应是吸热反应,
的反应,该反应是吸热反应, 与
与 的总能量比2molNO的总能量
的总能量比2molNO的总能量___________ (填“高”或“低”)。
(2)已知:
 ,
,
 。下列能量变化示意图中,正确的是___________(填字母)。
。下列能量变化示意图中,正确的是___________(填字母)。
(3) 是一种温室气体,其存储能量的能力是
是一种温室气体,其存储能量的能力是 的上万倍,在大气中的寿命可长达740年。如表所示是断裂1mol某些化学键所需要的能量数据:
的上万倍,在大气中的寿命可长达740年。如表所示是断裂1mol某些化学键所需要的能量数据:
根据上述数据分析最稳定的物质是___________ (填“ ”“
”“ ”或“
”或“ ”),写出
”),写出 和
和 生成
生成 的热化学方程式:
的热化学方程式:___________ 。
(4)火箭的常规燃料是液态四氧化二氮和液态肼( ),
), 作氧化剂。用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂。用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:①
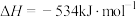
②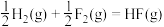
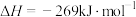
③
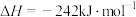
请写出肼和氟气反应的热化学方程式:___________ 。
(1)机动车发动机工作时会引发
 与
与 的反应,该反应是吸热反应,
的反应,该反应是吸热反应, 与
与 的总能量比2molNO的总能量
的总能量比2molNO的总能量(2)已知:

 ,
,
 。下列能量变化示意图中,正确的是___________(填字母)。
。下列能量变化示意图中,正确的是___________(填字母)。A.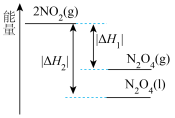 | B.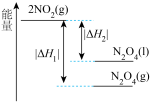 |
C.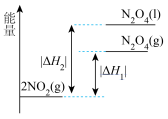 | D.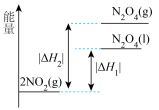 |
 是一种温室气体,其存储能量的能力是
是一种温室气体,其存储能量的能力是 的上万倍,在大气中的寿命可长达740年。如表所示是断裂1mol某些化学键所需要的能量数据:
的上万倍,在大气中的寿命可长达740年。如表所示是断裂1mol某些化学键所需要的能量数据:| 化学键 |  |  |  |
能量 | 946 | 154.8 | 283 |
 ”“
”“ ”或“
”或“ ”),写出
”),写出 和
和 生成
生成 的热化学方程式:
的热化学方程式:(4)火箭的常规燃料是液态四氧化二氮和液态肼(
 ),
), 作氧化剂。用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂。用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。已知:①

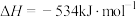
②
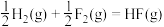
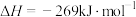
③

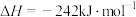
请写出肼和氟气反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图为氢氧燃料电池示意图,按此图的提示,回答下列问题:
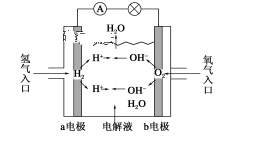
(1)a电极是__________ ,b电极是___________ 。
(2)不管燃料电池的电解液是酸性的还是碱性的,放电后电解质溶液的pH___________ (填“增大”“减小”或“不变”)
(3)当电解质溶液为碱性时,b电极发生的电极反应为:__________________________________________ pH_____________________
(4)氢氧燃料电池是一种______ (填“需要”或“不需要”)将还原剂和氧化剂全部储藏在电池内的新型发电装置

(1)a电极是
(2)不管燃料电池的电解液是酸性的还是碱性的,放电后电解质溶液的pH
(3)当电解质溶液为碱性时,b电极发生的电极反应为:
(4)氢氧燃料电池是一种
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是___________ (至少答出两点)。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:___________ 。
(2)以甲烷为原料可制得氢气。下图是一定温度、压强下, 与
与 反应生成CO(g)和
反应生成CO(g)和 的能量(KJ)变化示意图,写出该反应的热化学方程式
的能量(KJ)变化示意图,写出该反应的热化学方程式___________ ( 用
用 、
、 、
、 表示)。
表示)。 ,同时获得氢气:通由
,同时获得氢气:通由 ,工作原理如图所示。装置通电后,铁电极附近生成紫红色的
,工作原理如图所示。装置通电后,铁电极附近生成紫红色的 ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知: 只在强碱性条件下稳定,易被
只在强碱性条件下稳定,易被 还原。
还原。 降低的区域在
降低的区域在___________ (填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是___________ 。
③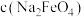 随初始c(NaOH)的变化如下图,分析N点
随初始c(NaOH)的变化如下图,分析N点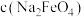 低于最高值的原因:
低于最高值的原因:___________ 。
(1)与汽油相比,氢气作为燃料的优点是
(2)以甲烷为原料可制得氢气。下图是一定温度、压强下,
 与
与 反应生成CO(g)和
反应生成CO(g)和 的能量(KJ)变化示意图,写出该反应的热化学方程式
的能量(KJ)变化示意图,写出该反应的热化学方程式 用
用 、
、 、
、 表示)。
表示)。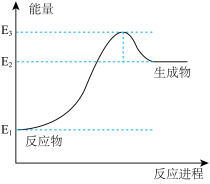
 ,同时获得氢气:通由
,同时获得氢气:通由 ,工作原理如图所示。装置通电后,铁电极附近生成紫红色的
,工作原理如图所示。装置通电后,铁电极附近生成紫红色的 ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知: 只在强碱性条件下稳定,易被
只在强碱性条件下稳定,易被 还原。
还原。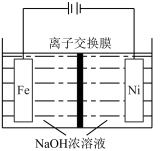
 降低的区域在
降低的区域在②电解过程中,须将阴极产生的气体及时排出,其原因是
③
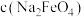 随初始c(NaOH)的变化如下图,分析N点
随初始c(NaOH)的变化如下图,分析N点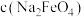 低于最高值的原因:
低于最高值的原因: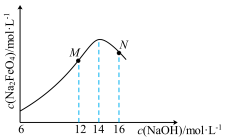
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.被誉为改变未来世界的十大新科技之一的燃料电池。 右图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.
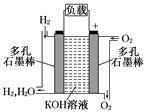
试回答下列问题:
(1)燃料电池的优点是________ ;电解质溶液中的OH -移向______ 极(填“负”或“正”).
(2)写出氢氧燃料电池工作时正极反应式:_______________________ 。
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为___________ .
(4)利用该装置可以处理氮的氧化物和NH 3尾气,总反应为:6NO 2 +8NH 3=7N 2+12H 2O,负极反应式为__________ 。
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为________________ ;
(2)通过导线的电子数为__________ (用 N A表示).

试回答下列问题:
(1)燃料电池的优点是
(2)写出氢氧燃料电池工作时正极反应式:
(3)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,负极反应式为
(4)利用该装置可以处理氮的氧化物和NH 3尾气,总反应为:6NO 2 +8NH 3=7N 2+12H 2O,负极反应式为
II.将锌片和银片浸入稀硫酸中组成原电池,若该电池中两电极的总质量为80 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为41g,试计算:
(1)产生氢气的体积(标准状况)为
(2)通过导线的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】电池是人类生产和生活中的重要能量来源。回答下列问题:
Ⅰ.硅是太阳能电池的重要材料,工业制备高纯硅的主要过程如下:

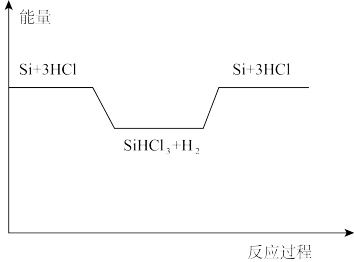
反应②、③的能量变化如右图所示。
(1)硅在元素周期表中的位置是___________ 。
(2)反应①还生成了可燃性气体,其化学方程式为___________ 。
(3)反应②是___________ 反应(填“放热”或“吸热”)。已知 与
与 结构相似,反应③生成
结构相似,反应③生成 时有
时有___________  化学键断裂。
化学键断裂。
Ⅱ.某种燃料电池的工作原理如图所示,a、b均为铂电极。
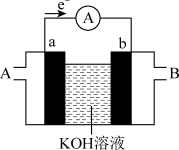
(4)电池工作时,电解质溶液中 向
向___________ 极迁移(填“a”或“b”),当有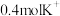 发生迁移,消耗
发生迁移,消耗 的体积为
的体积为___________ L(标准状况下)。
(5)若该电池是氢氧燃料电池,则通入氢气端是___________ (填“A”或“B”)。
Ⅰ.硅是太阳能电池的重要材料,工业制备高纯硅的主要过程如下:

反应②、③的能量变化如右图所示。

(1)硅在元素周期表中的位置是
(2)反应①还生成了可燃性气体,其化学方程式为
(3)反应②是
 与
与 结构相似,反应③生成
结构相似,反应③生成 时有
时有 化学键断裂。
化学键断裂。Ⅱ.某种燃料电池的工作原理如图所示,a、b均为铂电极。

(4)电池工作时,电解质溶液中
 向
向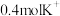 发生迁移,消耗
发生迁移,消耗 的体积为
的体积为(5)若该电池是氢氧燃料电池,则通入氢气端是
您最近一年使用:0次
【推荐2】人类使用能源经历了三个时期。
Ⅰ. 柴草时期
(1)从能量转化的角度看,木材燃烧时化学能主要转化成_______ 能和光能。
Ⅱ. 化石能源时期
(2)天然气的主要成分是甲烷,甲烷的化学式为 ,其结构式为
,其结构式为_______ 。
(3)某化合物分子的球棍模型如图所示,据此写出该物质的结构式________ 。

Ⅲ. 多能源结构时期
(4)基于环保理念,海南省将逐步减少传统燃油汽车的使用,燃料电池汽车将有更广阔的发展前景。如图所示为氢氧燃料电池的示意图,其基本工作原理与铜锌原电池的相同。根据图中电子流动方向判断,A电极是_______ (填“正极”或“负极”);氢氧燃料电池的优点是_________ (写一条即可)。

Ⅰ. 柴草时期
(1)从能量转化的角度看,木材燃烧时化学能主要转化成
Ⅱ. 化石能源时期
(2)天然气的主要成分是甲烷,甲烷的化学式为
 ,其结构式为
,其结构式为(3)某化合物分子的球棍模型如图所示,据此写出该物质的结构式

Ⅲ. 多能源结构时期
(4)基于环保理念,海南省将逐步减少传统燃油汽车的使用,燃料电池汽车将有更广阔的发展前景。如图所示为氢氧燃料电池的示意图,其基本工作原理与铜锌原电池的相同。根据图中电子流动方向判断,A电极是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ书写下列物质的电子式:
O2:______________ N2:____________ .Cl2:______________ H2O:____________ . NaOH:___________ Na2O2:___________ .
Ⅱ 写出下列电极反应式:
(1)碱性锌锰电池负极反应式:____________________________________ .
(2)铅蓄电池的负极反应式:___________________________________________ .
(3)氢氧燃料电池酸性介质的负极反应式:_______________________________ .正极反应式:_______________________________ .
O2:
Ⅱ 写出下列电极反应式:
(1)碱性锌锰电池负极反应式:
(2)铅蓄电池的负极反应式:
(3)氢氧燃料电池酸性介质的负极反应式:
您最近一年使用:0次



