某学习小组同学用如图所示装置进行实验,以探究苯与溴发生反应的原理并分离提纯反应的产物。请回答下列问题:
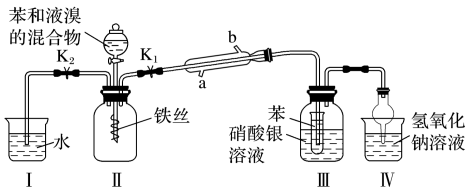
(1)冷凝管所起的作用为冷凝回流蒸气.冷凝水从______________ (填“a”或“b”)口进入。
(2)实验开始时,关闭 K2、开启 K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始,Ⅲ中小试管 内苯的作用是____________ 。
(3)能说明苯与液溴发生了取代反应的现象是______________________________ ;若把Ⅲ中盛于洗气瓶内的硝酸银溶液 换为______________ (填试剂名称),当出现____________________ 现象也能说明发生取代反应。
(4)反应结束后,要让装置 I 中的水倒吸入装置 II 中,这样操作的目的是____________________________ .简述这一操作的方 法_______________________ 。
(5)四个实验装置中能起到防倒吸的装置有________________________ 。
(6)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。
①蒸馏水洗涤,振荡,分液;②用 5%的 NaOH 溶液洗涤,振荡,分液:③用蒸馏水洗涤,振荡,分 液:④加入无水氯化钙干燥。⑤________________ (填操作名称)。
(7)装置Ⅱ中的化学方程式为________________________ ,_________________________ 。
装置Ⅲ中离子方程式为_________________________ .

(1)冷凝管所起的作用为冷凝回流蒸气.冷凝水从
(2)实验开始时,关闭 K2、开启 K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始,Ⅲ中小试管 内苯的作用是
(3)能说明苯与液溴发生了取代反应的现象是
(4)反应结束后,要让装置 I 中的水倒吸入装置 II 中,这样操作的目的是
(5)四个实验装置中能起到防倒吸的装置有
(6)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。
①蒸馏水洗涤,振荡,分液;②用 5%的 NaOH 溶液洗涤,振荡,分液:③用蒸馏水洗涤,振荡,分 液:④加入无水氯化钙干燥。⑤
(7)装置Ⅱ中的化学方程式为
装置Ⅲ中离子方程式为
更新时间:2017-06-13 12:12:41
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】为探究苯与溴的取代反应,甲用下图装置Ⅰ进行如下实验:
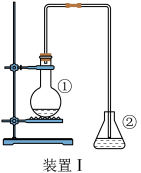
将一定量的苯和溴放在烧瓶中,同时加入少量铁屑做催化剂,3~5分钟后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应。
(1)装置Ⅰ中①的化学方程式为_________________________________ 。
②中离子方程式为__________________________ 。
(2)①中长导管的作用是________________________ 。
(3)烧瓶中生成的红褐色油状液滴的成分是________ ,要想得到纯净的产物,可用NaOH溶液试剂洗涤。洗涤后分离粗产品应使用的仪器是________ 。
(4)甲做实验时,乙观察到烧瓶中液体沸腾并有红棕色气体从导管中逸出,提出必须先除去红棕色气体,才能验证锥形瓶中的产物。原因是__________________________________________ 。
(5)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验。

可选用的试剂是:苯;液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳。a的作用是_____________ ,b中的试剂是_____________ 。

将一定量的苯和溴放在烧瓶中,同时加入少量铁屑做催化剂,3~5分钟后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应。
(1)装置Ⅰ中①的化学方程式为
②中离子方程式为
(2)①中长导管的作用是
(3)烧瓶中生成的红褐色油状液滴的成分是
(4)甲做实验时,乙观察到烧瓶中液体沸腾并有红棕色气体从导管中逸出,提出必须先除去红棕色气体,才能验证锥形瓶中的产物。原因是
(5)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验。

可选用的试剂是:苯;液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳。a的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】化学离不开实验,实验是检验真理的唯一标准。
Ⅰ.某化学实验小组将足量 加入100 mL 0.05mol/L溴水中,溴水褪色。
加入100 mL 0.05mol/L溴水中,溴水褪色。
(1)同学们结合乙醛的结构提出猜想:
甲:乙醛中有氢原子,只与溴水发生取代反应;
乙:乙醛中有不饱和碳原子,只与溴水发生_______ 反应;
丙:溴水有氧化性,乙醛只发生氧化反应。
丁:……
(2)为验证猜想,设计定量实验方案:
取褪色后的溶液于反应容器中,滴加足量的 溶液,产生淡黄色沉淀x mol。
溶液,产生淡黄色沉淀x mol。
①若丙猜想正确,则x=_______ ,反应方程式为_______ 。
②若实际测得x=0.005,_______ (选填“能”或“不能”)证明甲猜想一定正确,原因是_______ 。
Ⅱ.为验证苯与液溴发生取代反应,该小组同学设计实验,装置图如图:
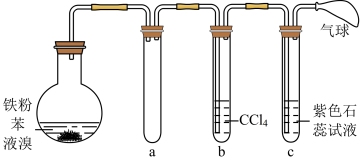
(3)能证明该反应是取代反应的现象是_______ 。
(4)a的作用是_______ 。
(5)实验结束后,发现烧瓶中的液体呈红褐色,为得到纯净的溴苯,同学们设计如图实验方案:

加入试剂X发生的离子反应方程式为_______ 。操作4是_______ 。
Ⅰ.某化学实验小组将足量
 加入100 mL 0.05mol/L溴水中,溴水褪色。
加入100 mL 0.05mol/L溴水中,溴水褪色。(1)同学们结合乙醛的结构提出猜想:
甲:乙醛中有氢原子,只与溴水发生取代反应;
乙:乙醛中有不饱和碳原子,只与溴水发生
丙:溴水有氧化性,乙醛只发生氧化反应。
丁:……
(2)为验证猜想,设计定量实验方案:
取褪色后的溶液于反应容器中,滴加足量的
 溶液,产生淡黄色沉淀x mol。
溶液,产生淡黄色沉淀x mol。①若丙猜想正确,则x=
②若实际测得x=0.005,
Ⅱ.为验证苯与液溴发生取代反应,该小组同学设计实验,装置图如图:

(3)能证明该反应是取代反应的现象是
(4)a的作用是
(5)实验结束后,发现烧瓶中的液体呈红褐色,为得到纯净的溴苯,同学们设计如图实验方案:

加入试剂X发生的离子反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】苯、甲苯,乙苯、二甲苯等均是重要的芳香族化合物。回答下列问题:
(1)苯的实验式为___________ 。
(2)1mol苯与3molH2发生加成反应,碳的杂化类型由___________ ,转化为___________ 。
(3)甲苯的一氯代物有___________ 种,由甲苯制备2,4,6-三硝基甲苯(TNT)的化学方程式为___________ 。
(4)向对二甲苯中加入足量酸性高锰酸钾溶液,生成的有机物中的官能团名称___________ 。
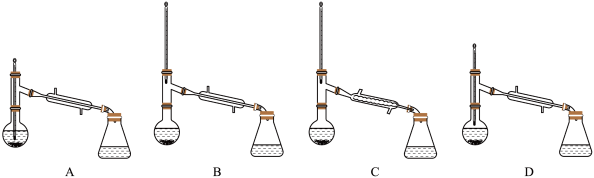
(5)如图是某同学设计的制取少量溴苯(熔点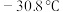 ,沸点
,沸点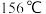 )的装置。实验时,打开K,向圆底烧瓶中滴加苯和溴的混合液,发现a中有微沸现象,b中的液体逐渐变为浅红色,c中有少量气泡产生,反应结束后,对a中的液体进行后续处理即可获得溴苯。
)的装置。实验时,打开K,向圆底烧瓶中滴加苯和溴的混合液,发现a中有微沸现象,b中的液体逐渐变为浅红色,c中有少量气泡产生,反应结束后,对a中的液体进行后续处理即可获得溴苯。___________ 。
②该实验___________ (填“放热”或“吸热”)。
③c中看到的现象证明___________ 。
④得到粗溴苯后,用如下操作进行精制:
①水洗 ②蒸馏 ③用干燥剂干燥 ④10%NaOH溶液洗
正确的操作顺序是___________ (填序号)。
A.①②③④② B.②④②③① C.④①③①② D.①④①③②
⑤进行蒸馏操作中,仪器选择及安装(夹持及加热装置已省略)均正确的是___________ (填字母)。
(1)苯的实验式为
(2)1mol苯与3molH2发生加成反应,碳的杂化类型由
(3)甲苯的一氯代物有
(4)向对二甲苯中加入足量酸性高锰酸钾溶液,生成的有机物中的官能团名称
(5)如图是某同学设计的制取少量溴苯(熔点
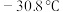 ,沸点
,沸点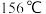 )的装置。实验时,打开K,向圆底烧瓶中滴加苯和溴的混合液,发现a中有微沸现象,b中的液体逐渐变为浅红色,c中有少量气泡产生,反应结束后,对a中的液体进行后续处理即可获得溴苯。
)的装置。实验时,打开K,向圆底烧瓶中滴加苯和溴的混合液,发现a中有微沸现象,b中的液体逐渐变为浅红色,c中有少量气泡产生,反应结束后,对a中的液体进行后续处理即可获得溴苯。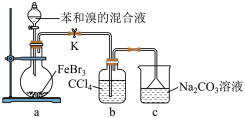
②该实验
③c中看到的现象证明
④得到粗溴苯后,用如下操作进行精制:
①水洗 ②蒸馏 ③用干燥剂干燥 ④10%NaOH溶液洗
正确的操作顺序是
A.①②③④② B.②④②③① C.④①③①② D.①④①③②
⑤进行蒸馏操作中,仪器选择及安装(夹持及加热装置已省略)均正确的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某实验小组采用氯化氢法对实验室NaCl粗品(含少量KNO3)进行提纯,并测定提纯产品中的NaCl纯度。实验装置及步骤如下,回答下列问题:
(1)装置A用于制取HCl气体利用了浓硫酸的性质为___________ (填字母标号),装置A中发生的化学反应方程式为___________ 。
a.脱水性 b.高沸点 c.强氧化性 d.强酸性
(2)仪器a的名称是___________ ,仪器b的作用是___________ 。
(3)B中析出NaCl晶体的原理是___________ 。待晶体不再析出后,停止通气,过滤、洗涤、干燥得到NaCl晶体。
Ⅱ.NaCl晶体纯度测定
称取1.000g干燥的NaCl晶体溶于烧杯中,转入100mL容量瓶,定容、摇匀。
移取10.00mL溶液于锥形瓶中,调节待测液的pH并滴加K2CrO4指示剂。
用0.1000mol/L标准AgNO3溶液在避光下滴定至终点。
(已知:Ag2CrO4为砖红色沉淀)
(4)称取NaCl晶体质量___________ (填“能”或“不能”)使用托盘天平。
(5)终点时的实验现象为___________ 。
(6)平行滴定三次,消耗AgNO3标准溶液的平均体积为17.05mL,所得产品中NaCl晶体纯度为___________ %。(保留小数点后2位)

(1)装置A用于制取HCl气体利用了浓硫酸的性质为
a.脱水性 b.高沸点 c.强氧化性 d.强酸性
(2)仪器a的名称是
(3)B中析出NaCl晶体的原理是
Ⅱ.NaCl晶体纯度测定
称取1.000g干燥的NaCl晶体溶于烧杯中,转入100mL容量瓶,定容、摇匀。
移取10.00mL溶液于锥形瓶中,调节待测液的pH并滴加K2CrO4指示剂。
用0.1000mol/L标准AgNO3溶液在避光下滴定至终点。
(已知:Ag2CrO4为砖红色沉淀)
(4)称取NaCl晶体质量
(5)终点时的实验现象为
(6)平行滴定三次,消耗AgNO3标准溶液的平均体积为17.05mL,所得产品中NaCl晶体纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】如图所示为实验室初步分离甲苯、苯胺、苯甲酸混合溶液的流程。

已知:苯胺(液体)和苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。
回答下列问题:
(1)水相Ⅰ加入氢氧化钠溶液后的分离操作,名称为_____ ,其主要仪器活塞处轻微渗水的处理方法是_____ ;水相Ⅱ加盐酸后分离得到产品③的操作,分离操作使用的玻璃仪器有_____ 。
(2)向有机相Ⅱ中加入过量碳酸钠溶液,反应的离子方程式为_____ 。
(3)产品①和产品③在一定条件下脱水,生成的有机产物结构简式为_____ ;产品②的主要成分为_____ (填名称),一个分子中σ键个数为_____ 。

已知:苯胺(液体)和苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。
回答下列问题:
(1)水相Ⅰ加入氢氧化钠溶液后的分离操作,名称为
(2)向有机相Ⅱ中加入过量碳酸钠溶液,反应的离子方程式为
(3)产品①和产品③在一定条件下脱水,生成的有机产物结构简式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】碘化钠是一种常用的分析试剂,也可用于医疗和照相业。某公司申请了专利:以NaOH、单质碘和水合肼(N2H4·H2O)为原料制备碘化钠。已知:水合肼具有还原性。回答下列问题:
(1)水合肼的制备。反应原理为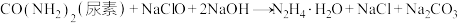 。
。
①制备次氯酸钠和氢氧化钠混合液的相关装置如下:

i.按气流方向,用接口字母表示装置的连接顺序为___________ 。
ii.装置B中盛装的试剂是___________ ,装置D的作用是___________ 。
iii.若该实验温度控制不当,反应后测得三颈瓶内ClO-与 的物质的量之比为4:1,则氯气与氢氧化钠反应的离子方程式为
的物质的量之比为4:1,则氯气与氢氧化钠反应的离子方程式为___________ 。
②为提高水合肼的产率,应采取的操作是___________ (填字母)。
A.缓慢滴加
B.快速滴加
C.将尿素溶液滴入NaClO溶液中
D.将NaClO溶液滴入尿素溶液中
(2)碘化钠的制备。采用水合肼还原法制取碘化钠固体,其制备流程如图所示。
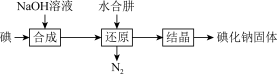
还原过程中,水合肼的作用是除去合成过程中的副产物 ,则合成时产生的I-和
,则合成时产生的I-和 的物质的量之比是
的物质的量之比是___________ 。工业上也可以用硫化钠或铁屑还原 ,但水合肼还原法制得的产品纯度更高,其原因是
,但水合肼还原法制得的产品纯度更高,其原因是___________ 。
(1)水合肼的制备。反应原理为
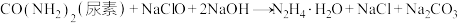 。
。①制备次氯酸钠和氢氧化钠混合液的相关装置如下:

i.按气流方向,用接口字母表示装置的连接顺序为
ii.装置B中盛装的试剂是
iii.若该实验温度控制不当,反应后测得三颈瓶内ClO-与
 的物质的量之比为4:1,则氯气与氢氧化钠反应的离子方程式为
的物质的量之比为4:1,则氯气与氢氧化钠反应的离子方程式为②为提高水合肼的产率,应采取的操作是
A.缓慢滴加
B.快速滴加
C.将尿素溶液滴入NaClO溶液中
D.将NaClO溶液滴入尿素溶液中
(2)碘化钠的制备。采用水合肼还原法制取碘化钠固体,其制备流程如图所示。

还原过程中,水合肼的作用是除去合成过程中的副产物
 ,则合成时产生的I-和
,则合成时产生的I-和 的物质的量之比是
的物质的量之比是 ,但水合肼还原法制得的产品纯度更高,其原因是
,但水合肼还原法制得的产品纯度更高,其原因是
您最近一年使用:0次
【推荐1】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
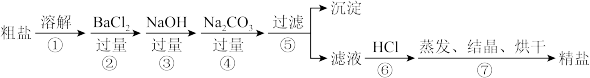
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是___________________________ 。
(2)第②步操作的目的是除去粗盐中的__________ (填化学式),判断BaCl2已过量的方法是____________________________________________________________ 。
(3)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是________________ 。
(4)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、________ 、__________ 。
(5)“蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、酒精灯、火柴、玻璃棒、______ 。
(6)第④步除原食盐中杂质离子与碳酸根的反应外还有的反应的离子方程式为:______________________________ ;
(7)第⑥步操作中涉及反应的离子方程式有:__________________ 、__________________ 。

(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是
(2)第②步操作的目的是除去粗盐中的
(3)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是
(4)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、
(5)“蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、酒精灯、火柴、玻璃棒、
(6)第④步除原食盐中杂质离子与碳酸根的反应外还有的反应的离子方程式为:
(7)第⑥步操作中涉及反应的离子方程式有:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是某研究性学习小组设计制取氯气,并以氯气为反应物进行特定反应的装置。
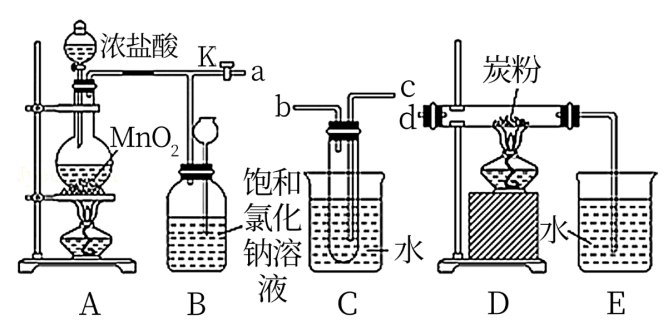
(1)装置A中发生的化学反应方程式___ 。
(2)先要将C装置接入B和D之间,实验开始时先点燃A处酒精灯,打开旋塞K,让Cl2刚好充满整个装置,再点燃D处酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为____ 。
(3)D处反应完毕后,关闭旋塞K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是____ ,B的作用是____ 。
(4)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由____ 。
(5)实验结束后,测得D装置质量减轻1.92 g,E中NaOH溶液(足量)增重36.08 g,可算出D中反应的氯气转化率为____ (转化率=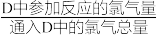 )。
)。

(1)装置A中发生的化学反应方程式
(2)先要将C装置接入B和D之间,实验开始时先点燃A处酒精灯,打开旋塞K,让Cl2刚好充满整个装置,再点燃D处酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为
(3)D处反应完毕后,关闭旋塞K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是
(4)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由
(5)实验结束后,测得D装置质量减轻1.92 g,E中NaOH溶液(足量)增重36.08 g,可算出D中反应的氯气转化率为
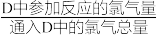 )。
)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】利用CaCl2在碱性条件下与H2O2反应制CaO2.某化学兴趣小组在实验室制备CaO2的实验方案和装置示意图如下:

(已知过氧化钙是一种白色晶体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。)
请回答下列问题:

(1)三颈烧瓶中发生的主要反应的化学方程式为___________ ;
(2)b装置的名称___________ ;支管a的作用___________ ;
(3)步骤③中洗涤CaO2·8H2O的液体A的最佳选择是___________;
(4)过氧化钙可用于长途运输鱼苗,这体现了过氧化钙___________的性质;
(5)已知CaO2在350℃时能迅速分解,生成CaO和O2.该小组采用如图所示的装置测定刚才制备的产品中CaO2的纯度(设杂质不分解产生气体),

①如何检验装置的气密性?___________
②准确称取0.5000g样品,置于试管中加热使其完全分解,收集到44.80mL(已换算为标准状况)气体,则产品中过氧化钙的质量分数___________ (保留4位有效数字)。

(已知过氧化钙是一种白色晶体,无臭无味,能潮解,难溶于水,可与水缓慢反应;不溶于醇类、乙醚等,易与酸反应,常用作杀菌剂、防腐剂等。)
请回答下列问题:

(1)三颈烧瓶中发生的主要反应的化学方程式为
(2)b装置的名称
(3)步骤③中洗涤CaO2·8H2O的液体A的最佳选择是___________;
| A.稀盐酸 | B.无水乙醇 | C.水 | D.CaCl2溶液 |
| A.能潮解 | B.能吸收鱼苗呼出的CO2气体 |
| C.可缓慢供氧 | D.可抑菌 |

①如何检验装置的气密性?
②准确称取0.5000g样品,置于试管中加热使其完全分解,收集到44.80mL(已换算为标准状况)气体,则产品中过氧化钙的质量分数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】苯甲醇与苯甲酸是重要的化工原料,可通过苯甲醛在氢氧化钠水溶液中的歧化反应制得,反应式为:2 +NaOH
+NaOH
 +
+ ,某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:
,某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:

重结晶过程:溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度较小。请根据以上信息,回答问题:
(1)萃取分离苯甲醇与苯甲酸钠时,合适的萃取剂是_______ ,其理由是_______ 充分萃取并静置分层,打开分液漏斗上口的玻璃塞后,上、下层依次分离。
(2)苯甲酸在A、B、C三种溶剂中的溶解度(s)随温度变化的曲线如下图所示:

①重结晶时,合适的溶剂是_______ (填字母)。
②洗涤时采用的合适洗涤剂是_______ (填字母)。
A.饱和食盐水 B.Na2CO3溶液 C.稀硫酸 D.蒸馏水
(3)如图是减压过滤装置,请指出其中一处明显错误:_______ 。

 +NaOH
+NaOH
 +
+ ,某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:
,某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:
重结晶过程:溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度较小。请根据以上信息,回答问题:
(1)萃取分离苯甲醇与苯甲酸钠时,合适的萃取剂是
(2)苯甲酸在A、B、C三种溶剂中的溶解度(s)随温度变化的曲线如下图所示:

①重结晶时,合适的溶剂是
②洗涤时采用的合适洗涤剂是
A.饱和食盐水 B.Na2CO3溶液 C.稀硫酸 D.蒸馏水
(3)如图是减压过滤装置,请指出其中一处明显错误:

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】金属钴在航空航天、电器制造等领域有着广泛的应用。以水钴矿(主要成分为Co2O3,含少量CuO、Fe3O4、Al2O3、MnO)为原料提取碳酸钴与单质钴的工艺流程如图所示。
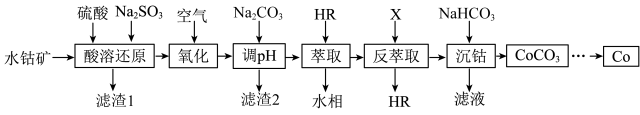
已知:部分阳离子以氢氧化物形式完全沉淀时溶液的pH如表。
请回答下列问题:
(1)酸溶过程中为提高钴的利用率,可采取的措施是_______ (写出一种即可)。
(2)还原过程中主要反应的离子方程式为_______ ,氧化过程中消耗的氧化剂与还原剂的物质的量之比为________ 。
(3)pH的调控范围是_______ ,HR必须具备的性质是________ 。
(4)沉钴时不宜使用Na2CO3,原因是_______ 。
(5)由CoCO3制备Co包括热分解、热还原两个过程,写出热还原过程的化学方程式________ 。

已知:部分阳离子以氢氧化物形式完全沉淀时溶液的pH如表。
| 金属离子 | Fe3+ | Fe2+ | Co2+ | Cu2+ | Al3+ | Mn2+ |
| 开始沉淀的pH | 2.3 | 7.5 | 7.6 | 4.4 | 3.4 | 7.7 |
| 完全沉淀的pH | 3.2 | 8.3 | 9.2 | 5.7 | 5.2 | 9.8 |
(1)酸溶过程中为提高钴的利用率,可采取的措施是
(2)还原过程中主要反应的离子方程式为
(3)pH的调控范围是
(4)沉钴时不宜使用Na2CO3,原因是
(5)由CoCO3制备Co包括热分解、热还原两个过程,写出热还原过程的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】溴和碘的提取方法有多种,试回答下列问题。
Ⅰ.空气吹出法是目前海水提溴的最主要方法之一。其工艺流程如下:

(1)写出步骤③的离子方程式:_______ 。
(2)步骤⑤的蒸馏过程中,温度应控制在80~90 ℃,温度过高或过低都不利于生产。实验室里蒸馏所用的盛装混合物的仪器名称为____ ,为控制温度,最好采用的加热方式为____ ;溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离,分离仪器的名称是____ 。
(3)溴水混合物Ⅱ中溶有一定量的氯气,因此在步骤⑤中可将蒸馏产生的气体通过____ (填试剂名称)溶液,以除去氯气。
(4)提取溴单质,采用蒸馏“溴水混合物Ⅱ”而不是蒸馏“溴水混合物Ⅰ”,请说明原因:_______ 。
Ⅱ.实验室从含碘废液(除H2O外,还含有CCl4、I2、I-等)中回收碘,其实验过程如下:

(5)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_______ ;
(6)该操作将I2还原为I-的目的是_______ 。操作X的名称为____ 。
Ⅰ.空气吹出法是目前海水提溴的最主要方法之一。其工艺流程如下:

(1)写出步骤③的离子方程式:
(2)步骤⑤的蒸馏过程中,温度应控制在80~90 ℃,温度过高或过低都不利于生产。实验室里蒸馏所用的盛装混合物的仪器名称为
(3)溴水混合物Ⅱ中溶有一定量的氯气,因此在步骤⑤中可将蒸馏产生的气体通过
(4)提取溴单质,采用蒸馏“溴水混合物Ⅱ”而不是蒸馏“溴水混合物Ⅰ”,请说明原因:
Ⅱ.实验室从含碘废液(除H2O外,还含有CCl4、I2、I-等)中回收碘,其实验过程如下:

(5)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为
(6)该操作将I2还原为I-的目的是
您最近一年使用:0次



