下列关于碱金属元素和卤素的说法中,错误的是
| A.随核电荷数的增加,碱金属元素和卤素的原子半径都逐渐增大 |
| B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强 |
| C.KOH比NaOH碱性强 |
| D.溴单质与水的反应比氯单质与水的反应更剧烈 |
更新时间:2017-06-14 20:10:10
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】如下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是
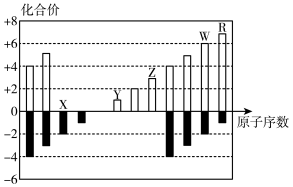

| A.气态氢化物的稳定性:X<W |
| B.X与Y可以形成阴阳离子个数比为1:1和1:2的两种离子化合物 |
| C.由X、Y、Z、W、R五种元素形成的简单离子中半径最小的是X2- |
| D.Y和W可以形成离子化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】几种短周期元素的原子半径及主要化合价如图所示,下列叙述正确的是
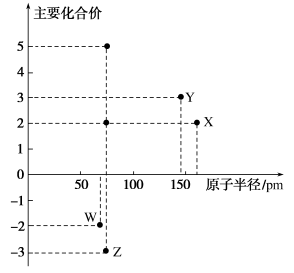

| A.X、Y的最高价氧化物都是两性氧化物 |
B.Y的最高价氧化物对应的水化物能溶于 溶液 溶液 |
| C.Z的非金属性强于W |
| D.X的单质在第三周期中还原性最强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关周期表、周期律的叙述,正确的是
| A.第ⅠA族除H外均为碱金属元素,对应单质均需要保存于煤油中 |
B.第ⅦA族卤素单质 (X2)与水反应均可以用: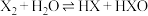 来表示 来表示 |
| C.同周期简单离子半径随原子序数增大而递减 |
| D.锑(Sb)元素位于第五周期第ⅤA族,原子序数为51 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】镓(31Ga)与砷(33As)形成的化合物砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入了“快车道”。下列有关说法不正确的是
| A.Ga位于元素周期表第四周期 | B.Ga为门捷列夫预言的“类铝” |
| C.砷在通常状况下是固体 | D.砷化氢(AsH3)比NH3稳定 |
您最近一年使用:0次



