(1)碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。
已知浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中 为:
为:_______ ,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(2)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl−,利用Ag+与CrO42−生成砖红色沉淀,指示到达滴定终点。当溶液中Cl−恰好沉淀完全(浓度等于1.0×10−5 mol·L−1)时,溶液中c(Ag+)为_______ mol·L−1,此时溶液中c(CrO42−)等于__________ mol·L−1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10−12和2.0×10−10)。
已知浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中
 为:
为:(2)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl−,利用Ag+与CrO42−生成砖红色沉淀,指示到达滴定终点。当溶液中Cl−恰好沉淀完全(浓度等于1.0×10−5 mol·L−1)时,溶液中c(Ag+)为
更新时间:2017-06-30 12:13:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度[S/(mol/L)]如图。
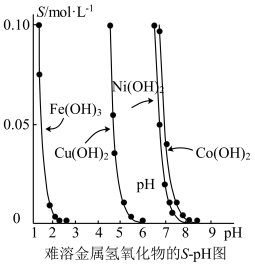
(1)pH=3时溶液中铜元素的主要存在形式是_______ 。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为_______ 。
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含的少量的Co2+杂质,_______ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是_______ 。
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式_______ 。
(5)已知常温下一些难溶物的溶度积常数如表:
常温下,饱和HgS溶液中c(Hg2+)=_______ mol·L-1,某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的_______ 除去它们(选填序号)。
A.NaOH B.FeS C.Na2S

(1)pH=3时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.<1 B.4左右 C.>6
(3)在Ni(OH)2溶液中含的少量的Co2+杂质,
(4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以加入氨水,生成[Cu(NH3)4]2+,写出反应的离子方程式
(5)已知常温下一些难溶物的溶度积常数如表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
常温下,饱和HgS溶液中c(Hg2+)=
A.NaOH B.FeS C.Na2S
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】锰废渣的硫酸浸出液含有大量 、
、 、
、 以及少量的
以及少量的 、
、 、
、 、
、 。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。
。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。 表示,萃取金属离子时,发生反应:
表示,萃取金属离子时,发生反应: (
( 代表被萃取的金属)。
代表被萃取的金属)。
(1)已知: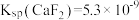 ,
,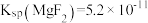 ,向除铁后的溶液中加入
,向除铁后的溶液中加入 ,当溶液中
,当溶液中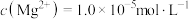 时,
时,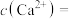
___________  。(保留1位有效数字)
。(保留1位有效数字)
 、
、 、
、 以及少量的
以及少量的 、
、 、
、 、
、 。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。
。通过沉淀-萃取法可以回收其中的锰、钴、镍,流程如图所示。
 表示,萃取金属离子时,发生反应:
表示,萃取金属离子时,发生反应: (
( 代表被萃取的金属)。
代表被萃取的金属)。(1)已知:
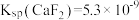 ,
,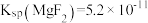 ,向除铁后的溶液中加入
,向除铁后的溶液中加入 ,当溶液中
,当溶液中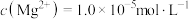 时,
时,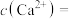
 。(保留1位有效数字)
。(保留1位有效数字)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】磷、碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下面问题:
(1)H3PI是一种三元弱酸,常温下其三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13。
①利用Ka与Kh的相对大小判断:常温下,NaH2PI的水溶液pH_______ 7(填“>”、“<”或“=”)。
②常温下,Na2HPI的水溶液中Kh =____________ (保留2位有效数字)。
(2)已知常温下,Ksp(AgCl)=1.8×10-10;Ksp(AgI)=9.0×10-17 ;Ksp(Ag2CrO4)=1.0×10-12。AgI为黄色固体;Ag2CrO4为红棕色固体。
①向AgCl悬浊液中加入适量KI溶液,发生AgCl(s)+I-(aq)⇌AgI(s)+Cl-(aq),该反应的化学平衡常数K=______________ 。
②测定水体中氯化物的含量,常用标准硝酸银法进行滴定,滴定时应加入的指示剂是________ 。
a.KI b.K2CrO4 c.KCl
滴定终点时锥形瓶中颜色的变化:__________________________________ 。
(3)某溶液中c(Fe3+)=c(Mg2+)=0.02 mol·L-1,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全,即溶液中c(Fe3+)=1.0×10-5 mol·L-1,此时是否有Mg3(PO4)2沉淀生成?(FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24)_________________ (列式计算)。
(1)H3PI是一种三元弱酸,常温下其三级电离常数分别是Ka1=7.1×10-3,Ka2=6.2×10-8,Ka3=4.5×10-13。
①利用Ka与Kh的相对大小判断:常温下,NaH2PI的水溶液pH
②常温下,Na2HPI的水溶液中Kh =
(2)已知常温下,Ksp(AgCl)=1.8×10-10;Ksp(AgI)=9.0×10-17 ;Ksp(Ag2CrO4)=1.0×10-12。AgI为黄色固体;Ag2CrO4为红棕色固体。
①向AgCl悬浊液中加入适量KI溶液,发生AgCl(s)+I-(aq)⇌AgI(s)+Cl-(aq),该反应的化学平衡常数K=
②测定水体中氯化物的含量,常用标准硝酸银法进行滴定,滴定时应加入的指示剂是
a.KI b.K2CrO4 c.KCl
滴定终点时锥形瓶中颜色的变化:
(3)某溶液中c(Fe3+)=c(Mg2+)=0.02 mol·L-1,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全,即溶液中c(Fe3+)=1.0×10-5 mol·L-1,此时是否有Mg3(PO4)2沉淀生成?(FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24)
您最近一年使用:0次



