已知反应2I-+S2O82-====I2+2SO42-,加入淀粉溶液可观察到溶液变蓝色。反应速率可以用淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。20℃时得到如下实验数据:
分析上述数据,下列说法正确的是
| 实验编号 | C(I-)/ mol•L | C(S2O82-)/ mol•L | t/s |
| 1 | 0.040 | 0.040 | 88.0 |
| 2 | 0.080 | 0.040 | 44.0 |
| 3 | 0.080 | 0.080 | 22.0 |
| 4 | 0.160 | 0.020 | 44.0 |
| 5 | 0.120 | 0.040 | 29.3 |
| A.I-的浓度越大,反应速率越快 |
| B.S2O82- 的浓度越大,反应速率越快 |
| C.该实验的目的是研究 I- 与S2O82- 的浓度对反应速率的影响 |
| D.5个实验中,编号3对应浓度的实验,反应速率最慢 |
更新时间:2017-07-08 15:15:25
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】10mL浓度为1mol・L-1的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应率但又不影响氢气生成量的是( )
| A.H2SO4 | B.K2SO4 | C.Na2CO3 | D.CuSO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在 的反应中,在其它条件不变的情况下,采取下列措施,其中能够使反应速率增大的措施是
的反应中,在其它条件不变的情况下,采取下列措施,其中能够使反应速率增大的措施是
 的反应中,在其它条件不变的情况下,采取下列措施,其中能够使反应速率增大的措施是
的反应中,在其它条件不变的情况下,采取下列措施,其中能够使反应速率增大的措施是| A.缩小容器体积 | B.增加碳的量 | C.恒压通入CO | D.恒容下充入N2 |
您最近一年使用:0次
【推荐3】下列实验的现象及相应的结论都正确的是
| 结论 | 选项 | 实验操作和现象 |
| A | 用坩埚钳夹住一小块用砂纸打磨过的铝箔在酒精灯上加热,熔化后无液滴滴落 | 金属铝的熔点很高 |
| B | 取两支试管,分别加入4mL0.01mol/LKMnO4酸性溶液,然后向一支试管中加入0.01mol/LH2C2O4溶液20mL,向另一支试管中加入0.01mol/L H2C2O4溶液40mL,第一支试管中褪色时间长 | 混合后KMnO4浓度不等,且生成的锰离子可作为催化剂,此现象不能确定浓度越大,反应速率越快 |
| C | 铜粉加入稀硫酸中加热,无明显现象,再加少量硝酸钾固体,振荡后溶液变蓝 | 硝酸钾起催化作用 |
| D | 无水乙醇与浓硫酸共热至170℃,将产生的气体通入溴水,溴水褪色 | 有乙烯生成,乙烯和溴水发生加成反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】100 mL 6mol/L硫酸溶液与过量锌粉反应,在一定温度下,为了减缓反应速率但又不影响生成氢气的总量,可向反应物中加入适量的
| A.碳酸钠 | B.水 | C.将稀硫酸改为浓硫酸 | D.烧碱溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】为探究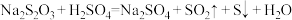 反应速率的影响因素,某同学设计了以下实验,下列说法正确的是
反应速率的影响因素,某同学设计了以下实验,下列说法正确的是
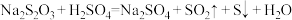 反应速率的影响因素,某同学设计了以下实验,下列说法正确的是
反应速率的影响因素,某同学设计了以下实验,下列说法正确的是| 锥形瓶号 | 反应温度/℃ |  溶液/mL 溶液/mL | 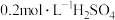 溶液/mL 溶液/mL |  | 浑浊出现时间/s | 备注 |
| 1 | 20 | 10 | 10 | 0 | 10 | |
| 2 | 20 | 10 | 5 | X | 16 | |
| 3 | 40 | 10 | 10 | 0 | 5 | 第10s开始浑浊不再增加 |
A.该实验也可以用 的体积变化来定量表示化学反应的快慢 的体积变化来定量表示化学反应的快慢 |
B.3号瓶用 表示0~10s内的平均反应速率为 表示0~10s内的平均反应速率为 |
| C.由1号瓶和2号瓶实验结果可得增大硫酸浓度,反应速率加快 |
| D.2号瓶中X的值等于6 |
您最近一年使用:0次



