已知:①Fe2O3(s)+3C(s) ===2Fe(s)+3CO(g) ΔH=+494kJ·mol-1
②CO(g)+1/2O2(g) ===CO2(g) ΔH=-283 kJ·mol-1
③C(s)+1/2O2(g)===CO(g) ΔH=-110kJ·mol-1
则反应Fe2O3(s)+3C(s)+ 3/2O2(g) ===2Fe(s)+3CO2(g)的焓变是
②CO(g)+1/2O2(g) ===CO2(g) ΔH=-283 kJ·mol-1
③C(s)+1/2O2(g)===CO(g) ΔH=-110kJ·mol-1
则反应Fe2O3(s)+3C(s)+ 3/2O2(g) ===2Fe(s)+3CO2(g)的焓变是
| A.-355 kJ | B.+355 kJ | C.-355 kJ • mol-1 | D.+355 kJ • mol-1 |
更新时间:2017-09-11 07:09:05
|
【知识点】 盖斯定律与热化学方程式解读
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】工业合成尿素以NH3和CO2作为原料,其能量转化关系如图。

已知2NH3(l)+CO2(g)=H2O(l)+H2NCONH2(l) △H=—103.7kJ·mol-1。下列有关说法正确的是

已知2NH3(l)+CO2(g)=H2O(l)+H2NCONH2(l) △H=—103.7kJ·mol-1。下列有关说法正确的是
| A.△S1>0,△H4>0 |
| B.△H1=—10.0kJ·mol-1 |
| C.H2NCONH4比H2NCONH2能量低,更稳定 |
| D.过程③反应速率慢,使用合适催化剂可减小△H3而加快反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】氢能是最具前景的清洁能源之一,目前水分解制氢技术及贮氢材料的开发应用都取得了很大进展。已知:2H2(g)+ O2(g)=2H2O(1)∆H=-571.6kJ·mol-1。下列说法错误的是
| A.1mol H2O(l)分解制得1molH2需要吸收571.6kJ的能量 |
| B.氢气作为新能源具有热值高、无污染、资源丰富、可再生等优点 |
| C.贮氢材料具有能大量、快速和高效率地吸收和释放氢气的特点 |
| D.利用太阳能光催化分解水制氢是一种理想的制氢手段 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】CO2催化加氢合成二甲醚是一种CO2转化方法,其过程中主要发生下列反应:
反应Ⅰ:CO2(g)+H2(g) CO(g)+H2O(g) △H1
CO(g)+H2O(g) △H1
反应Ⅱ:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H2
CH3OCH3(g)+3H2O(g) △H2
恒压,投入1 mol CO2和适当过量的H2,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。其中:

CH3OCH3的选择性=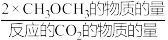 ×100%
×100%
下列说法中不正确 的是
反应Ⅰ:CO2(g)+H2(g)
 CO(g)+H2O(g) △H1
CO(g)+H2O(g) △H1反应Ⅱ:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) △H2
CH3OCH3(g)+3H2O(g) △H2恒压,投入1 mol CO2和适当过量的H2,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。其中:

CH3OCH3的选择性=
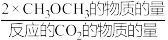 ×100%
×100%下列说法中
| A.△H1>0,△H2<0 |
| B.温度高于300℃,反应Ⅰ正移程度超过反应Ⅱ逆移程度 |
| C.220℃时,反应一段时间后,测得CH3OCH3的选择性为48%(即图中A点)。此时反应Ⅰ和Ⅱ均未达到平衡状态 |
| D.若平衡时CH3OCH3的选择性为48%,则体系中c(CH3OCH3)∶c(CO)=48∶52 |
您最近一年使用:0次



