煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.在煤的气化反应器中发生如下几种反应:
C(s)十H2O(g)═CO(g)+H2(g)△H=+131kJ/mol
C(s)+O2(g)═CO2(g)△H=﹣394kJ/mol
CO(g)+1/2O2(g)═CO2(g)△H=﹣283kJ/mol
则CO(g)+H2O(g) H2(g)+CO2(g)△H=
H2(g)+CO2(g)△H=____ .
C(s)十H2O(g)═CO(g)+H2(g)△H=+131kJ/mol
C(s)+O2(g)═CO2(g)△H=﹣394kJ/mol
CO(g)+1/2O2(g)═CO2(g)△H=﹣283kJ/mol
则CO(g)+H2O(g)
 H2(g)+CO2(g)△H=
H2(g)+CO2(g)△H=
更新时间:2017-10-18 19:51:38
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2、和CO的燃烧热(△H)分别为﹣890.2kJ•mol﹣1、﹣285.8kJ•mol﹣1和﹣283.0kJ•mol﹣1,则生成1mol CO所需热量为_____ .
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】在101 kPa时,1 g CH4完全燃烧生成CO2和液态H2O,放出55.64 kJ的热量。
(1)写出CH4燃烧热表示的热化学方程式。
(2)1000 L CH4(标准状况)燃烧后所产生的热量为多少?
(1)写出CH4燃烧热表示的热化学方程式。
(2)1000 L CH4(标准状况)燃烧后所产生的热量为多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】(1)已知SO2(g)+ 1/2 O2(g)  SO3(g) △H = -98.30kJ/mol,现将4molSO2与一定量O2混合后充分反应,当放出314.56kJ热量时,SO2的转化率为
SO3(g) △H = -98.30kJ/mol,现将4molSO2与一定量O2混合后充分反应,当放出314.56kJ热量时,SO2的转化率为_________________ 。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:_____________________________
(3)在一定条件下,CH4 和CO的燃烧的热化学方程式分别为:
CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g ) △H = -890 kJ/mol
2CO ( g ) + O2 ( g ) = 2CO2 ( g ) △H = -566 kJ/mol
一定量的CH4和CO的混合气体完全燃烧时,放出的热量为262.9 kJ,生成的CO2用过量的饱和石灰水完全吸收,可得到50 g白色沉淀。求混合气体中CH4 和CO的体积比_____________ 。
 SO3(g) △H = -98.30kJ/mol,现将4molSO2与一定量O2混合后充分反应,当放出314.56kJ热量时,SO2的转化率为
SO3(g) △H = -98.30kJ/mol,现将4molSO2与一定量O2混合后充分反应,当放出314.56kJ热量时,SO2的转化率为(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
(3)在一定条件下,CH4 和CO的燃烧的热化学方程式分别为:
CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g ) △H = -890 kJ/mol
2CO ( g ) + O2 ( g ) = 2CO2 ( g ) △H = -566 kJ/mol
一定量的CH4和CO的混合气体完全燃烧时,放出的热量为262.9 kJ,生成的CO2用过量的饱和石灰水完全吸收,可得到50 g白色沉淀。求混合气体中CH4 和CO的体积比
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】氮及其化合物与人们的生活息息相关。
(1)氮元素在周期表中的位置是_______ 。
(2)实验室可用铜与稀硝酸反应制取NO,其离子方程式是_______ 。为防止环境污染,可用碱液吸收氮的氧化物。NO与NO2按物质的量之比1:1被NaOH溶液完全吸收后得到一种钠盐,该化学方程式是________________ 。
(3)已知:① CH4(g) + 4 NO2(g) = 4 NO(g) + CO2(g) +2 H2O(g)ΔH= -574 kJ·mol-1
② CH4(g) + 4 NO(g) =2N2(g) + CO2(g) + 2 H2O(g) ΔH= -1160 kJ·mol-1
根据①和②,标准状况下,4.48 L CH4恰好将NO2转化为N2时,ΔH=__________ 。
由反应①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) ΔH____ -574 kJ·mol-1。
(4)同温同压下,3.5 L NH3恰好将3.0 L NO和NO2的混合气完全转化为N2,则原混合气中 NO和NO2的体积比是__ 。
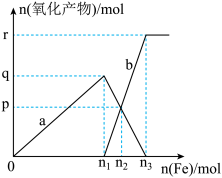
(5)含有1mol HNO3的稀硝酸分别与不同质量的铁粉,所得氧化产物a、b与铁粉物质的量关系如下图所示。 b是________ n3 =_________ p=_________ 。
(1)氮元素在周期表中的位置是
(2)实验室可用铜与稀硝酸反应制取NO,其离子方程式是
(3)已知:① CH4(g) + 4 NO2(g) = 4 NO(g) + CO2(g) +2 H2O(g)ΔH= -574 kJ·mol-1
② CH4(g) + 4 NO(g) =2N2(g) + CO2(g) + 2 H2O(g) ΔH= -1160 kJ·mol-1
根据①和②,标准状况下,4.48 L CH4恰好将NO2转化为N2时,ΔH=
由反应①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) ΔH
(4)同温同压下,3.5 L NH3恰好将3.0 L NO和NO2的混合气完全转化为N2,则原混合气中 NO和NO2的体积比是
(5)含有1mol HNO3的稀硝酸分别与不同质量的铁粉,所得氧化产物a、b与铁粉物质的量关系如下图所示。 b是

您最近一年使用:0次
【推荐2】为防止氮的氧化物污染空气,可用活性炭或一氧化碳还原氮氧化物。
已知: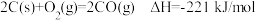 ①
①
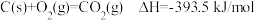 ②
②
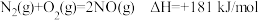 ③
③
回答下列问题:
Ⅰ.消除上述气体污染物可用CO与NO反应生成 和
和 。
。
(1)请完成热化学方程式: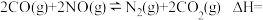
___________  ,反应的平衡常数表达式为
,反应的平衡常数表达式为
___________ 。
(2)为提高此反应中NO的转化率,下列措施可行的是___________ (填字母代号)。
A.增大压强 B.升高温度
C.使用催化剂 D.增大CO的浓度
Ⅱ.向2 L的密闭容器中加入活性炭(足量)和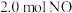 ,发生反应:
,发生反应: 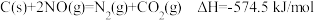
NO和 的物质的量变化如下表所示:
的物质的量变化如下表所示:
(1)0~5 min内,以 表示的该反应速率
表示的该反应速率
___________  ,该条件下的平衡常数
,该条件下的平衡常数
___________ 。
(2)第15 min后,温度调整到 ,则
,则
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)若30 min时,温度保持 不变,向该容器中再加入该四种反应混合物各
不变,向该容器中再加入该四种反应混合物各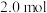 ,则此时反应
,则此时反应___________ (填“正向”“逆向”或“不”)移动。
已知:
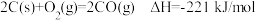 ①
①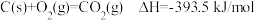 ②
②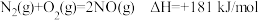 ③
③回答下列问题:
Ⅰ.消除上述气体污染物可用CO与NO反应生成
 和
和 。
。(1)请完成热化学方程式:
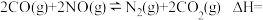
 ,反应的平衡常数表达式为
,反应的平衡常数表达式为
(2)为提高此反应中NO的转化率,下列措施可行的是
A.增大压强 B.升高温度
C.使用催化剂 D.增大CO的浓度
Ⅱ.向2 L的密闭容器中加入活性炭(足量)和
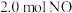 ,发生反应:
,发生反应: 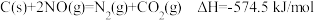
NO和
 的物质的量变化如下表所示:
的物质的量变化如下表所示:物质的量浓度/( ) ) | 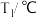 | 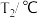 | |||||
| 0 | 5min | 10min | 15min | 20min | 25min | 30min | |
| NO |  | 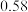 |  |  |  | 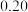 | 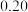 |
 | 0 | 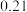 | 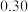 | 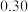 | 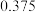 |  |  |
(1)0~5 min内,以
 表示的该反应速率
表示的该反应速率
 ,该条件下的平衡常数
,该条件下的平衡常数
(2)第15 min后,温度调整到
 ,则
,则
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)若30 min时,温度保持
 不变,向该容器中再加入该四种反应混合物各
不变,向该容器中再加入该四种反应混合物各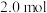 ,则此时反应
,则此时反应
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】(1)已知:①CO(g)+ O2(g)=CO2(g)△H=-283.0kJ•mol-1
O2(g)=CO2(g)△H=-283.0kJ•mol-1
②CH3OH(l)+ O2(g)=CO2(g)+2H2O(l)△H=-726.5kJ•mol-1
O2(g)=CO2(g)+2H2O(l)△H=-726.5kJ•mol-1
请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______ 。
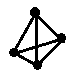
(2)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则1molN4气体转化为2molN2时的△H=______ 。
 O2(g)=CO2(g)△H=-283.0kJ•mol-1
O2(g)=CO2(g)△H=-283.0kJ•mol-1 ②CH3OH(l)+
 O2(g)=CO2(g)+2H2O(l)△H=-726.5kJ•mol-1
O2(g)=CO2(g)+2H2O(l)△H=-726.5kJ•mol-1 请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(2)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则1molN4气体转化为2molN2时的△H=

您最近一年使用:0次



