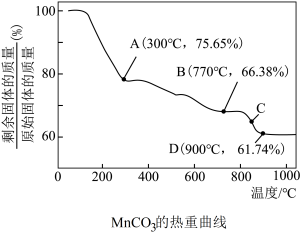
酸雨是指含有一定酸性的物质,pH值小于5.6的雨水,主要是由于含硫矿物燃料燃烧、含硫矿石的冶炼产生的二氧化硫以及氮氧化物等排放到大气中,然后进行了一系列的变化形成的。
(1)用化学方程式表示直接排放含SO2的烟气形成酸雨的过程:_____________ 。
(2)为消除二氧化硫的污染,通常需要对原料或烟气进行处理,某种脱硫技术的基本原理如下:
该技术的第一步反应的离子方程式为____________ 。
处理1千克含75% FeS2的黄铁矿,共消耗O2(标况)的体积为__________ L。
(3)工业生产中的尾气(主要成分为NO2和NO)可用纯碱溶液吸收,有关的化学方程式为
2NO2+Na2CO3=NaNO2+NaNO3+CO2↑ NO+NO2+Na2CO3=2NaNO2+CO2↑
NO、NO2的混合气体可用NOx表示,则混合气体被氢氧化钠完全吸收时X的取值范围为___________ 。
(4)利用氨水可用将SO2和NO2吸收,原理如下图所示:
NO2被吸收的离子方程式是_____________ 。
(1)用化学方程式表示直接排放含SO2的烟气形成酸雨的过程:
(2)为消除二氧化硫的污染,通常需要对原料或烟气进行处理,某种脱硫技术的基本原理如下:

该技术的第一步反应的离子方程式为
处理1千克含75% FeS2的黄铁矿,共消耗O2(标况)的体积为
(3)工业生产中的尾气(主要成分为NO2和NO)可用纯碱溶液吸收,有关的化学方程式为
2NO2+Na2CO3=NaNO2+NaNO3+CO2↑ NO+NO2+Na2CO3=2NaNO2+CO2↑
NO、NO2的混合气体可用NOx表示,则混合气体被氢氧化钠完全吸收时X的取值范围为
(4)利用氨水可用将SO2和NO2吸收,原理如下图所示:

NO2被吸收的离子方程式是
更新时间:2017-10-19 20:58:08
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】下图为实验室某浓盐酸试剂瓶标签上的有关信息,试根据标签上的有关数据,回答下列问题(一)(二):(计算结果保留一位小数)

(一).(1)浓盐酸中HCl的物质的量浓度为________ mol·L-1。
(2) 量取________ mL浓盐酸加水稀释就得到500 mL、0.4mol·L-1的稀盐酸。
(二).取该浓盐酸10g与某MgCl2溶液90g混合,向混合溶液中逐滴加入10%的NaOH溶液,生成的沉淀的质量与加入的NaOH溶液质量关系如下图所示。

回答下列问题
(1)A点溶液的溶质化学式为_______________ 。
(2)与MgCl2反应的溶质氢氧化钠的质量为__________ g。
(3)恰好沉淀完全时,C点所得溶液中溶质的质量分数为______________________ 。

(一).(1)浓盐酸中HCl的物质的量浓度为
(2) 量取
(二).取该浓盐酸10g与某MgCl2溶液90g混合,向混合溶液中逐滴加入10%的NaOH溶液,生成的沉淀的质量与加入的NaOH溶液质量关系如下图所示。

回答下列问题
(1)A点溶液的溶质化学式为
(2)与MgCl2反应的溶质氢氧化钠的质量为
(3)恰好沉淀完全时,C点所得溶液中溶质的质量分数为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】有一稀硫酸和硝酸铁的混合溶液,向其中加入铁粉,溶液中的 Fe2+浓度如图所示(不考虑溶液体积的变化):
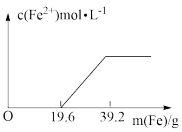
(1)铁离子和铁粉会反应,请写出反应的离子方程式_______
(2)溶液中H2SO4与 Fe(NO3)3的物质的量之比为_______

(1)铁离子和铁粉会反应,请写出反应的离子方程式
(2)溶液中H2SO4与 Fe(NO3)3的物质的量之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】某溶液只可能含有Fe2+、Mg2+、Cu2+、NH 、Al3+、Cl-、OH-中的一种或几种。当加入一种淡黄色固体并加热时,有刺激性气味气体和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系如图所示。用该淡黄色物质做焰色反应,火焰呈黄色。
、Al3+、Cl-、OH-中的一种或几种。当加入一种淡黄色固体并加热时,有刺激性气味气体和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系如图所示。用该淡黄色物质做焰色反应,火焰呈黄色。
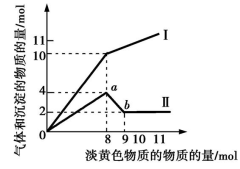
请回答下列问题:
(1)所加的淡黄色固体是_______ (写化学式)。
(2)生成气体的曲线是_____ (填“Ⅰ”或“Ⅱ”)。
(3)生成气体的离子方程式为________________________ 。
(4)ab段发生反应的离子方程式为_____________________ 。
(5)原溶液中含有的离子是____________ ,所含离子的物质的量浓度之为_____ 。
 、Al3+、Cl-、OH-中的一种或几种。当加入一种淡黄色固体并加热时,有刺激性气味气体和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系如图所示。用该淡黄色物质做焰色反应,火焰呈黄色。
、Al3+、Cl-、OH-中的一种或几种。当加入一种淡黄色固体并加热时,有刺激性气味气体和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系如图所示。用该淡黄色物质做焰色反应,火焰呈黄色。
请回答下列问题:
(1)所加的淡黄色固体是
(2)生成气体的曲线是
(3)生成气体的离子方程式为
(4)ab段发生反应的离子方程式为
(5)原溶液中含有的离子是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)写出下列反应的离子方程式。
①酸性KMnO4溶液和草酸(H2C2O4)溶液反应_____ 。
②硫代硫酸钠与稀硫酸反应_____ 。
③用硫氰化钾溶液检验Fe3+_____ 。
(2)利用电解技术,以氯化氢为原料回收氯气的过程如图所示,回答下列问题:H+由_____ 极区向_____ 极区迁移(填阴、阳);阳极电极反应式:____ ;阴极电极反应式:______ 。
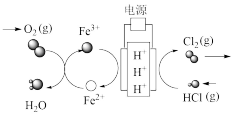
(3)燃料种类很多,如氢氧燃料电池(如KOH为电解液)。写出该电池电极反应式正极:______ ;负极:_____ 。
(4)氯碱工业原理的化学方程式:______ 。如图为用阳离子交换膜法进行该工业生产的装置示意图,标出a~f处所对应的原料或产品:_____ 。

生成0.4kg烧碱时,转移电子的物质的量是____ mol。(相对原子质量Na-23、H-1、O-16)
①酸性KMnO4溶液和草酸(H2C2O4)溶液反应
②硫代硫酸钠与稀硫酸反应
③用硫氰化钾溶液检验Fe3+
(2)利用电解技术,以氯化氢为原料回收氯气的过程如图所示,回答下列问题:H+由
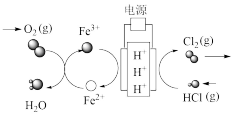
(3)燃料种类很多,如氢氧燃料电池(如KOH为电解液)。写出该电池电极反应式正极:
(4)氯碱工业原理的化学方程式:

生成0.4kg烧碱时,转移电子的物质的量是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】(1)取300 mL 0.2 mol/L的 KI溶液与一定量的酸性 KMnO4 溶液恰好反应,生成等物质的量的 I2和 KIO3,则消耗 KMnO4的物质的量是___ mol。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是___ ,又变为棕黄色的原因是(用离子方程式解释)____ 。
(3)在 100 mLFeBr2 溶液中通入标准状况下3.36 L Cl2,溶液中有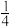 的 Br -被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为
的 Br -被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为_____ mol/L。
(4)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。
①写出该反应的化学方程式____ 。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是___ 。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
(3)在 100 mLFeBr2 溶液中通入标准状况下3.36 L Cl2,溶液中有
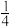 的 Br -被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为
的 Br -被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为(4)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。
①写出该反应的化学方程式
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
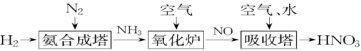
【推荐1】氮元素形成的化合物种类十分丰富。请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题: 的说法中,不正确的是___________(填字母)。
的说法中,不正确的是___________(填字母)。
(2) 易溶于水,标准状况下,用充满
易溶于水,标准状况下,用充满 的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为
的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为___________  。
。
(3)氨气燃烧的化学方程式为___________ 。
(4) 是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、铁钝化,说明浓硝酸具有很强的
是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、铁钝化,说明浓硝酸具有很强的___________ 性。
(5)“吸收塔”尾部会有含NO、 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
①纯碱溶液吸收法。
纯碱溶液与 反应的原理为
反应的原理为
___________ 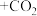 (请填写完成化学方程式,已配平)。
(请填写完成化学方程式,已配平)。
②氨转化法。
已知7mol氨恰好能将含NO和 共6mol的混合气体完全转化为
共6mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比为
的物质的量之比为___________ ,若用通式 表示氮氧化物,则每摩尔氨可将
表示氮氧化物,则每摩尔氨可将___________ mol的 转化为
转化为 。
。
(6)工业上可采用碱液吸收和氨还原处理含 尾气,其中用碱液吸收的化学方程式为
尾气,其中用碱液吸收的化学方程式为 ,
, 。根据上述原理,下列气体中被过量NaOH溶液吸收后有气体剩余的是___________。
。根据上述原理,下列气体中被过量NaOH溶液吸收后有气体剩余的是___________。
 的说法中,不正确的是___________(填字母)。
的说法中,不正确的是___________(填字母)。A.工业合成 需要在高温、高压、催化剂下进行 需要在高温、高压、催化剂下进行 |
B. 可用来生产碳铵和尿素等化肥 可用来生产碳铵和尿素等化肥 |
C. 可用浓硫酸或无水氯化钙干燥 可用浓硫酸或无水氯化钙干燥 |
D. 受热易分解,须置于冷暗处保存 受热易分解,须置于冷暗处保存 |
 易溶于水,标准状况下,用充满
易溶于水,标准状况下,用充满 的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为
的烧瓶做喷泉实验,水充满整个烧瓶后所形成溶液的物质的量浓度为 。
。(3)氨气燃烧的化学方程式为
(4)
 是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、铁钝化,说明浓硝酸具有很强的
是一种重要的化工原料,工厂生产出的浓硝酸可用铝槽车或铁槽车来运输。在常温下能使铝、铁钝化,说明浓硝酸具有很强的(5)“吸收塔”尾部会有含NO、
 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用以下两种方法处理:①纯碱溶液吸收法。
纯碱溶液与
 反应的原理为
反应的原理为
 (请填写完成化学方程式,已配平)。
(请填写完成化学方程式,已配平)。②氨转化法。
已知7mol氨恰好能将含NO和
 共6mol的混合气体完全转化为
共6mol的混合气体完全转化为 ,则混合气体中NO和
,则混合气体中NO和 的物质的量之比为
的物质的量之比为 表示氮氧化物,则每摩尔氨可将
表示氮氧化物,则每摩尔氨可将 转化为
转化为 。
。(6)工业上可采用碱液吸收和氨还原处理含
 尾气,其中用碱液吸收的化学方程式为
尾气,其中用碱液吸收的化学方程式为 ,
, 。根据上述原理,下列气体中被过量NaOH溶液吸收后有气体剩余的是___________。
。根据上述原理,下列气体中被过量NaOH溶液吸收后有气体剩余的是___________。A.1mol  和4mol 和4mol  | B.1mol NO和4mol  |
C.1mol  和7mol NO 和7mol NO | D.4mol NO和4mol  |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】将19.2g的铜和某浓度的硝酸反应,生成8.96L(标况)的气体,则参加反应的硝酸为____ mol,将这8.96L的气体和标况下________ L的氧气混合,再通入水中没有气体剩余。
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】工业上用氨气与空气的混合气在一定条件下制硝酸,发生的反应是:
①4NH3+5O2 →4NO+6H2O
②4NO+3O2+2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空及计算:
(1)为使氨气恰好完全氧化为一氧化氮,氨气与空气的混合气中氨的体积分数(用小数表示)为________ (保留2位小数)。现将1 mol的氨气与12 mol的空气混合反应,可得到硝酸___________ mol;
(2)向上述溶液中加入________ mL 20%的硝酸(密度1.11g/mL),才能得到69%的硝酸溶液。
(3)现有100mol的原料气,其中含氨气为xmol,反应后生成的硝酸ymol。在得到硝酸的条件下,写出x与y的关系式。(写出解题过程)________________
①4NH3+5O2 →4NO+6H2O
②4NO+3O2+2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空及计算:
(1)为使氨气恰好完全氧化为一氧化氮,氨气与空气的混合气中氨的体积分数(用小数表示)为
(2)向上述溶液中加入
(3)现有100mol的原料气,其中含氨气为xmol,反应后生成的硝酸ymol。在得到硝酸的条件下,写出x与y的关系式。(写出解题过程)
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】有下列物质:A.甲醛 B.葡萄糖 C.乙醇 D.乙酸 E.油脂 F.二氧化硫 G.氢氧化铝 (填写序号):
(1)工业上制备肥皂的主要原料是_________ ;
(2)注射时用于皮肤杀菌、消毒的物质主要成分是_________ ;
(3)能用于除去热水瓶胆水垢〔主要成分:CaCO3,Mg(OH)2〕的是_________ ;
(4)既能与强酸反应又能与强碱反应生成盐和水的物质是_________ ;
(5)形成酸雨的主要物质是_________ ;
(6)可用于标本制作的防腐剂的是_________ ;
(7)糖尿病人通常是指病人的尿液中_________ 的含量高。
(1)工业上制备肥皂的主要原料是
(2)注射时用于皮肤杀菌、消毒的物质主要成分是
(3)能用于除去热水瓶胆水垢〔主要成分:CaCO3,Mg(OH)2〕的是
(4)既能与强酸反应又能与强碱反应生成盐和水的物质是
(5)形成酸雨的主要物质是
(6)可用于标本制作的防腐剂的是
(7)糖尿病人通常是指病人的尿液中
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】空气质量与我们的健康息息相关,目前我国通过监测6项污染物的百分比浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物。
(1)上述3种气体直接排入空气后会引起酸雨的气体有_______________ (填化学式)。
(2)早期人们曾经使用铅室法生产硫酸,其主要反应为:SO2(g)+NO2(g) SO3(g)+NO(g)
SO3(g)+NO(g)
①若已知2SO2(g)+O2(g) 2SO3(g) + Q1 2NO(g)+O2(g)
2SO3(g) + Q1 2NO(g)+O2(g)  2NO2(g) + Q2
2NO2(g) + Q2
则SO2(g)+NO2(g) SO3(g)+NO(g)+ Q3 , Q3=
SO3(g)+NO(g)+ Q3 , Q3=_________ kJ·mol-1。
②一定温度下,向固定体积为2 L的密闭容器中充入SO2和NO2各1 mol,发生反应:SO2(g)+NO2(g) SO3(g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是
SO3(g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是____ (选填序号)。
a.体系压强保持不变 b.混合气体的颜色保持不变
c.NO的物质的量保持不变 d.每生成1 mol SO3的同时消耗1 mol NO2
(3)矿石燃料的燃烧是造成酸雨的主要因素之一 。而甲醇日趋成为重要的有机燃料,通常利用CO和H2 合成甲醇,其反应的化学方程式为CO(g)+ 2H2(g) CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
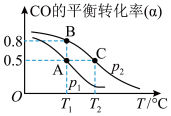
①上述合成甲醇的反应为________ 反应(填“放热”或“吸热”)。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为_____________________ 。
(1)上述3种气体直接排入空气后会引起酸雨的气体有
(2)早期人们曾经使用铅室法生产硫酸,其主要反应为:SO2(g)+NO2(g)
 SO3(g)+NO(g)
SO3(g)+NO(g)①若已知2SO2(g)+O2(g)
 2SO3(g) + Q1 2NO(g)+O2(g)
2SO3(g) + Q1 2NO(g)+O2(g)  2NO2(g) + Q2
2NO2(g) + Q2则SO2(g)+NO2(g)
 SO3(g)+NO(g)+ Q3 , Q3=
SO3(g)+NO(g)+ Q3 , Q3=②一定温度下,向固定体积为2 L的密闭容器中充入SO2和NO2各1 mol,发生反应:SO2(g)+NO2(g)
 SO3(g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是
SO3(g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是a.体系压强保持不变 b.混合气体的颜色保持不变
c.NO的物质的量保持不变 d.每生成1 mol SO3的同时消耗1 mol NO2
(3)矿石燃料的燃烧是造成酸雨的主要因素之一 。而甲醇日趋成为重要的有机燃料,通常利用CO和H2 合成甲醇,其反应的化学方程式为CO(g)+ 2H2(g)
 CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
①上述合成甲醇的反应为
②A、B、C三点的平衡常数KA、KB、KC的大小关系为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】防治环境污染,保护生态环境已成为全人类的共识。
①近年,我国不少地区雾霾天气频发,给人们的生产生活和健康造成了严重影响。导致雾霾形成的主要污染物是________ 。
空气污染指数是根据空气中SO2、________ 和可吸入颗粒物等污染物的浓度计算出来的数值。
② 燃煤产生的CO2、SO2经处理可生产多种化工产品。将CO2通入氨的氯化钠饱和溶液中可制得碳酸氢钠,该反应的化学方程式为____________________________ 。
SO2经石灰石—石膏法或氨水法处理后可分别得到副产品石膏(CaSO4·2H2O)和硫酸铵,这两种副产品中,硫元素的质量分数较高的是______________ (填化学式)。
③ 工业废水中的重金属离子的去除,通常采用加入适量碱控制废水的pH,将重金属离子转化为________ (填“盐”“氧化物”或“氢氧化物”)的形式而沉淀除去。“地沟油”流入餐桌已严重威胁到人的健康,综合利用“地沟油”的一种方法是将其发生________ (填“氧化”“水解”或“加成”)反应以获取甘油和高级脂肪酸。
①近年,我国不少地区雾霾天气频发,给人们的生产生活和健康造成了严重影响。导致雾霾形成的主要污染物是
空气污染指数是根据空气中SO2、
② 燃煤产生的CO2、SO2经处理可生产多种化工产品。将CO2通入氨的氯化钠饱和溶液中可制得碳酸氢钠,该反应的化学方程式为
SO2经石灰石—石膏法或氨水法处理后可分别得到副产品石膏(CaSO4·2H2O)和硫酸铵,这两种副产品中,硫元素的质量分数较高的是
③ 工业废水中的重金属离子的去除,通常采用加入适量碱控制废水的pH,将重金属离子转化为
您最近一年使用:0次