空气质量与我们的健康息息相关,目前我国通过监测6项污染物的百分比浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物。
(1)上述3种气体直接排入空气后会引起酸雨的气体有_______________ (填化学式)。
(2)早期人们曾经使用铅室法生产硫酸,其主要反应为:SO2(g)+NO2(g) SO3(g)+NO(g)
SO3(g)+NO(g)
①若已知2SO2(g)+O2(g) 2SO3(g) + Q1 2NO(g)+O2(g)
2SO3(g) + Q1 2NO(g)+O2(g)  2NO2(g) + Q2
2NO2(g) + Q2
则SO2(g)+NO2(g) SO3(g)+NO(g)+ Q3 , Q3=
SO3(g)+NO(g)+ Q3 , Q3=_________ kJ·mol-1。
②一定温度下,向固定体积为2 L的密闭容器中充入SO2和NO2各1 mol,发生反应:SO2(g)+NO2(g) SO3(g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是
SO3(g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是____ (选填序号)。
a.体系压强保持不变 b.混合气体的颜色保持不变
c.NO的物质的量保持不变 d.每生成1 mol SO3的同时消耗1 mol NO2
(3)矿石燃料的燃烧是造成酸雨的主要因素之一 。而甲醇日趋成为重要的有机燃料,通常利用CO和H2 合成甲醇,其反应的化学方程式为CO(g)+ 2H2(g) CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
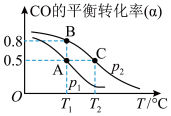
①上述合成甲醇的反应为________ 反应(填“放热”或“吸热”)。
②A、B、C三点的平衡常数KA、KB、KC的大小关系为_____________________ 。
(1)上述3种气体直接排入空气后会引起酸雨的气体有
(2)早期人们曾经使用铅室法生产硫酸,其主要反应为:SO2(g)+NO2(g)
 SO3(g)+NO(g)
SO3(g)+NO(g)①若已知2SO2(g)+O2(g)
 2SO3(g) + Q1 2NO(g)+O2(g)
2SO3(g) + Q1 2NO(g)+O2(g)  2NO2(g) + Q2
2NO2(g) + Q2则SO2(g)+NO2(g)
 SO3(g)+NO(g)+ Q3 , Q3=
SO3(g)+NO(g)+ Q3 , Q3=②一定温度下,向固定体积为2 L的密闭容器中充入SO2和NO2各1 mol,发生反应:SO2(g)+NO2(g)
 SO3(g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是
SO3(g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是a.体系压强保持不变 b.混合气体的颜色保持不变
c.NO的物质的量保持不变 d.每生成1 mol SO3的同时消耗1 mol NO2
(3)矿石燃料的燃烧是造成酸雨的主要因素之一 。而甲醇日趋成为重要的有机燃料,通常利用CO和H2 合成甲醇,其反应的化学方程式为CO(g)+ 2H2(g)
 CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
CH3OH(g)。今在一容积可变的密闭容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示:
①上述合成甲醇的反应为
②A、B、C三点的平衡常数KA、KB、KC的大小关系为
2014·上海奉贤·二模 查看更多[1]
(已下线)上海市奉贤区2014届高三4月调研测试(二模)化学试题
更新时间:2020-03-23 17:15:34
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】酸雨是指含有一定酸性的物质,pH值小于5.6的雨水,主要是由于含硫矿物燃料燃烧、含硫矿石的冶炼产生的二氧化硫以及氮氧化物等排放到大气中,然后进行了一系列的变化形成的。
(1)用化学方程式表示直接排放含SO2的烟气形成酸雨的过程:_____________ 。
(2)为消除二氧化硫的污染,通常需要对原料或烟气进行处理,某种脱硫技术的基本原理如下:
该技术的第一步反应的离子方程式为____________ 。
处理1千克含75% FeS2的黄铁矿,共消耗O2(标况)的体积为__________ L。
(3)工业生产中的尾气(主要成分为NO2和NO)可用纯碱溶液吸收,有关的化学方程式为
2NO2+Na2CO3=NaNO2+NaNO3+CO2↑ NO+NO2+Na2CO3=2NaNO2+CO2↑
NO、NO2的混合气体可用NOx表示,则混合气体被氢氧化钠完全吸收时X的取值范围为___________ 。
(4)利用氨水可用将SO2和NO2吸收,原理如下图所示:
NO2被吸收的离子方程式是_____________ 。
(1)用化学方程式表示直接排放含SO2的烟气形成酸雨的过程:
(2)为消除二氧化硫的污染,通常需要对原料或烟气进行处理,某种脱硫技术的基本原理如下:

该技术的第一步反应的离子方程式为
处理1千克含75% FeS2的黄铁矿,共消耗O2(标况)的体积为
(3)工业生产中的尾气(主要成分为NO2和NO)可用纯碱溶液吸收,有关的化学方程式为
2NO2+Na2CO3=NaNO2+NaNO3+CO2↑ NO+NO2+Na2CO3=2NaNO2+CO2↑
NO、NO2的混合气体可用NOx表示,则混合气体被氢氧化钠完全吸收时X的取值范围为
(4)利用氨水可用将SO2和NO2吸收,原理如下图所示:

NO2被吸收的离子方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】防治环境污染,保护生态环境已成为全人类的共识。
①近年,我国不少地区雾霾天气频发,给人们的生产生活和健康造成了严重影响。导致雾霾形成的主要污染物是________ 。
空气污染指数是根据空气中SO2、________ 和可吸入颗粒物等污染物的浓度计算出来的数值。
② 燃煤产生的CO2、SO2经处理可生产多种化工产品。将CO2通入氨的氯化钠饱和溶液中可制得碳酸氢钠,该反应的化学方程式为____________________________ 。
SO2经石灰石—石膏法或氨水法处理后可分别得到副产品石膏(CaSO4·2H2O)和硫酸铵,这两种副产品中,硫元素的质量分数较高的是______________ (填化学式)。
③ 工业废水中的重金属离子的去除,通常采用加入适量碱控制废水的pH,将重金属离子转化为________ (填“盐”“氧化物”或“氢氧化物”)的形式而沉淀除去。“地沟油”流入餐桌已严重威胁到人的健康,综合利用“地沟油”的一种方法是将其发生________ (填“氧化”“水解”或“加成”)反应以获取甘油和高级脂肪酸。
①近年,我国不少地区雾霾天气频发,给人们的生产生活和健康造成了严重影响。导致雾霾形成的主要污染物是
空气污染指数是根据空气中SO2、
② 燃煤产生的CO2、SO2经处理可生产多种化工产品。将CO2通入氨的氯化钠饱和溶液中可制得碳酸氢钠,该反应的化学方程式为
SO2经石灰石—石膏法或氨水法处理后可分别得到副产品石膏(CaSO4·2H2O)和硫酸铵,这两种副产品中,硫元素的质量分数较高的是
③ 工业废水中的重金属离子的去除,通常采用加入适量碱控制废水的pH,将重金属离子转化为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】NOx、SO2是主要的大气污染物,能引发雾霾、光化学烟雾及酸雨。
(1)NO2会产生硝酸型酸雨,硝酸型酸雨中主要溶质的化学式为_______________ 。
(2)目前新出厂的汽车均加装尿素[CO(NH2)2]箱,尾气中NO、NO2及尿素以物质的量之比1:1:1加热催化生成无害气体的化学方程式为_____________________________ 。
(3)氨化法同时脱硫脱硝的原理如下(已知NH4NO2在浓度较大时会分解)

①“催化氧化”的目的是________________ 。
②最终得到副产品的主要成分为____________ (填化学式)。
③相同条件下用氨水作吸收剂,NOx的脱除率与pH及 的关系如图所示。
的关系如图所示。

pH及其他条件相同时, 的比值越大,NOx的拖出率也越大,其主要原因是
的比值越大,NOx的拖出率也越大,其主要原因是_________________ 。
(1)NO2会产生硝酸型酸雨,硝酸型酸雨中主要溶质的化学式为
(2)目前新出厂的汽车均加装尿素[CO(NH2)2]箱,尾气中NO、NO2及尿素以物质的量之比1:1:1加热催化生成无害气体的化学方程式为
(3)氨化法同时脱硫脱硝的原理如下(已知NH4NO2在浓度较大时会分解)

①“催化氧化”的目的是
②最终得到副产品的主要成分为
③相同条件下用氨水作吸收剂,NOx的脱除率与pH及
 的关系如图所示。
的关系如图所示。
pH及其他条件相同时,
 的比值越大,NOx的拖出率也越大,其主要原因是
的比值越大,NOx的拖出率也越大,其主要原因是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】煤燃烧产生的SO2是引起酸雨的原因之一。
(1)每隔一定时间测定某处雨水样品的pH值:

雨水样品pH值变小的主要原因是____________________ 。
(2)反应2SO2(g)+O2(g) 2SO3(g)+Q (Q>0),其化学平衡常数表达式
2SO3(g)+Q (Q>0),其化学平衡常数表达式_______ ;升高温度,K____________ (填“变大”或者“变小”)。
(3)判断已达到化学平衡状态的描述是______ (选填编号)。
(4)防治酸雨常用的措施:向煤中加石灰,减少 SO2的产生。这种煤燃烧后,大部分硫元素最终转化为固体盐是_____________ 。
(5)把CO2气体通入澄清的石灰水,立即会产生浑浊,但把SO2气体通入澄清的石灰水,却不容易看到浑浊,而CaCO3和CaSO3都是难溶的电解质,试说明原因:_____________________ 。
(6)Na2SO3溶液呈碱性,可吸收尾气SO2。Na2SO3溶液呈碱性的原因(用离子方程式表示)_____________________ ;常温下,0.1mol/L该溶液中离子浓度由大到小排列___________ (用离子符号表示)。
(7)常温下,NaHSO3溶液呈酸性,在Na2SO3溶液中滴加稀盐酸至中性时,溶质的主要成分有__________________ 。(用化学式表示)。
(1)每隔一定时间测定某处雨水样品的pH值:

雨水样品pH值变小的主要原因是
(2)反应2SO2(g)+O2(g)
 2SO3(g)+Q (Q>0),其化学平衡常数表达式
2SO3(g)+Q (Q>0),其化学平衡常数表达式(3)判断已达到化学平衡状态的描述是
a.体系的压强不再发生变化 | b.2υ正(SO2)=υ逆(O2) |
c.c(SO2) = c(SO3) | d.气体总质量不再变化 |
(5)把CO2气体通入澄清的石灰水,立即会产生浑浊,但把SO2气体通入澄清的石灰水,却不容易看到浑浊,而CaCO3和CaSO3都是难溶的电解质,试说明原因:
(6)Na2SO3溶液呈碱性,可吸收尾气SO2。Na2SO3溶液呈碱性的原因(用离子方程式表示)
(7)常温下,NaHSO3溶液呈酸性,在Na2SO3溶液中滴加稀盐酸至中性时,溶质的主要成分有
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。催化剂常具有较强的选择性,即专一性。已知:
反应I:4NH3(g) +5O2(g) 4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
反应 II:4NH3(g)+3O2(g) 2N2(g) +6H2O(g) △H=?
2N2(g) +6H2O(g) △H=?
(1)
△H=__________________ 。
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是__________________ 。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内n(NO)/n(NH3)=1时,说明反应已达平衡
(3)氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1 mol NH3和2mol O2,测得有关物质的量关系如下图:
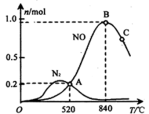
①该催化剂在高温时选择反应____________ (填“ I ”或“ II”)。
②520℃时,4NH3(g)+5O2 4NO(g) +6H2O(g)的平衡常数K=
4NO(g) +6H2O(g)的平衡常数K=___________________ (不要求得出计算结果,只需列出数字计算式)。
③有利于提高NH3转化为N2平衡转化率的措施有_______________
A.使用催化剂Pt/Ru
B.使用催化剂Cu/TiO2
C.增大NH3和O2的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
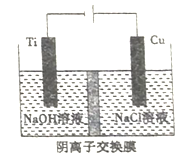
(4)纳米级Cu2O 由于具有优良的催化性能而受到关注,工业上常用电解法Cu2O,其反应为2Cu+H2O Cu2O+H2↑ 采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,则阳极上的电极反应式为
Cu2O+H2↑ 采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,则阳极上的电极反应式为___________________ ,当生成_______ 克Cu2O时,就会有NA个阴离子通过离子交换膜。
反应I:4NH3(g) +5O2(g)
 4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1反应 II:4NH3(g)+3O2(g)
 2N2(g) +6H2O(g) △H=?
2N2(g) +6H2O(g) △H=?(1)
| 化学键 | H—O | O===O | N≡N | N—H |
| 键能kJ·molˉ1 | a | b | c | d |
△H=
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内n(NO)/n(NH3)=1时,说明反应已达平衡
(3)氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1 mol NH3和2mol O2,测得有关物质的量关系如下图:

①该催化剂在高温时选择反应
②520℃时,4NH3(g)+5O2
 4NO(g) +6H2O(g)的平衡常数K=
4NO(g) +6H2O(g)的平衡常数K=③有利于提高NH3转化为N2平衡转化率的措施有
A.使用催化剂Pt/Ru
B.使用催化剂Cu/TiO2
C.增大NH3和O2的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
(4)纳米级Cu2O 由于具有优良的催化性能而受到关注,工业上常用电解法Cu2O,其反应为2Cu+H2O
 Cu2O+H2↑ 采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,则阳极上的电极反应式为
Cu2O+H2↑ 采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,则阳极上的电极反应式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】(1)已知25 ℃时有关弱酸的电离平衡常数:
① 同温度下,等pH值的a. NaHCO3、b. NaCN、c.Na2CO3溶液的物质的量浓度由大到小的顺序为__________ (填序号)。
② 25 ℃时,将20mL 0.1mol/LCH3COOH溶液和20mL0.1mol/LHSCN溶液分别与20ml0.1mol/L NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:
反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是:________ 反应结束后所得两溶液中,c(SCN-)________ c(CH3COO-)(填“> ”、“< ”或“= ”)
③ 若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是______ (填序号)。
a.c(CH3COO-) b.c(H+) c.Kwd.醋酸电离平衡常数
(2)煤燃烧产生的烟气也含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ mol-1
2NO2(g) N2O4(g) △H=-56.9kJ mol-1
N2O4(g) △H=-56.9kJ mol-1
H2O(g)=H2O(l) △H=-44.0kJ mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(l)的热化学方程式_________
(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图:请回答下列问题:
①甲烷燃料电池的负极反应式是____________
② 当A中消耗0.15mol氧气时.B 中____ 极增重_______ g。
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
① 同温度下,等pH值的a. NaHCO3、b. NaCN、c.Na2CO3溶液的物质的量浓度由大到小的顺序为
② 25 ℃时,将20mL 0.1mol/LCH3COOH溶液和20mL0.1mol/LHSCN溶液分别与20ml0.1mol/L NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:

反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是:
③ 若保持温度不变,在醋酸溶液中加入一定量氨气,下列量会变小的是
a.c(CH3COO-) b.c(H+) c.Kwd.醋酸电离平衡常数
(2)煤燃烧产生的烟气也含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867.0kJ mol-1
2NO2(g)
 N2O4(g) △H=-56.9kJ mol-1
N2O4(g) △H=-56.9kJ mol-1H2O(g)=H2O(l) △H=-44.0kJ mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(l)的热化学方程式
(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图:请回答下列问题:

①甲烷燃料电池的负极反应式是
② 当A中消耗0.15mol氧气时.B 中
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】已知下列三个反应的热化学反应方程式:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=+58 kJ/mol;②2CH3OH(g)+O2(g)=2CO2(g)+4H2(g) △H2;③2H2O(g)=2H2(g)+O2(g) △H3=+483.6kJ/mol
(1)反应②的△H2=__________ kJ/mol。
(2)已知反应① 中的相关的化学键键能数据如下表所示:
表中X=__________ 。
(3)CH3OH(g)、H2O(g)、O2(g)的混合气在绝热条件下经①②恰好完全反应,体系温度反应前后不发生变化,将生成的气体通过足量Na2O2 固体,过氧化钠增重56g,则原混合气体中CH3OH(g) 、H2O(g)、O2(g)对应的物质的量为__________ 、__________ 、__________ 。
(1)反应②的△H2=
(2)已知反应① 中的相关的化学键键能数据如下表所示:
| 化学键 | C-H | C-O | H-O | C=O | H-H |
| 键能(kJ/mol) | 413 | 343 | 465 | X | 436 |
(3)CH3OH(g)、H2O(g)、O2(g)的混合气在绝热条件下经①②恰好完全反应,体系温度反应前后不发生变化,将生成的气体通过足量Na2O2 固体,过氧化钠增重56g,则原混合气体中CH3OH(g) 、H2O(g)、O2(g)对应的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】反应速率与化学平衡均是化工生产中关注的重要问题。
(1)平衡常数K能为化学工作者提供许多信息。
实验测得下列3个反应的平衡常数K与温度T的函数关系如下:
则在该实验条件下,反应Ⅰ的活化能Ea(正) ___________ Ea(逆)(填“>”或“<”), 的数值范围是
的数值范围是___________ 。
A.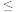 2 B.-2~0 C.0~2 D.>2
2 B.-2~0 C.0~2 D.>2
(2)工业上利用CO2氧化乙苯制苯乙烯的反应为:

①催化剂MxOy作用下,该反应可能存在如下图所示反应机理:

写出该机理表示的两个基元反应:
ⅰ:___________ 。
ⅱ:___________ 。
②常压下,乙苯和CO2在催化剂MxOy作用下反应。控制投料比[n(CO2):n(乙苯)]分别为1:1、5:1和10:1,乙苯平衡转化率与反应温度的关系如下图所示:

乙苯平衡转化率相同时,投料比越高,对应的反应温度越___________ (填“高”或“低”)。相同温度下,投料比远大于10:1时,乙苯的消耗速率明显下降,可能的原因是___________ 。
③700K时,向恒容密闭容器中加入过量CaCO3和一定量乙苯,初始和平衡时容器内压强分别为p1kPa和p2kPa,则平衡时苯乙烯的分压为___________ kPa(以含有p1、p2、p3的代数式表示)。[已知:CaCO3(s) CaO(s)+CO2(g) Kp=p3kPa]
CaO(s)+CO2(g) Kp=p3kPa]
(1)平衡常数K能为化学工作者提供许多信息。
实验测得下列3个反应的平衡常数K与温度T的函数关系如下:
| 序号 | 化学反应 | K与T的关系(c1、c2、c3为常数) |
| Ⅰ | 2O3(g) 3O2(g) △H1 3O2(g) △H1 | 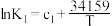 |
| Ⅱ | 4NO2(g)+O2(g) 2N2O5(g) △H2 2N2O5(g) △H2 | 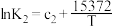 |
| Ⅲ | 2NO2(g)+O3(g) N2O5(g)+O2(g) △H3 N2O5(g)+O2(g) △H3 | 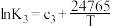 |
 的数值范围是
的数值范围是A.
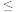 2 B.-2~0 C.0~2 D.>2
2 B.-2~0 C.0~2 D.>2(2)工业上利用CO2氧化乙苯制苯乙烯的反应为:

①催化剂MxOy作用下,该反应可能存在如下图所示反应机理:

写出该机理表示的两个基元反应:
ⅰ:
ⅱ:
②常压下,乙苯和CO2在催化剂MxOy作用下反应。控制投料比[n(CO2):n(乙苯)]分别为1:1、5:1和10:1,乙苯平衡转化率与反应温度的关系如下图所示:

乙苯平衡转化率相同时,投料比越高,对应的反应温度越
③700K时,向恒容密闭容器中加入过量CaCO3和一定量乙苯,初始和平衡时容器内压强分别为p1kPa和p2kPa,则平衡时苯乙烯的分压为
 CaO(s)+CO2(g) Kp=p3kPa]
CaO(s)+CO2(g) Kp=p3kPa]
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】肼,又名联氨,化学式为 N2H4,是一种无色油状液体,沸点 113.5℃,具有强还原性。已知:
① N2 (g) +2O2 (g) == 2NO2(g) ΔH = +68 kJ•mol-1
② N2H4(l) + 3O2 (g) == 2NO2(g) + 2H2O (l) ΔH= -622kJ•mol-1
③ H2O (g) == H2O (l) ΔH = - 44 kJ•mol-1
(1)火箭发射时可用肼作燃料,NO2 作氧化剂,生成 N2 ( g) 和 H2O (g)。写出该反应的热化学方程式:______________________________________________ 。
(2)肼具有弱碱性和强还原性,工业上利用尿素[CO(NH2)2]、NaClO 在 NaOH 溶液中发生反应生成水合肼(N2H4·H2O)、Na2CO3 等产物。上述生成水合肼的反应中尿素是_____ (填“氧化剂”或“还原剂”),反应的化学方程式为_________________ 。
(3)肼已应用于燃料电池。以 N2H4(l)为燃料和O2(g)为氧化剂,Pt 为电极催化剂,阳离子交换膜(只允许H+ 透过)为电解质。电池反应产物只有 N2(g)和H2O(l)。通入肼的一极是电池的___ 极,该极上的电极反应式为_________________ 。
(4)As2S3 和 HNO3 有如下反应:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O。若生成 2 mol H3AsO4,则反应中转移电子的物质的量为________ 。若将该反应设计成一原电池,则 NO2 应该在________ (填“正极”或“负极”)附近逸出。
① N2 (g) +2O2 (g) == 2NO2(g) ΔH = +68 kJ•mol-1
② N2H4(l) + 3O2 (g) == 2NO2(g) + 2H2O (l) ΔH= -622kJ•mol-1
③ H2O (g) == H2O (l) ΔH = - 44 kJ•mol-1
(1)火箭发射时可用肼作燃料,NO2 作氧化剂,生成 N2 ( g) 和 H2O (g)。写出该反应的热化学方程式:
(2)肼具有弱碱性和强还原性,工业上利用尿素[CO(NH2)2]、NaClO 在 NaOH 溶液中发生反应生成水合肼(N2H4·H2O)、Na2CO3 等产物。上述生成水合肼的反应中尿素是
(3)肼已应用于燃料电池。以 N2H4(l)为燃料和O2(g)为氧化剂,Pt 为电极催化剂,阳离子交换膜(只允许H+ 透过)为电解质。电池反应产物只有 N2(g)和H2O(l)。通入肼的一极是电池的
(4)As2S3 和 HNO3 有如下反应:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O。若生成 2 mol H3AsO4,则反应中转移电子的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】工业废气、汽车尾气排放出的SO2、NOx等,是形成雾霾的重要因素。霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾。
(1)NOx和SO2 在空气中存在下列平衡:2NO(g)+O2(g)
在空气中存在下列平衡:2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1,2SO2(g)+O2(g)
2NO2(g) ΔH=-113.0 kJ·mol-1,2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1。SO2通常在NO2的存在下,进一步被氧化生成SO3(g)。写出NO2和SO2反应生成NO(g)和SO3(g)的热化学方程式为
2SO3(g) ΔH=-196.6 kJ·mol-1。SO2通常在NO2的存在下,进一步被氧化生成SO3(g)。写出NO2和SO2反应生成NO(g)和SO3(g)的热化学方程式为________ 。
(2)提高2SO2(g)+O2(g) 2SO3(g)反应中SO2的转化率,是减少SO2排放的有效措施。
2SO3(g)反应中SO2的转化率,是减少SO2排放的有效措施。
①温度为T℃时,在2 L的密闭容器中加入2.0 mol 和1.0 mol O2发生反应,达到平衡时容器内气体压强变为起始时的
和1.0 mol O2发生反应,达到平衡时容器内气体压强变为起始时的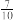 。该反应的平衡常数为
。该反应的平衡常数为_____ 。
②在①中条件下,反应达到平衡后,改变下列条件,能使SO2的转化率提高的是_____ 。
A.在其他条件不变时,减少容器的体积
B.在其他条件不变时,改用高效催化剂
C.在其他条件不变时,升高体系温度
D.1.0mol温度和容器体积不变,充入1.0 mol氦气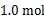
E.温度和容器体积不变,充入1.0 mol O2
(3)利用如图所示的电解装置,可将雾霾中的NO、SO2转化为硫酸铵,从而实现废气的回收再利用。通入NO的电极反应式为______ ;若通入的NO体积为4.48 L(标况下),则理论上另一电极通入SO2的物质的量应为_______ 。
(1)NOx和SO2
 在空气中存在下列平衡:2NO(g)+O2(g)
在空气中存在下列平衡:2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1,2SO2(g)+O2(g)
2NO2(g) ΔH=-113.0 kJ·mol-1,2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1。SO2通常在NO2的存在下,进一步被氧化生成SO3(g)。写出NO2和SO2反应生成NO(g)和SO3(g)的热化学方程式为
2SO3(g) ΔH=-196.6 kJ·mol-1。SO2通常在NO2的存在下,进一步被氧化生成SO3(g)。写出NO2和SO2反应生成NO(g)和SO3(g)的热化学方程式为(2)提高2SO2(g)+O2(g)
 2SO3(g)反应中SO2的转化率,是减少SO2排放的有效措施。
2SO3(g)反应中SO2的转化率,是减少SO2排放的有效措施。①温度为T℃时,在2 L的密闭容器中加入2.0 mol
 和1.0 mol O2发生反应,达到平衡时容器内气体压强变为起始时的
和1.0 mol O2发生反应,达到平衡时容器内气体压强变为起始时的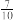 。该反应的平衡常数为
。该反应的平衡常数为②在①中条件下,反应达到平衡后,改变下列条件,能使SO2的转化率提高的是
A.在其他条件不变时,减少容器的体积
B.在其他条件不变时,改用高效催化剂
C.在其他条件不变时,升高体系温度
D.1.0mol温度和容器体积不变,充入1.0 mol氦气
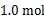
E.温度和容器体积不变,充入1.0 mol O2
(3)利用如图所示的电解装置,可将雾霾中的NO、SO2转化为硫酸铵,从而实现废气的回收再利用。通入NO的电极反应式为

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)  CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下表:
请回答下列问题:
(1)该反应的化学平衡常数表达式K=________________ 。
(2)该反应为____________ 反应(填“吸热”或“放热”)。
(3)830℃,在1L的固定容器的密闭容器中放入1 mol CO和5 mol H2O,反应达平衡后,其化学平衡常数K_________ 1.0(填“大于”、“小于”或“等于”)
(4)830℃,容器中的反应达到平衡。在其他条件不变的情况下,扩大容器的体积,平衡_______ 移动。(填“向正方向”、“向逆方向”或“不”)
(5)若1200℃时,在某时刻该容器中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为_________ (选填“正反应方向”、“逆反应方向”、“不移动”)。
 CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下表:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答下列问题:
(1)该反应的化学平衡常数表达式K=
(2)该反应为
(3)830℃,在1L的固定容器的密闭容器中放入1 mol CO和5 mol H2O,反应达平衡后,其化学平衡常数K
(4)830℃,容器中的反应达到平衡。在其他条件不变的情况下,扩大容器的体积,平衡
(5)若1200℃时,在某时刻该容器中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。回答下列问题:
(1)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表。
①写出NaClO2溶液脱硝过程中主要反应的离子方程式___ 。增加压强,NO的转化率__ (填“提高”、“不变”或“降低”)。
②由实验结果可知,脱硫反应速率___ 脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是__ 。
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压pe如图所示。
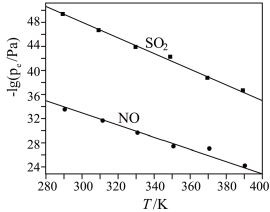
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均__ (填“增大”、“不变”或“减小”)。
②反应ClO2-+2SO32-=2SO42-+Cl-的平衡常数K表达式为___ 。
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是__ 。
(1)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1。反应一段时间后溶液中离子浓度的分析结果如下表。
| 离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
| c/(mol·L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式
②由实验结果可知,脱硫反应速率
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压pe如图所示。

①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均
②反应ClO2-+2SO32-=2SO42-+Cl-的平衡常数K表达式为
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是
您最近一年使用:0次



