向铝粉中添加少量NH4Cl固体并充分混合,将其加热到1000℃时可与N2反应制备AlN,下列说法正确的是
| A.AlN是一种金属材料 |
| B.AlN与足量氢氧化钠溶液共热时生成氢氧化铝和氨气 |
| C.少量NH4Cl能够破坏Al表面的Al2O3薄膜 |
| D.AlN与足量盐酸反应的离子方程式为AlN+3H+=Al3++NH3↑ |
更新时间:2017-10-30 11:04:28
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】短周期主族元素X、Y、Z、W在周期表中位置如图,下列表述正确的是
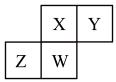

| A.Y最高正价可能为+6价 |
| B.W有可能周期数等于其族序数 |
| C.Z的最高价氧化物有可能与Y的最高价氧化物对应的水化物反应 |
| D.若X为氧元素,则离子半径顺序:r(W2-)>r(Y-)>r(X2-)>r(Z3-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】三氧化二铬(Cr2O3) 是一种深绿色的固体,熔点很高,难溶于水,其化学性质类似于Al2O3,水溶液中Cr(+3)具有还原性。下列关于Cr2O3的说法错误的是
| A.与稀硫酸反应: Cr2O3+ 3H2SO4 = Cr2(SO4)3+ 3H2O |
B.与NaOH溶液反应: Cr2O3+ 4OH- = 2 +2H2O +2H2O |
C.碱性条件下被H2O2氧化为Cr(+6): Cr2O3+ 3H2O2+ 4OH- =2 + 5H2O + 5H2O |
| D.由于金属性铝强于铬,且铬的熔点较高,故可用铝热法还原Cr2O3制取金属铬 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某同学研究铝及其化合物的性质时设计了如下两个实验方案。

方案①:2.7gAl X溶液
X溶液 Al(OH)3沉淀
Al(OH)3沉淀
方案②:2.7gAl Y溶液
Y溶液 Al(OH)3沉淀
Al(OH)3沉淀
NaOH和HCl的浓度均是3 mol/L,如图是向X溶液和Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是

方案①:2.7gAl
 X溶液
X溶液 Al(OH)3沉淀
Al(OH)3沉淀方案②:2.7gAl
 Y溶液
Y溶液 Al(OH)3沉淀
Al(OH)3沉淀NaOH和HCl的浓度均是3 mol/L,如图是向X溶液和Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是
| A.b曲线表示的是向X溶液中加入NaOH溶液 |
| B.在O点时两方案中所得溶液浓度相等 |
| C.a、b曲线表示的反应都是非氧化还原反应 |
| D.X溶液是AlCl3溶液,Y溶液显碱性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】在100mL含Cu2+、Al3+、NH4+、H+、NO3-的溶液中,逐滴加入2.5mol·L-1NaOH溶液,所加NaOH 溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是( )
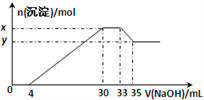

| A.x-y=2×10-3mol |
| B.原溶液中n(Cu2+)=0.025mol |
| C.原溶液的pH=2 |
| D.原溶液中c(NH4+)=7.5×10-3mol·L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】某无色溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、Cu2+、CO32—、SO42—、NO3—中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法错误的是


| A.溶液中的阳离子有H+、Mg2+、Al3+、NH4+ |
| B.cd段的离子方程式为Al(OH)3+OH—=AlO2—+2H2O |
| C.溶液中n(NH4+)=0.2mol |
| D.n(H+):n(Mg2+):n(Al3+)=1:1:1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】化学与生活密切相关,下列说法正确的是
| A.用聚乙烯塑料代替聚乳酸塑料可减少白色污染 |
| B.用于光缆通信的光导纤维和制作航天服的聚酯纤维都是新型无机非金属材料 |
| C.用高锰酸钾溶液、酒精、氯水的强氧化性进行杀菌消毒 |
| D.高纯硅广泛应用于太阳能电池和半导体材料的制造 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】科研团队通过皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管合成T-碳。T-碳的晶体结构可以看作金刚石结构中的一个碳原子被四个碳原子构成的一个正四面体结构单元替代(如图所示,所有小球都代表碳原子),T-碳的密度约为金刚石的一半。下列说法不正确的是
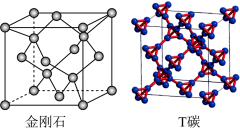

| A.T-碳与金刚石互为同素异形体 |
| B.金刚石晶体中碳原子所连接的最小环为六元环 |
| C.T-碳晶胞和金刚石晶胞的棱长之比为2:1 |
D.T-碳中 的最小夹角约为 的最小夹角约为 |
您最近一年使用:0次

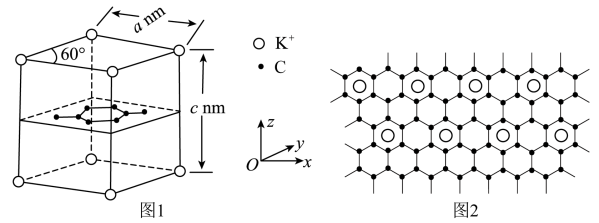
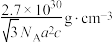 (
( 表示阿伏加德罗常数的值)
表示阿伏加德罗常数的值)

