三盐基硫酸铅(3PbO·PbSO4·H2O)简称三盐,白色或微黄色粉末,稍带甜味、有毒。200℃以上开始失去结晶水,不溶于水及有机溶剂。可用作聚氯乙烯的热稳定剂。以铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。
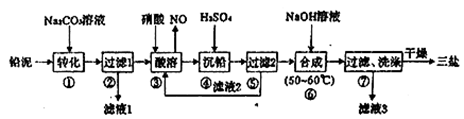
已知:常温下PbSO4的溶解度比PbCO3的溶解度大
请回答下列问题:
(1)步骤①转化的目的是____________ ,滤液1中的溶质为Na2CO3和_________ (填化学式)。
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是___________ (任写一条)。其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为__________________ 。
(3)滤液2中可循环利用的溶质为__________ (填化学式)。
(4)步骤⑥合成三盐的化学方程式为_______________________________________ (已知反应中元素价态不变)。
(5)简述步骤⑦洗涤沉淀的方法__________________________________________ 。

已知:常温下PbSO4的溶解度比PbCO3的溶解度大
请回答下列问题:
(1)步骤①转化的目的是
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是
(3)滤液2中可循环利用的溶质为
(4)步骤⑥合成三盐的化学方程式为
(5)简述步骤⑦洗涤沉淀的方法
更新时间:2017-11-03 11:53:45
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过如下实验流程制得:
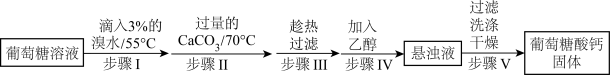
已知:a.反应原理: 。
。
b.相关物质的溶解性如下表:
c.相关物质的酸性:氢溴酸>葡萄糖酸>碳酸。
回答下列问题:
(1)步骤I中溴水氧化葡萄糖时采用了如图所示反应装置,你认为缺少的仪器是___________ ,恒压滴液漏斗使用时需要打开的活塞或玻璃塞是___________ (填“a”“b”或“a和b”)。烧杯中 溶液水浴的作用是
溶液水浴的作用是___________ 。
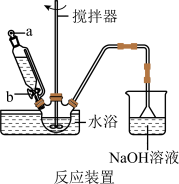
(2)制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是___________(填序号)。
(3)步骤Ⅱ中加入过量的 ,生成葡萄糖酸钙的化学方程式为
,生成葡萄糖酸钙的化学方程式为___________ 。加入过量的 除了能提高葡萄糖酸的转化率,还有的作用是
除了能提高葡萄糖酸的转化率,还有的作用是___________ 。
(4)洗涤操作中最合适的洗涤剂是___________ (填序号),理由是___________ 。
A.冷水 B.热水 C.乙醇
(5)利用重结晶法可除去葡萄糖酸钙粗品中的杂质,提高产品的质量,选出葡萄糖酸钙重结晶过程中合理的操作并排序:___________ (填序号,操作步骤不可重复使用)。
①蒸发浓缩至溶液表面出现晶膜
②待晶体充分析出后,减压过滤
③将滤液冷却至室温,加入 95%的乙醇溶液并搅拌,促进晶体析出
95%的乙醇溶液并搅拌,促进晶体析出
④趁热减压过滤,除去不溶物
⑤在50℃下用恒温干燥箱烘干,称重
⑥取烧杯加入 蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液

已知:a.反应原理:
 。
。b.相关物质的溶解性如下表:
| 物质的名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 |
| 在水中的溶解性 | 可溶于冷水,易溶于热水 | 可溶 | 极易溶 |
| 在乙醇中的溶解性 | 微溶 | 微溶 | 可溶 |
回答下列问题:
(1)步骤I中溴水氧化葡萄糖时采用了如图所示反应装置,你认为缺少的仪器是
 溶液水浴的作用是
溶液水浴的作用是
(2)制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其他试剂,下列物质中最适合的是___________(填序号)。
A.新制 悬浊液 悬浊液 | B.酸性 溶液 溶液 |
C. /葡萄糖氧化酶 /葡萄糖氧化酶 | D. 溶液 溶液 |
(3)步骤Ⅱ中加入过量的
 ,生成葡萄糖酸钙的化学方程式为
,生成葡萄糖酸钙的化学方程式为 除了能提高葡萄糖酸的转化率,还有的作用是
除了能提高葡萄糖酸的转化率,还有的作用是(4)洗涤操作中最合适的洗涤剂是
A.冷水 B.热水 C.乙醇
(5)利用重结晶法可除去葡萄糖酸钙粗品中的杂质,提高产品的质量,选出葡萄糖酸钙重结晶过程中合理的操作并排序:
①蒸发浓缩至溶液表面出现晶膜
②待晶体充分析出后,减压过滤
③将滤液冷却至室温,加入
 95%的乙醇溶液并搅拌,促进晶体析出
95%的乙醇溶液并搅拌,促进晶体析出④趁热减压过滤,除去不溶物
⑤在50℃下用恒温干燥箱烘干,称重
⑥取烧杯加入
 蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
蒸馏水,加热至微沸,加入葡萄糖酸钙粗品,得到葡萄糖酸钙饱和溶液
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】从砷盐净化渣(成分为Cu、As、Zn、ZnO、Co和SiO2)中回收有利用价值的金属,解决了长期以来影响砷盐净化工艺推广的技术难题,具有较强的实践指导意义。其工艺流程如图,请回答下列问题∶
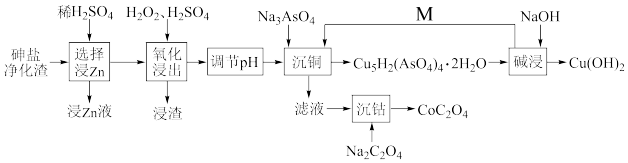
(1)在“选择浸Zn”之前,将砷盐净化渣进行球磨的目的是___ 。其他条件不变时,Zn和Co的浸出率随pH变化如图所示,则“选择浸Zn”过程中,最好控制溶液的pH=___ 。
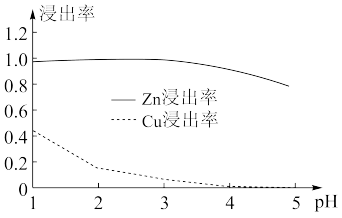
(2)“氧化浸出”时,As被氧化为H3AsO4的化学方程式为___ 。
(3)用NaOH溶液调节氧化浸出液至弱酸性,再加入Na3AsO4进行“沉铜”,得到难溶性的Cu5H2(AsO4)4·2H2O,则“沉铜”的离子方程式为___ 。
(4)“碱浸”时,除回收得到Cu(OH)2外,还得到物质M,且M在该工艺流程中可循环利用,M的化学式为___ 。
(5)为测定草酸钴产品的纯度,现称取mg样品,先用适当试剂将其转化,得到纯净的草酸铵溶液,再用过量的稀硫酸酸化,用cmol·L-1高锰酸钾标准液滴定,达到滴定终点时的现象为___ 。共用去VmL高锰酸钾标准液,则该草酸钴产品的纯度为___ 。

(1)在“选择浸Zn”之前,将砷盐净化渣进行球磨的目的是

(2)“氧化浸出”时,As被氧化为H3AsO4的化学方程式为
(3)用NaOH溶液调节氧化浸出液至弱酸性,再加入Na3AsO4进行“沉铜”,得到难溶性的Cu5H2(AsO4)4·2H2O,则“沉铜”的离子方程式为
(4)“碱浸”时,除回收得到Cu(OH)2外,还得到物质M,且M在该工艺流程中可循环利用,M的化学式为
(5)为测定草酸钴产品的纯度,现称取mg样品,先用适当试剂将其转化,得到纯净的草酸铵溶液,再用过量的稀硫酸酸化,用cmol·L-1高锰酸钾标准液滴定,达到滴定终点时的现象为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】海水中有非常丰富的化学资源,从海水中可提取多种化工原料.某工厂对海水资源综合开发利用的部分工艺流程图如下.回答下列问题:

(1)化学实验中常用到与海水晒盐原理相同的操作名称是_______ ,必需的仪器有铁架台(含铁圈)、_______ 、_______ 、_______ 。
(2)精制食盐水时下列物质中,不必用到的有_______ 。
①NaOH溶液②盐酸③K2CO3溶液④BaCl2溶液⑤硫酸⑥Na2CO3溶液⑦Ba(NO3)2溶液
(3)下列说法错误的是_______
(4)步骤②中已获得Br2,步骤③中又将Br2还原为Br,其目的为_______ 。
(5)步骤③反应的离子方程式为_______ ;该步骤也可以采用纯碱吸收,反应方程式: 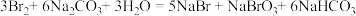 ,当转移
,当转移 个电子时,吸收Br2的物质的量为
个电子时,吸收Br2的物质的量为_______ 。
(6)若步骤⑤所得 沉淀中混有
沉淀中混有 杂质,写出除去杂质的实验步骤
杂质,写出除去杂质的实验步骤_______ 。

(1)化学实验中常用到与海水晒盐原理相同的操作名称是
(2)精制食盐水时下列物质中,不必用到的有
①NaOH溶液②盐酸③K2CO3溶液④BaCl2溶液⑤硫酸⑥Na2CO3溶液⑦Ba(NO3)2溶液
(3)下列说法错误的是
| A.海水中的镁、溴、碘元素都处于化合态 |
| B.步骤②④中通入Cl2能制得单质溴,因为Cl2的氧化性比Br2强 |
| C.步骤③中鼓入热空气分离出Br2,利用了Br2的挥发性 |
D.步骤⑤发生反应的离子方程式为: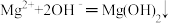 |
(5)步骤③反应的离子方程式为
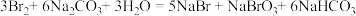 ,当转移
,当转移 个电子时,吸收Br2的物质的量为
个电子时,吸收Br2的物质的量为(6)若步骤⑤所得
 沉淀中混有
沉淀中混有 杂质,写出除去杂质的实验步骤
杂质,写出除去杂质的实验步骤
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】高铁酸钾(K2FeO4)是一种高效多功能的新型非氯绿色消毒剂。查阅资料可知:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
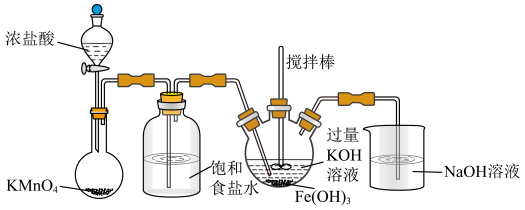
(1)A为氯气发生装置。A中反应的离子方程式是_______ (锰被还原为Mn2+)。
(2)装置B的作用为_______ 。
(3)C中得到紫色固体和溶液。C中Cl2发生的反应有:①2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6KCl+8H2O和②_______ (写离子方程式)。
(4)C中搅拌的作用是_______ 。
(5)反应结束后,过滤C中生成固体,并用KOH溶液充分洗涤,即可得到K2FeO4。使用KOH溶液而非蒸馏水洗涤的目的是_______ 。
(6)通过计算得知K2FeO4的消毒效率(以单位质量得到的电子数表示,消毒后Fe元素变为+3价)约是氯气的_______ 倍(保留两位小数)。与氯气相比较,该消毒剂的优越性_______ 。

(1)A为氯气发生装置。A中反应的离子方程式是
(2)装置B的作用为
(3)C中得到紫色固体和溶液。C中Cl2发生的反应有:①2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6KCl+8H2O和②
(4)C中搅拌的作用是
(5)反应结束后,过滤C中生成固体,并用KOH溶液充分洗涤,即可得到K2FeO4。使用KOH溶液而非蒸馏水洗涤的目的是
(6)通过计算得知K2FeO4的消毒效率(以单位质量得到的电子数表示,消毒后Fe元素变为+3价)约是氯气的
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】工业上用铬铁矿(主要成分可表示为FeO·Cr2O3,还含有Al2O3、MgCO3、SiO2等杂质)为原料制备重铬酸钾晶体(K2Cr2O7)和铁红的流程如下:
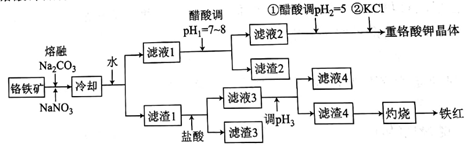
已知: I.常见离子开始生成沉淀和沉淀完全的pH如下表所示:
II. 熔融 Na2CO3条件下主要发生反应:
2FeO·Cr2O3+4Na2CO3+7NaNO3=4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
(1)熔融 Na2CO3条件下还可以得到的副产物为NaAlO2 和Na2SiO3,生成这两种副产物的化学方程式为___________________ 。
(2)滤渣2 的主要成分为________ (填化学式)。
(3)用醋酸调节pH2 =5的目的为__________ ;若调节的pH过低,NO2-可被氧化为NO3-,其离子方程式为______________ 。
(4)调节pH2后,加入KCl控制一定条件,可析出K2Cr2O7晶体的可能理由是_______ 。
(5)调节pH3的范围为______ 。
(6)检验滤液4中Fe3+是否沉淀完全的方法是____________ 。

已知: I.常见离子开始生成沉淀和沉淀完全的pH如下表所示:
| Fe3+ | Al3+ | Mg2+ | SiO32- | AlO2- | |
| 开始沉淀的pH | 1.9 | 4.2 | 8.1 | 9.5 | 10.2 |
| 沉淀完全的pH | 3.2 | 5.3 | 9.4 | 8.0 | 8.5 |
II. 熔融 Na2CO3条件下主要发生反应:
2FeO·Cr2O3+4Na2CO3+7NaNO3=4Na2CrO4+Fe2O3+4CO2↑+7NaNO2。
(1)熔融 Na2CO3条件下还可以得到的副产物为NaAlO2 和Na2SiO3,生成这两种副产物的化学方程式为
(2)滤渣2 的主要成分为
(3)用醋酸调节pH2 =5的目的为
(4)调节pH2后,加入KCl控制一定条件,可析出K2Cr2O7晶体的可能理由是
(5)调节pH3的范围为
(6)检验滤液4中Fe3+是否沉淀完全的方法是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高氯酸铜易溶于水,在130℃时会发生分解反应,是一种燃烧催化剂。以食盐等为原料制备高氯酸铜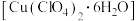 的一种工艺流程如图1所示:
的一种工艺流程如图1所示:

(1)发生“电解Ⅰ”时,所用的交换膜是_______ (填“阳”或“阴”)离子交换膜。
(2)歧化反应是同一种物质中同种元素自身的氧化还原反应,已知上述工艺流程中“歧化反应”的产物之一为 。
。
①“歧化反应”的化学方程式为_______ 。
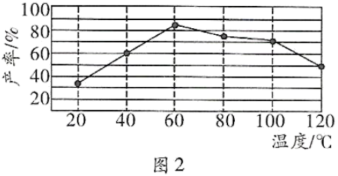
②“歧化反应”阶段所采用的不同温度对产率的影响结果如图2所示。则该反应最适宜的温度是____ 。
(3)操作a的名称是_______ ,该流程中可循环利用的物质是_______ (填化学式)。
(4)用该工艺流程制备高氯酸铜时,若起始时 的质量为
的质量为 t,最终制得的
t,最终制得的 为
为 t,则产率为
t,则产率为_______ (用含a、b的代数式表示)。
(5)某温度下,高氯酸铜按A、B两种方式同时分解,分解过程中铜的化合价不发生改变。A方式为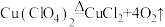 ,若4
,若4 高氯酸铜在该温度下按A、B各占50%的方式完全分解,且A、B两种方式转移的电子数之比为
高氯酸铜在该温度下按A、B各占50%的方式完全分解,且A、B两种方式转移的电子数之比为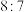 ,则B方式为
,则B方式为_______ (用化学方程式表示)。
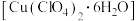 的一种工艺流程如图1所示:
的一种工艺流程如图1所示:
(1)发生“电解Ⅰ”时,所用的交换膜是
(2)歧化反应是同一种物质中同种元素自身的氧化还原反应,已知上述工艺流程中“歧化反应”的产物之一为
 。
。①“歧化反应”的化学方程式为
②“歧化反应”阶段所采用的不同温度对产率的影响结果如图2所示。则该反应最适宜的温度是

(3)操作a的名称是
(4)用该工艺流程制备高氯酸铜时,若起始时
 的质量为
的质量为 t,最终制得的
t,最终制得的 为
为 t,则产率为
t,则产率为(5)某温度下,高氯酸铜按A、B两种方式同时分解,分解过程中铜的化合价不发生改变。A方式为
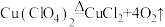 ,若4
,若4 高氯酸铜在该温度下按A、B各占50%的方式完全分解,且A、B两种方式转移的电子数之比为
高氯酸铜在该温度下按A、B各占50%的方式完全分解,且A、B两种方式转移的电子数之比为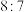 ,则B方式为
,则B方式为
您最近半年使用:0次



