(1)47.5g某二价金属的氯化物中含有1molCl-,则该金属氯化物的摩尔质量为_______ ;该金属的相对原子质量为_______ 。
(2)标准状况下,3.4g NH3 的体积为_______ ;它与标准状况下_______ L H2S含有相同数目的氢原子。
(3)已知CO、CO2混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量为_______ ;CO2在相同状况下的体积为_______ 。
(4)将4g NaOH 溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的物质 的量浓度为_______ 。
(5)已知ag氢气中含有b个氢原子,则阿伏伽德罗常数的值可表示为_______ 。
(2)标准状况下,3.4g NH3 的体积为
(3)已知CO、CO2混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量为
(4)将4g NaOH 溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的物质 的量浓度为
(5)已知ag氢气中含有b个氢原子,则阿伏伽德罗常数的值可表示为
17-18高一上·河南南阳·阶段练习 查看更多[5]
内蒙古自治区赤峰市赤峰二中2019-2020学年高一10月月考化学试题西藏拉萨中学2019-2020学年高一上学期期中考试化学试卷吉林蛟河一中2019-2020学年高一上学期第一次月考化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》 第一单元 从实验学化学单元测试 B卷河南省镇平县第一高级中学2017-2018学年高一10月月考化学试题
更新时间:2017-11-09 10:29:41
|
相似题推荐
【推荐1】二氧化氯( )是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:
)是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:
(1)将二氧化氯通入品红溶液中,溶液褪色的原因是_______ 。
(2)配平下列反应的化学方程式:_______ 。
_______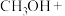 _______
_______ _______= CO2↑_______
_______= CO2↑_______ _______
_______ _______
_______
(3)上述反应中,被氧化的元素是_______ 。还原产物与氧化产物的物质的量之比是_______ 。
(4)根据上述反应可推知_______ (填字母)。
a.氧化性: b.氧化性:
b.氧化性: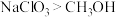
c.还原性: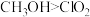 d.还原性:
d.还原性:
(5)若转移的电子数目为 (
( 为阿伏加德罗常数的值)则反应产生气体的体积约为
为阿伏加德罗常数的值)则反应产生气体的体积约为_______ L(标准状况)。
 )是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:
)是一种黄绿色到橙黄色的气体。工业上制备二氧化氯的方法之一是用甲醇在酸性介质中与氯酸钠反应。二氧化氯能与许多化学物质发生爆炸性反应,遇水则生成次氯酸、氯气和氧气。回答下列问题:(1)将二氧化氯通入品红溶液中,溶液褪色的原因是
(2)配平下列反应的化学方程式:
_______
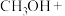 _______
_______ _______= CO2↑_______
_______= CO2↑_______ _______
_______ _______
_______(3)上述反应中,被氧化的元素是
(4)根据上述反应可推知
a.氧化性:
 b.氧化性:
b.氧化性: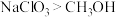
c.还原性:
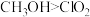 d.还原性:
d.还原性:
(5)若转移的电子数目为
 (
( 为阿伏加德罗常数的值)则反应产生气体的体积约为
为阿伏加德罗常数的值)则反应产生气体的体积约为
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】现有短周期元素X形成的单质A与NaOH溶液反应,有如下转化关系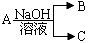 ,(若产物中有水生成则省略未表示出来)。
,(若产物中有水生成则省略未表示出来)。
(1)若常温常压下,A为气态,且B、C中均有X元素,则A与NaOH溶液反应的离子方程式为__ ;
(2)若常温常压下,A为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为__ ;
(3)若A为金属,C为气体,则A 与NaOH溶液反应的离子方程式为_____
(4)由(2)和(3)中两种单质形成合金在工业、建筑业中有重要的用途。一个探究性学习小组,他们拟
用该合金与足量稀硫酸的反应测定通常状况下气体摩尔体积,实验装置如下:

①装置中导管a的作用是平衡分液漏斗上下管口的压强,有利于液体滴下和____ ;
②实验中准确测得4个数据:实验前该合金的质量m1g,实验后残留固体的质量m2g,实验前后碱式滴定管中液面读数分别为V1mL、V2mL;则通常状况时气体摩尔体积Vm=_____ L·moL-1。
 ,(若产物中有水生成则省略未表示出来)。
,(若产物中有水生成则省略未表示出来)。(1)若常温常压下,A为气态,且B、C中均有X元素,则A与NaOH溶液反应的离子方程式为
(2)若常温常压下,A为非金属固态单质,且其在电子工业中有着重要的用途,则工业制取A化学方程式为
(3)若A为金属,C为气体,则A 与NaOH溶液反应的离子方程式为
(4)由(2)和(3)中两种单质形成合金在工业、建筑业中有重要的用途。一个探究性学习小组,他们拟
用该合金与足量稀硫酸的反应测定通常状况下气体摩尔体积,实验装置如下:

①装置中导管a的作用是平衡分液漏斗上下管口的压强,有利于液体滴下和
②实验中准确测得4个数据:实验前该合金的质量m1g,实验后残留固体的质量m2g,实验前后碱式滴定管中液面读数分别为V1mL、V2mL;则通常状况时气体摩尔体积Vm=
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】某学生试图用电解法根据电极上析出物质的质量来验证阿伏加德罗常数值,其实验方案的要点为:
①用直流电电解氯化铜溶液,所用仪器如下图。
②强度为I A,通电时间为t s后,精确测得某电极上析出的铜的质量为m g。

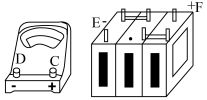
试回答:
(1)这些仪器的正确连接顺序为(用图中标注仪器接线柱的英文字母表示,下同):E接___________ ,C接___________ ,___________ 接F。实验线路中的电流方向为___________→___________→___________→C→___________→___________;___________
(2)写出B电极上发生反应的离子方程式___________ ,G试管中淀粉KI溶液变化的现象为___________ ,相应的离子方程式是___________ ;
(3)为精确测定电极上析出铜的质量,所必需的实验步骤的先后顺序是___________ ;
①称量电解前电极质量 ②刮下电解后电极上的铜并清洗 ③用蒸馏水清洗电解后电极 ④低温烘干电极后称量 ⑤低温烘干刮下的铜后称量 ⑥再次低温烘干后称量至恒重
(4)已知电子的电量为1.6×10-19 C。试列出阿伏加德罗常数的计算表达式:NA=___________ 。
①用直流电电解氯化铜溶液,所用仪器如下图。
②强度为I A,通电时间为t s后,精确测得某电极上析出的铜的质量为m g。


试回答:
(1)这些仪器的正确连接顺序为(用图中标注仪器接线柱的英文字母表示,下同):E接
(2)写出B电极上发生反应的离子方程式
(3)为精确测定电极上析出铜的质量,所必需的实验步骤的先后顺序是
①称量电解前电极质量 ②刮下电解后电极上的铜并清洗 ③用蒸馏水清洗电解后电极 ④低温烘干电极后称量 ⑤低温烘干刮下的铜后称量 ⑥再次低温烘干后称量至恒重
(4)已知电子的电量为1.6×10-19 C。试列出阿伏加德罗常数的计算表达式:NA=
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】将一定质量的镁铝合金投入到200 mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加 5 mol • L-1的NaOH溶液至过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。求:

(1)原合金中Mg的质量________ g;Al的质量________ g
(2)盐酸的物质的量浓度______ mol/L。

(1)原合金中Mg的质量
(2)盐酸的物质的量浓度
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】完成下列问题。
(1)某化学研究性学习小组用NH4Cl、KCl、(NH4)2SO4配制含有 、Cl-、K+、
、Cl-、K+、 的溶液,且要求该溶液中,c(Cl-)=c(K+)=c(
的溶液,且要求该溶液中,c(Cl-)=c(K+)=c( )=0.4mol/L,则
)=0.4mol/L,则 的物质的量浓度为
的物质的量浓度为___________ 。
(2)向含有2molHNO3和0.6molH2SO4的混合稀溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。

①a表示的是___________ 的变化曲线。
②n1=___________ ,n3=___________ 。
③向P点溶液中加入铜粉,最多可溶解铜粉的质量是___________ g。
(1)某化学研究性学习小组用NH4Cl、KCl、(NH4)2SO4配制含有
 、Cl-、K+、
、Cl-、K+、 的溶液,且要求该溶液中,c(Cl-)=c(K+)=c(
的溶液,且要求该溶液中,c(Cl-)=c(K+)=c( )=0.4mol/L,则
)=0.4mol/L,则 的物质的量浓度为
的物质的量浓度为(2)向含有2molHNO3和0.6molH2SO4的混合稀溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。

①a表示的是
②n1=
③向P点溶液中加入铜粉,最多可溶解铜粉的质量是
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】按要求回答问题。
(1)将19.4gCO2和水蒸气的混合气体,与足量的Na2O2反应,收集到标准状况下5.6L的气体,试确定混合气体的平均相对分子质量为_______ ,CO2与水蒸气的物质的量之比为_______ 。
(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入4.032L(标准状况下的)O2,在高温下充分反应后测得气体的密度为1.34g·L-1(已折算成标准状况,AlN不跟O2反应),则所得气体的摩尔质量为_______ g·mol-1,该气体的成分是_______ (写化学式),该样品中含杂质碳_______ g。
(1)将19.4gCO2和水蒸气的混合气体,与足量的Na2O2反应,收集到标准状况下5.6L的气体,试确定混合气体的平均相对分子质量为
(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入4.032L(标准状况下的)O2,在高温下充分反应后测得气体的密度为1.34g·L-1(已折算成标准状况,AlN不跟O2反应),则所得气体的摩尔质量为
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】(1)标准状况下:22g CO2的体积是______ .
(2)0.01 mol某气体的质量是0.28g,该气体的摩尔质量是________ ;
(3)相同条件下,CH4与O2的质量比是1:8时二者的体积比是______ 。
(4)2gNaOH溶于水配制成______ mL溶液时其物质的量浓度为2mol/L。
(2)0.01 mol某气体的质量是0.28g,该气体的摩尔质量是
(3)相同条件下,CH4与O2的质量比是1:8时二者的体积比是
(4)2gNaOH溶于水配制成
您最近半年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)1LAl2(SO4)3和MgSO4的混合溶液中,含Mg2+2.4g,SO 的物质的量浓度为1mol·L-1,则Al3+的物质的量浓度是
的物质的量浓度为1mol·L-1,则Al3+的物质的量浓度是___ ,将该混合液加水稀释至体积为100L,稀释后溶液中MgSO4的物质的量浓度为___ mol·L-1。
(2)若一氧化碳和二氧化碳的混合气体的密度与同温同压下氧气的密度相同,混合气体中二氧化碳所占的质量分数为( )
A.75.0% B.25.0% C.65.625% D.34.375%
 的物质的量浓度为1mol·L-1,则Al3+的物质的量浓度是
的物质的量浓度为1mol·L-1,则Al3+的物质的量浓度是(2)若一氧化碳和二氧化碳的混合气体的密度与同温同压下氧气的密度相同,混合气体中二氧化碳所占的质量分数为
A.75.0% B.25.0% C.65.625% D.34.375%
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】现有下列物质:①铜丝②FeCl3溶液③氯化氢气体④NaHSO4固体⑤干冰⑥ 胶体⑦硫酸亚铁铵晶体
胶体⑦硫酸亚铁铵晶体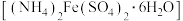 ⑧稀氨水
⑧稀氨水
(1)上述物质中属于电解质的是___________ (填序号,下同),能够导电的是___________ 。写出属于酸式盐的物质溶于水的电离方程式___________ 。
(2)②与⑧在溶液中反应的离子方程式为___________ 。
(3)硫酸亚铁铵晶体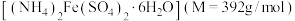 俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制
俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制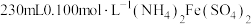 溶液,回答问题:
溶液,回答问题:
①配制溶液过程中需要的玻璃仪器除量筒、烧杯、玻璃棒外,还需___________ 。
②用电子天平(精确度为0.01g)称量硫酸亚铁铵晶体___________ g。
③下列操作将导致所配制的溶液浓度偏高的是___________ (填选项)。
A.摩尔盐放置过程中失去了部分结晶水
B.配制过程中没有洗涤烧杯和玻璃棒
C.定容时俯视刻度线
D.定容后振荡容量瓶发现液面低于刻度线,继续加蒸馏水定容
(4)将VL标准状况下的物质③溶于100mL水中(水的密度近似为1g·mL-1),得到密度为ρg·mL-1的溶液,该溶液的物质的量浓度是___________ mol·L-1(列出计算式)。
 胶体⑦硫酸亚铁铵晶体
胶体⑦硫酸亚铁铵晶体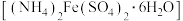 ⑧稀氨水
⑧稀氨水(1)上述物质中属于电解质的是
(2)②与⑧在溶液中反应的离子方程式为
(3)硫酸亚铁铵晶体
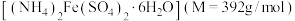 俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制
俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制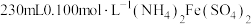 溶液,回答问题:
溶液,回答问题:①配制溶液过程中需要的玻璃仪器除量筒、烧杯、玻璃棒外,还需
②用电子天平(精确度为0.01g)称量硫酸亚铁铵晶体
③下列操作将导致所配制的溶液浓度偏高的是
A.摩尔盐放置过程中失去了部分结晶水
B.配制过程中没有洗涤烧杯和玻璃棒
C.定容时俯视刻度线
D.定容后振荡容量瓶发现液面低于刻度线,继续加蒸馏水定容
(4)将VL标准状况下的物质③溶于100mL水中(水的密度近似为1g·mL-1),得到密度为ρg·mL-1的溶液,该溶液的物质的量浓度是
您最近半年使用:0次



