下列说法正确的是
| A.活化分子间的碰撞一定能发生化学反应 |
| B.升高温度时,化学反应速率加快,主要原因是反应物分子的能量增加,活化分子百分数增大,单位时间内有效碰撞次数增多 |
| C.自发进行的反应一定迅速 |
| D.凡是熵增加的过程都是自发过程 |
更新时间:2017-11-14 22:18:23
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】恒容密闭容器中进行反应FeO(s)+CO(g) Fe(s)+CO2(g)
Fe(s)+CO2(g)  H<0。下列说法正确的是
H<0。下列说法正确的是
 Fe(s)+CO2(g)
Fe(s)+CO2(g)  H<0。下列说法正确的是
H<0。下列说法正确的是| A.当混合气体的密度不再变化时,反应达到平衡状态 |
| B.增大CO浓度,因为增大了活化分子百分数,导致反应速率增大 |
| C.该反应在高温下为自发反应 |
| D.平衡时,向容器中加入FeO可促使平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关碰撞理论的说法正确的是
| A.反应物的活化分子的数目越多,反应速率越快 |
| B.反应物的分子的每次碰撞都能发生化学反应 |
| C.活化分子的平均能量就是活化能 |
| D.能发生有效碰撞的分子一定是活化分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
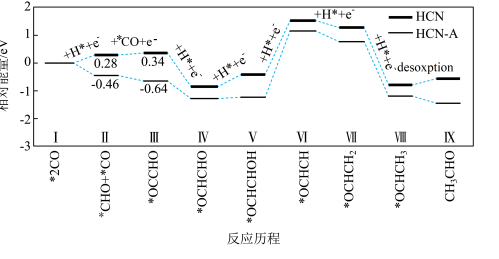
【推荐1】我国学者通过局域晶态氮化碳调控*OCCHO中间体路径实现光催化选择性还原CO制取CH3CHO,在不同催化剂(HCN、HCN-A)作用下其反应历程中能量变化如图所示(部分物质省略),其中HCN-A表现出优异的催化性能。
下列说法错误的是

下列说法错误的是
| A.步骤Ⅲ→Ⅳ过程中存在C-H的形成 |
| B.*CO转化为CH3CHO的反应为放热反应 |
| C.决定*CO→CH3CHO反应速率的步骤是Ⅵ→Ⅶ |
| D.HCN-A优于HCN的重要原因之一是*CHO和*CO生成*OCCHO的△H<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】反应 分两步进行:①
分两步进行:①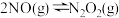 (快),②
(快),②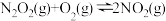 (慢)。恒容条件下,按物质的量之比为2∶1加入
(慢)。恒容条件下,按物质的量之比为2∶1加入 和
和 ,测得起始
,测得起始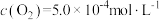 。在相同时间内,测得不同温度下
。在相同时间内,测得不同温度下 转化为
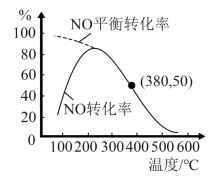
转化为 的转化率如图所示,下列说法错误的是
的转化率如图所示,下列说法错误的是
 分两步进行:①
分两步进行:①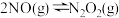 (快),②
(快),②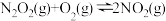 (慢)。恒容条件下,按物质的量之比为2∶1加入
(慢)。恒容条件下,按物质的量之比为2∶1加入 和
和 ,测得起始
,测得起始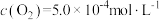 。在相同时间内,测得不同温度下
。在相同时间内,测得不同温度下 转化为
转化为 的转化率如图所示,下列说法错误的是
的转化率如图所示,下列说法错误的是
| A.反应的活化能:①<② |
B. 时, 时,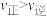 |
| C.两步反应均为吸热反应 |
D. 时,反应达到平衡时 时,反应达到平衡时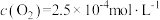 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A.反应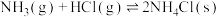 在低温下能自发进行,则该反应的 在低温下能自发进行,则该反应的 |
B.对于反应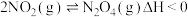 ,恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的 ,恒温时,缩小容积,气体颜色变深,是平衡正向移动导致的 |
C.反应 ,在恒温恒压下,加入催化剂,平衡常数增大 ,在恒温恒压下,加入催化剂,平衡常数增大 |
| D.升高温度或加入催化剂能使单位体积内活化分子的百分数增大,但原因不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确的是
A. 、 、 的反应在任何温度下都能自发进行 的反应在任何温度下都能自发进行 |
B.反应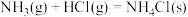 在室温下可自发进行,则该反应的 在室温下可自发进行,则该反应的 |
| C.活化分子间的碰撞都能使化学反应发生,单位体积内碰撞越多,反应速率越高 |
| D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的速率 |
您最近一年使用:0次


 CH3OH(g)+H2O(g)的历程如图所示。下列说法正确的是
CH3OH(g)+H2O(g)的历程如图所示。下列说法正确的是
 CO(g)+H2(g)
CO(g)+H2(g)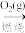 CO2(g)+H2O(g);途径b:C(s)
CO2(g)+H2O(g);途径b:C(s)

