次氯酸钠(NaClO)是漂白液的主要成分,次氯酸钠溶液可用于消毒、杀菌及水处理。一种生产次氯酸钠的工艺如图所示。
-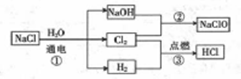
(1)Cl 元素位于元素周期表第______ 周期___ 族。
(2)写出NaOH的电子式:__________ 。
(3)写出反应②的化学方程式:_______________ 。该反应中每生成1mol NaClO时,转移______ mol 电子。
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是_____________________ (用离子方程式表示)。
-

(1)Cl 元素位于元素周期表第
(2)写出NaOH的电子式:
(3)写出反应②的化学方程式:
(4)“84”消毒液( 主要成分为NaClO)和洁厕灵( 主要成分为浓盐酸)不能混在一起使用,原因是
更新时间:2017-11-21 22:32:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出氮元素的原子结构示意图:_______ 。
(2)通常情况下,氮气性质不活泼,其原因是__________。
(3)N2的电子式:_______ ,将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现人工固氮的是_______ 。
A.N2和H2在一定条件下反应生成NH3 B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO D.NH3和HNO3反应生成NH4NO3
(4)氨气的电子式:_______ 。
(5)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出此反应的化学方程式_____ 。
(1)写出氮元素的原子结构示意图:
(2)通常情况下,氮气性质不活泼,其原因是__________。
| A.氮分子是双原子分子 | B.氮元素的非金属性很强 |
| C.氮原子的半径较小 | D.破坏氮分子中的化学键很难 |
A.N2和H2在一定条件下反应生成NH3 B.雷雨闪电时空气中的N2和O2化合生成NO
C.NH3经过催化氧化生成NO D.NH3和HNO3反应生成NH4NO3
(4)氨气的电子式:
(5)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。写出此反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】高纯硅具有良好的硬度和耐磨性以及良好的光、电性能,广泛用于芯片、集成电路、光伏电池板等领域。工业上制备高纯硅反应的化学方程式: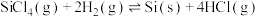
(1)此反应方程式中,呈正四面体型分子的电子式是___________ 。
(2)HCl的稳定性___________ (填“大于”“小于”)HF,说明理由___________ 。
(3)根据下表判断,此反应的 为___________
为___________
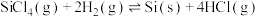
(1)此反应方程式中,呈正四面体型分子的电子式是
(2)HCl的稳定性
(3)根据下表判断,此反应的
 为___________
为___________| 化学键 |  |  |  |  |  |  |
| 键能(kJ/mol) | 460 | 360 | 436 | 431 | 176 | 347 |
| A.+412 kJ/mol | B.+236 kJ/mol | C.-116 kJ/mol | D.-236 kJ/mol |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.肼(N2H4)是一种重要的化工产品,有广泛用途,可用作火焰燃料。回答下列问题:
(1)N2H4的电子式为______ 。
(2)已知N2H4(g)+O2(g)=N2(g)+2H2O(g)的能量变化如图所示:
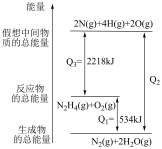
①则该反应为______ (填“吸热反应”或“放热反应”)。
②2molN原子、4molH原子、2molO原子生成1molN2(g)和2molH2O(g)的过程中放出_____ kJ能量。
Ⅱ.“绿色办奥”是北京冬奥会四大办奥理念之首,在“双碳”目标驱动下,全球首次服务体育赛事的大批量氢燃料客车在北京冬奥会上闪亮登场。工作原理如图所示:
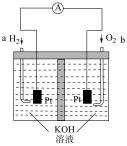
(3)氢燃料电池工作时H2从______ (填“正极”或“负极”)通入。
(4)负极发生的反应方程式为______ ,原电池总反应方程式为______ 。
(5)溶液中OH-向______ 电极(填“a”或“b”)移动。
(6)当有16g气体被还原时,回路中转移的电子数为______ 。
(1)N2H4的电子式为
(2)已知N2H4(g)+O2(g)=N2(g)+2H2O(g)的能量变化如图所示:

①则该反应为
②2molN原子、4molH原子、2molO原子生成1molN2(g)和2molH2O(g)的过程中放出
Ⅱ.“绿色办奥”是北京冬奥会四大办奥理念之首,在“双碳”目标驱动下,全球首次服务体育赛事的大批量氢燃料客车在北京冬奥会上闪亮登场。工作原理如图所示:

(3)氢燃料电池工作时H2从
(4)负极发生的反应方程式为
(5)溶液中OH-向
(6)当有16g气体被还原时,回路中转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】NaCl是一种化工原料,可以制备多种物质,如图所示:
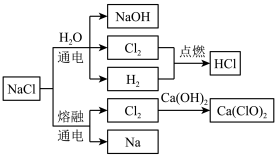
请根据以上转化关系填写下列空白。
(1)实验室用浓盐酸和MnO2制取氯气,其反应的化学方程式为___________ 。该反应中盐酸表现的性质有___________ 。
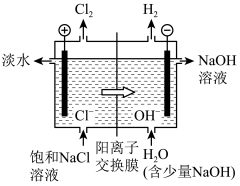
(2)饱NaCl溶液通电后发生反应的离子方程式为___________ 。电解饱和NaCl溶液的装置如图所示,在装置中间添加阳离子交换膜(只允许阳离子通过,不允许气体和阴离子通过),其作用是___________ 。
(3)将氯气溶于水配成饱和溶液,用胶头滴管将饱和氯水慢慢滴入含有酚酞的氢氧化钠稀溶液中,当滴到一定量时,红色突然褪去。产生上述现象的原因可能有两种:①氢氧化钠完全反应,反应后溶液碱性减弱,酚酞变无色;②过量饱和氯水中的次氯酸利用漂白性使溶液红色褪去。设计实验证明红色褪去的原因是①或②,简述实验方案和结论:___________ 。

请根据以上转化关系填写下列空白。
(1)实验室用浓盐酸和MnO2制取氯气,其反应的化学方程式为
(2)饱NaCl溶液通电后发生反应的离子方程式为

(3)将氯气溶于水配成饱和溶液,用胶头滴管将饱和氯水慢慢滴入含有酚酞的氢氧化钠稀溶液中,当滴到一定量时,红色突然褪去。产生上述现象的原因可能有两种:①氢氧化钠完全反应,反应后溶液碱性减弱,酚酞变无色;②过量饱和氯水中的次氯酸利用漂白性使溶液红色褪去。设计实验证明红色褪去的原因是①或②,简述实验方案和结论:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】除去下列物质中混有的少量杂质,用有关反应的离子方程式表示:
(1)Fe2O3中混有Al2O3:___________________________________
(2)Na2CO3溶液中混有NaHCO3:__________________________
(3)FeCl2溶液中混有FeCl3:______________________________
(4)“84”消毒液是生活中常用的含氯消毒剂,其制备过程的主要反应是将氯气通入氢氧化钠溶液中,反应的化学方程式为________________________________________
(1)Fe2O3中混有Al2O3:
(2)Na2CO3溶液中混有NaHCO3:
(3)FeCl2溶液中混有FeCl3:
(4)“84”消毒液是生活中常用的含氯消毒剂,其制备过程的主要反应是将氯气通入氢氧化钠溶液中,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
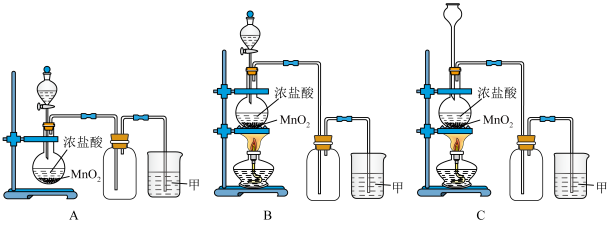
(1)A、B、C三套装置中,应选用的装置是___________ (选填“A”、“B”、“C”)。
(2)写出制取氯气的化学方程式___________ 。
(3)为了防止氯气污染环境,图中溶液甲中发生的化学反应方程式___________ 。
(4)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的原理是___________ (用化学方程式说明)
(5)实验室也可用 固体和浓盐酸反应制取氯气,反应方程式:
固体和浓盐酸反应制取氯气,反应方程式: 。请用双线桥标出电子转移的方向和数目:
。请用双线桥标出电子转移的方向和数目:___________ 。若反应中有5mol电子转移,被氧化HCl的的物质的量为___________ 。

(1)A、B、C三套装置中,应选用的装置是
(2)写出制取氯气的化学方程式
(3)为了防止氯气污染环境,图中溶液甲中发生的化学反应方程式
(4)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,在空气中漂白粉长期存放会变质而失效的原理是
(5)实验室也可用
 固体和浓盐酸反应制取氯气,反应方程式:
固体和浓盐酸反应制取氯气,反应方程式: 。请用双线桥标出电子转移的方向和数目:
。请用双线桥标出电子转移的方向和数目:
您最近一年使用:0次



