请回答下列问题。
(1)碳酸氢钠俗称小苏打,其水溶液显____________ 性(填“酸”、“碱”或“中”) ;
(2)等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者____________ 后者(填“>”、“<”或“=”) ;
(3)除去碳酸钠固体中碳酸氢钠的方法是____________ (填“加热”或“溶解过滤”) ;
(4)若金属钠长时间在潮湿的空气中放置,最后生成的物质是_________ ;
(5)将一小块金属钠投入水中,发生反应的离子方程式为_________________________ ;
(6)铝是一种比较活泼的金属,在空气中极易被氧化而生成一种致密的氧化膜,从而保护内部的铝不再被氧化。请写出此反应的化学方程式________________ 。
(1)碳酸氢钠俗称小苏打,其水溶液显
(2)等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者
(3)除去碳酸钠固体中碳酸氢钠的方法是
(4)若金属钠长时间在潮湿的空气中放置,最后生成的物质是
(5)将一小块金属钠投入水中,发生反应的离子方程式为
(6)铝是一种比较活泼的金属,在空气中极易被氧化而生成一种致密的氧化膜,从而保护内部的铝不再被氧化。请写出此反应的化学方程式
17-18高一上·江西九江·阶段练习 查看更多[2]
更新时间:2017-12-23 07:41:30
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E五种物质的焰色反应都显黄色,A、B与水反应都有气体放出,A与水的反应放出的气体只具有氧化性,同时都生成溶液C,C与少量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能变成D。
(1)写出下列物质的化学式:A____________ 、C____________ 、E_____________ 。
(2)B与水反应的离子方程式是:______________________________________________ 。
(3)D溶液中通入CO2的离子方程式:__________________________________________ 。
(4)7.8g的A加入到足量的硫酸铜溶液中,标况下,产生气体的体积为________ L, 生成沉淀的质量为________ g。
(1)写出下列物质的化学式:A
(2)B与水反应的离子方程式是:
(3)D溶液中通入CO2的离子方程式:
(4)7.8g的A加入到足量的硫酸铜溶液中,标况下,产生气体的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)写出钠在氧气中燃烧的化学方程式,并用单线桥法分析其电子转移情况_______ ,其中被还原的物质是_______ ;
(2)写出钠在水中反应的化学方程式,并用双线桥法分析其电子转移情况_______ ,其中水作_______ 剂(填氧化或还原)
(2)写出钠在水中反应的化学方程式,并用双线桥法分析其电子转移情况
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】钠和钠的化合物有许多重要的用途,碳酸钠可与氯气发生反应,涉及的反应如下: 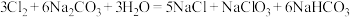
(1)用单线桥法标出电子转移的方向和数目_____________________ 。
(2)该反应中氧化剂与还原剂的个数之比是_____________ ,若  被氧化时,转移的电子是
被氧化时,转移的电子是_____________  。
。
(3)少量的钠应保存在_________ 中;钠着火时应采取的灭火措施是_____________ ,不能用水灭火,原因是_____________________ (涉及反应的离子方程式)。
(4)在实验室配制好的 溶液中通入过量的二氧化碳时发生的离子反应方程式是
溶液中通入过量的二氧化碳时发生的离子反应方程式是_________________________ 。
(5)实验室制备少量氯气的化学反应方程式是_____________________ 。
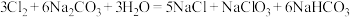
(1)用单线桥法标出电子转移的方向和数目
(2)该反应中氧化剂与还原剂的个数之比是
 被氧化时,转移的电子是
被氧化时,转移的电子是 。
。(3)少量的钠应保存在
(4)在实验室配制好的
 溶液中通入过量的二氧化碳时发生的离子反应方程式是
溶液中通入过量的二氧化碳时发生的离子反应方程式是(5)实验室制备少量氯气的化学反应方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】写出下列反应的离子方程式,是氧化还原反应的,用双线桥标出电子转移的方向和数目。
(1)镁与稀硫酸反应:___________ 。
(2)钠与水的反应:___________ 。
(3)向碳酸钠溶液中滴加少量盐酸:___________ 。
(4)Ba(OH)2溶液与H2SO4溶液混合:___________ 。
(1)镁与稀硫酸反应:
(2)钠与水的反应:
(3)向碳酸钠溶液中滴加少量盐酸:
(4)Ba(OH)2溶液与H2SO4溶液混合:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】我国著名化学家侯德榜发明的“联合制碱法”的反应原理用化学方程式可简要表示为:
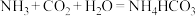 ,
,
 ;
;
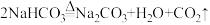 。
。
(1)纯碱属于___________ (填“酸”“碱”或“盐”)。
(2)检验碳酸氢钠中含有碳酸钠的方法是___________ 。
(3) ,请写出该反应能发生的原因
,请写出该反应能发生的原因_________ 。
(4)向含有碳酸钠和碳酸氢钠的溶液中逐滴滴加1 mol/L盐酸,产生标准状况下气体的体积与盐酸体积关系如图所示:
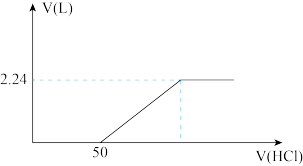
①逐滴滴加盐酸的过程中 物质的量变化趋势是
物质的量变化趋势是___________ ;
②上述混合溶液碳酸氢钠的物质的量是___________ 。
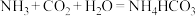 ,
, ;
;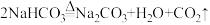 。
。(1)纯碱属于
(2)检验碳酸氢钠中含有碳酸钠的方法是
(3)
 ,请写出该反应能发生的原因
,请写出该反应能发生的原因(4)向含有碳酸钠和碳酸氢钠的溶液中逐滴滴加1 mol/L盐酸,产生标准状况下气体的体积与盐酸体积关系如图所示:

①逐滴滴加盐酸的过程中
 物质的量变化趋势是
物质的量变化趋势是②上述混合溶液碳酸氢钠的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某品牌小苏打粉中含有杂质NaCl,化学兴趣小组的同学进行了如下实验探究:称取10g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,并绘制出加入稀盐酸的质量与放出气体质量的关系如图:

(1)反应的化学方程式为_______ 。
(2)计算该样品的纯度_______ (写出计算过程)。
(3)计算当盐酸与小苏打恰好完全反应时,所得溶液的溶质质量分数是_______ (写出计算过程,结果保留一位小数)

(1)反应的化学方程式为
(2)计算该样品的纯度
(3)计算当盐酸与小苏打恰好完全反应时,所得溶液的溶质质量分数是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】胃酸过多是常见的胃病。下面是甲、乙两种常见胃药的说明摘要。
甲:(1)白色结晶状粉末,可缓缓分解;(2)能溶于水,水溶液呈弱碱性;(3)遇酸及酸性药物则产生二氧化碳;(4)胃酸过多患者服用多见胃胀气,甚至有引起胃穿孔的危险。
乙:(1)与胃酸的中和作用缓慢而持久,可维持3~4小时;(2)凝胶本身覆盖于溃疡面上,具有保护作用;(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成分是______ (填化学式);乙中含有的主要化学成分是__________ (填化学式)。
(2)试写出甲中含有的主要化学成分引起胃胀气反应的离子方程式:_________ 。
(3)试写出乙中含有的主要化学成分分别与稀盐酸和氢氧化钠溶液反应的离子方程式:___ 。
甲:(1)白色结晶状粉末,可缓缓分解;(2)能溶于水,水溶液呈弱碱性;(3)遇酸及酸性药物则产生二氧化碳;(4)胃酸过多患者服用多见胃胀气,甚至有引起胃穿孔的危险。
乙:(1)与胃酸的中和作用缓慢而持久,可维持3~4小时;(2)凝胶本身覆盖于溃疡面上,具有保护作用;(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成分是
(2)试写出甲中含有的主要化学成分引起胃胀气反应的离子方程式:
(3)试写出乙中含有的主要化学成分分别与稀盐酸和氢氧化钠溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铝是地壳中含量最高的金属元素,化学性质活泼。
(1)在通常情况下,金属铝制品能稳定地存在,不被氧化且不跟水作用,是因为______
(2)将在空气中长时间放置的铝条浸入6mol/L的氢氧化钠溶液中,发现刚开始没有气泡,后来出现大量气泡。出现这一现象的原因是(用文字和方程式表述)____________
(3)明矾是常见的净水剂,写出明矾净水的原因(用文字和方程式表述)____________
(1)在通常情况下,金属铝制品能稳定地存在,不被氧化且不跟水作用,是因为
(2)将在空气中长时间放置的铝条浸入6mol/L的氢氧化钠溶液中,发现刚开始没有气泡,后来出现大量气泡。出现这一现象的原因是(用文字和方程式表述)
(3)明矾是常见的净水剂,写出明矾净水的原因(用文字和方程式表述)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铝(熔点660℃)是一种应用广泛的金属,工业上用 (熔点2045℃)和冰晶石(
(熔点2045℃)和冰晶石(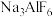 )混合熔融后电解制得。请回答下列问题:
)混合熔融后电解制得。请回答下列问题:
(1)铝属于活泼金属却能在空气中稳定存在,其原因是__________ ,冶金工业上常用金属铝作还原剂冶炼钒、铬、锰等金属,请写出铝与V2O5在高温下反应的化学方程式:___________ 。
(2)将 液和
液和 溶液混合制取
溶液混合制取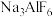 。该实验用于盛装NaF溶液的试剂瓶
。该实验用于盛装NaF溶液的试剂瓶_________ (填“能”或“不能”)用玻璃瓶,原因是_______ 。
(3)下列关于铝元素的叙述不正确的是__________ (填序号)。
A.铝是人类最早使用的金属
B.镁铝合金既可完全溶于过量的盐酸,又可完全溶于过量的NaOH溶液
C.氢氧化铝是一种两性氢氧化物,既能溶于盐酸又能溶于NaOH溶液
D.铝是人体必需的微量元素之一,因此在生活中人们应尽量使用铝制炊具和餐具更有利于身体健康
(4)某工厂排放出有毒物质NOCl,它遇水就会生成 。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为
。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_______ ,水源中的 对人类健康会产生危害,为了降低水源中
对人类健康会产生危害,为了降低水源中 的浓度,有研究人员建议在碱性条件下用铝粉将
的浓度,有研究人员建议在碱性条件下用铝粉将 还原为N2,此时铝主要以
还原为N2,此时铝主要以 的形式存在于溶液中,请写出该反应的离子方程式:
的形式存在于溶液中,请写出该反应的离子方程式:_______ ,当该反应转移10mol电子时,产生的 在标准状况下的体积约为
在标准状况下的体积约为______ (写出计算过程)。
 (熔点2045℃)和冰晶石(
(熔点2045℃)和冰晶石(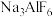 )混合熔融后电解制得。请回答下列问题:
)混合熔融后电解制得。请回答下列问题:(1)铝属于活泼金属却能在空气中稳定存在,其原因是
(2)将
 液和
液和 溶液混合制取
溶液混合制取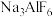 。该实验用于盛装NaF溶液的试剂瓶
。该实验用于盛装NaF溶液的试剂瓶(3)下列关于铝元素的叙述不正确的是
A.铝是人类最早使用的金属
B.镁铝合金既可完全溶于过量的盐酸,又可完全溶于过量的NaOH溶液
C.氢氧化铝是一种两性氢氧化物,既能溶于盐酸又能溶于NaOH溶液
D.铝是人体必需的微量元素之一,因此在生活中人们应尽量使用铝制炊具和餐具更有利于身体健康
(4)某工厂排放出有毒物质NOCl,它遇水就会生成
 。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为
。NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为 对人类健康会产生危害,为了降低水源中
对人类健康会产生危害,为了降低水源中 的浓度,有研究人员建议在碱性条件下用铝粉将
的浓度,有研究人员建议在碱性条件下用铝粉将 还原为N2,此时铝主要以
还原为N2,此时铝主要以 的形式存在于溶液中,请写出该反应的离子方程式:
的形式存在于溶液中,请写出该反应的离子方程式: 在标准状况下的体积约为
在标准状况下的体积约为
您最近一年使用:0次





