如图实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题
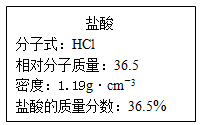
(1)该浓盐酸中HCl的物质的量浓度为______ mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______ 。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol/L的稀盐酸。该学生需要量取______ mL上述浓盐酸进行配制。
(4)①假设该同学成功配制了0.400 mol/L的盐酸,他又用该盐酸中和含0.4 g NaOH的NaOH溶液,则该同学需取______ mL盐酸。
②配制100mL0.4mol/L的盐酸溶液,所需的玻璃仪器有烧杯、玻璃棒、量筒和_______ 。

(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol/L的稀盐酸。该学生需要量取
(4)①假设该同学成功配制了0.400 mol/L的盐酸,他又用该盐酸中和含0.4 g NaOH的NaOH溶液,则该同学需取
②配制100mL0.4mol/L的盐酸溶液,所需的玻璃仪器有烧杯、玻璃棒、量筒和
更新时间:2017-12-23 12:45:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现将600mL稀硫酸等体积分为6份,并向其中5份中分别加入质量不等的Zn粒,并收集生成的氢气,有以下记录结果。(氢气的体积已折算为标准状况)
(1)由实验结果可推知,此稀硫酸的物质的量浓度为____________ 。
(2)实验②收集到H2的体积为____________ 。
(3)若向第6份稀硫酸中不断加入Zn粒,请在下图中画出H2体积(V)与Zn粒质量(m)的关系图象____________ 。

| 实验① | 实验② | 实验③ | 实验④ | 实验⑤ | |
| Zn质量(g) | 5.0 | 8.0 | 12 | 14 | 16 |
| H2体积(L) | 1.72 | 4.14 | 4.48 | 4.48 |
(1)由实验结果可推知,此稀硫酸的物质的量浓度为
(2)实验②收集到H2的体积为
(3)若向第6份稀硫酸中不断加入Zn粒,请在下图中画出H2体积(V)与Zn粒质量(m)的关系图象

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】浓硫酸和铜片加热后反应,铜片完全溶解后测得产生2.24L(S.T.P)气体,把反应后溶液稀释至1L,取20mL溶液加入足量BaCl2溶液产生3.728g沉淀,求原硫酸溶液的物质的量是多少?_________
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氨和硝酸都是重要的工业原料.
(1)标准状况下,将500L氨气溶于水形成1L氨水,则此氨水的物质的量浓度为______ mol/L(保留三位有效数字).工业上常用过量氨水吸收二氧化硫,该反应的化学方程式为_______ .
(2)工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH﹣=NO2﹣+NO3﹣+H2O和NO+NO2+2OH﹣=□_____ +H2O(配平该方程式).
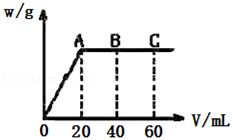
(3)有H2SO4和HNO3的混合溶液20mL,加入0.25mol•L﹣1 Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C 点混合液呈中性).则原混合液中H2SO4的物质的量浓度为______ mol/L,HNO3的物质的量浓度为_____ mol/L.
(1)标准状况下,将500L氨气溶于水形成1L氨水,则此氨水的物质的量浓度为
(2)工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH﹣=NO2﹣+NO3﹣+H2O和NO+NO2+2OH﹣=□
(3)有H2SO4和HNO3的混合溶液20mL,加入0.25mol•L﹣1 Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C 点混合液呈中性).则原混合液中H2SO4的物质的量浓度为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.实验室配制490mL0.3mol/L的NaOH溶液
(1)需称量NaOH固体_____ g
(2)在该溶液的配制过程中,用到的玻璃仪器:量筒、烧杯、玻璃棒_____ 。
(3)如果在定容时仰视,溶液浓度将_____ ;(填“偏大”“偏小”“不影响” )
Ⅱ、取上述实验中配制的NaOH溶液200mL,缓慢通入一定量的CO2,充分反应,测最后溶液的pH>7。在上述所得溶液中,逐滴缓慢滴加一定浓度的盐酸,所得气体的体积与所加盐酸的体积(不考虑溶解于水)关系如图所示:

(4)加入盐酸200mL之前,无气体产生,写出OA段发生反应的离子方程式_____ 。
(5)A点时,反应所得溶液中溶质的成分有______
(6)产生的CO2在标准状况下的体积为_____ mL。
(1)需称量NaOH固体
(2)在该溶液的配制过程中,用到的玻璃仪器:量筒、烧杯、玻璃棒
(3)如果在定容时仰视,溶液浓度将
Ⅱ、取上述实验中配制的NaOH溶液200mL,缓慢通入一定量的CO2,充分反应,测最后溶液的pH>7。在上述所得溶液中,逐滴缓慢滴加一定浓度的盐酸,所得气体的体积与所加盐酸的体积(不考虑溶解于水)关系如图所示:

(4)加入盐酸200mL之前,无气体产生,写出OA段发生反应的离子方程式
(5)A点时,反应所得溶液中溶质的成分有
(6)产生的CO2在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】从溶质改变角度分析产生的误差(用“偏大”“偏小”或“无影响”填空)。
(1)配制450mL0.1mol·L-1的NaOH溶液,用托盘天平称取NaOH固体1.8g:___________ 。
(2)配制500mL0.1mol·L-1的硫酸铜溶液,用托盘天平称取胆矾8.0g:___________ 。
(3)配制NaOH溶液时,托盘天平的两个托盘上放两张质量相等的纸片,其他操作均正确:___________ 。
(4)配制一定物质的量浓度的NaOH溶液,需称量溶质4.4g,称量时物码放置颠倒:_______ 。
(5)用量筒量取浓硫酸时,仰视读数:___________ 。
(6)定容时,加水超过刻度线,用胶头滴管吸取多余的液体至刻度线:___________ 。
(7)未洗涤烧杯及玻璃棒:___________ 。
(1)配制450mL0.1mol·L-1的NaOH溶液,用托盘天平称取NaOH固体1.8g:
(2)配制500mL0.1mol·L-1的硫酸铜溶液,用托盘天平称取胆矾8.0g:
(3)配制NaOH溶液时,托盘天平的两个托盘上放两张质量相等的纸片,其他操作均正确:
(4)配制一定物质的量浓度的NaOH溶液,需称量溶质4.4g,称量时物码放置颠倒:
(5)用量筒量取浓硫酸时,仰视读数:
(6)定容时,加水超过刻度线,用胶头滴管吸取多余的液体至刻度线:
(7)未洗涤烧杯及玻璃棒:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)0.5 mol H2O的质量为____ ,含有______ 个原子。
(2)质量都是50 g的 HCl、CH4、N2三种气体中,原子数目最多的是气体是_______ ,在相同温度和相同压强条件下,密度最大的气体是__________ 。
(3)标准状况下11.2L,由CO和H2组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为_______ 。
(4)实验室需用浓硫酸配制100 mL 1 mol•L-1的稀硫酸。可供选用的仪器有:
①量筒;②烧杯;③胶头滴管,还必须需要的玻璃仪器有________________ (写仪器名称)。
(5)一定条件下,RO 和Cl2可发生如下反应:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,从而可知在RO
和Cl2可发生如下反应:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,从而可知在RO 中,元素R的化合价是
中,元素R的化合价是_____ ,当有标准状况下8.96L Cl2被消耗时,反应中共转移电子物质的量为____ mol。
(2)质量都是50 g的 HCl、CH4、N2三种气体中,原子数目最多的是气体是
(3)标准状况下11.2L,由CO和H2组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为
(4)实验室需用浓硫酸配制100 mL 1 mol•L-1的稀硫酸。可供选用的仪器有:
①量筒;②烧杯;③胶头滴管,还必须需要的玻璃仪器有
(5)一定条件下,RO
 和Cl2可发生如下反应:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,从而可知在RO
和Cl2可发生如下反应:RO3n-+Cl2+H2O==RO42-+2Cl-+2H+ ,从而可知在RO 中,元素R的化合价是
中,元素R的化合价是
您最近一年使用:0次



