将一块表面氧化为Na2O的钠块共5.22克放入水中,充分反应后收集到标准状况下的氢气2.24L,并恰好生成500mL溶液,试计算:(请写出计算过程)
(1)钠块表面被氧化的钠的质量;
(2)所得溶液物质的量浓度。
(1)钠块表面被氧化的钠的质量;
(2)所得溶液物质的量浓度。
更新时间:2017-12-23 10:46:25
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)标准状况下,33.6 L 的 HCl 所具有的物质的量为___________ ,将其溶解于水配成3 L的溶液,所得盐酸的物质的量浓度为___________ 。
(2)商品硫酸的质量分数为 98%,密度为 1.84g/cm3,则它的物质的量浓度为___________ ,18 mol/L 浓 H2SO4100mL,可配制 6 mol / L 的稀 H2SO4___________ mL
(3)如果 ag 某气体中含有的分子数为 b,则 cg 该气体在标准状况下的体积是___________ L
(2)商品硫酸的质量分数为 98%,密度为 1.84g/cm3,则它的物质的量浓度为
(3)如果 ag 某气体中含有的分子数为 b,则 cg 该气体在标准状况下的体积是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)标准状况下,2.24LCl2的质量为__ g;标准状况下,将aLHCl气体溶于水配成500mL0.4mol•L-1的溶液,则a=__ 。
(2)在无土栽培中,1L营养液的标准配置为5mol/LNH4Cl、1.6mol/LKCl、2.4mol/LK2SO4,若改用KCl、NH4Cl、(NH4)2SO4配制1L营养液,则NH4Cl的物质的量浓度为__ 。
(3)标准状况下,mg气体A和ng气体B具有相等的体积,则同温同压下A、B的密度之比为__ ,同质量的A、B的分子数目之比为__ 。
(4)在标准状况下,由CO和CO2组成的混合气体11.2L,质量为20g,该混合气体中,CO和CO2物质的量之比为___ ,碳与氧两种原子的数目之比为__ 。
(1)标准状况下,2.24LCl2的质量为
(2)在无土栽培中,1L营养液的标准配置为5mol/LNH4Cl、1.6mol/LKCl、2.4mol/LK2SO4,若改用KCl、NH4Cl、(NH4)2SO4配制1L营养液,则NH4Cl的物质的量浓度为
(3)标准状况下,mg气体A和ng气体B具有相等的体积,则同温同压下A、B的密度之比为
(4)在标准状况下,由CO和CO2组成的混合气体11.2L,质量为20g,该混合气体中,CO和CO2物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】计算:
(1)3.6 g H2O的物质的量是_______ mol,含有_______ mol质子。
(2)22 g CO2在标准状况下的体积是_______ L。
(3)10.6 g Na2CO3固体溶于水配成100 mL溶液,其物质的量浓度为_______ mol/L。将其稀释至1000 mL,其物质的量浓度为_______ mol/L。
(4)现有200 mL0.27 kg的质量分数为10%的CuCl2溶液。计算:溶液中CuCl2物质的量浓度为_______ 。
(1)3.6 g H2O的物质的量是
(2)22 g CO2在标准状况下的体积是
(3)10.6 g Na2CO3固体溶于水配成100 mL溶液,其物质的量浓度为
(4)现有200 mL0.27 kg的质量分数为10%的CuCl2溶液。计算:溶液中CuCl2物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】化学计量在化学中占有重要地位,请回答下列问题。
(1)0.3molNH3分子中所含原子数与____________ 个H2O分子中所含原子数相等。
(2)含0.4mol Al3+的Al2(SO4)3中所含的SO 的物质的量是
的物质的量是____________ 。
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为_____________ 。
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是_______________ 。
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO ,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol·L-l、0.25mol·L-l、0.4mol·L-l,则c(SO42-)=
,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol·L-l、0.25mol·L-l、0.4mol·L-l,则c(SO42-)=_____________ 。
(1)0.3molNH3分子中所含原子数与
(2)含0.4mol Al3+的Al2(SO4)3中所含的SO
 的物质的量是
的物质的量是(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO
 ,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol·L-l、0.25mol·L-l、0.4mol·L-l,则c(SO42-)=
,测得Na+、Mg2+和Cl-的物质的量浓度依次为:0.2mol·L-l、0.25mol·L-l、0.4mol·L-l,则c(SO42-)=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】准确称取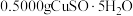 样品,加适量水溶解,转移至碘量瓶中,加过量
样品,加适量水溶解,转移至碘量瓶中,加过量 溶液并用稀
溶液并用稀 酸化,以淀粉溶液为指示剂,用
酸化,以淀粉溶液为指示剂,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 的溶液
的溶液 。测定过程中发生下列反应:
。测定过程中发生下列反应: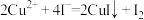 、
、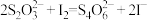 。计算
。计算 样品的纯度(写出计算过程):
样品的纯度(写出计算过程):_________ 。
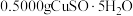 样品,加适量水溶解,转移至碘量瓶中,加过量
样品,加适量水溶解,转移至碘量瓶中,加过量 溶液并用稀
溶液并用稀 酸化,以淀粉溶液为指示剂,用
酸化,以淀粉溶液为指示剂,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 的溶液
的溶液 。测定过程中发生下列反应:
。测定过程中发生下列反应: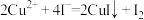 、
、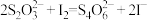 。计算
。计算 样品的纯度(写出计算过程):
样品的纯度(写出计算过程):
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)12.4gNa2X中含有0.4molNa+,则Na2X的摩尔质量为______ 。
(2)50mL1mol/LMgCl2溶液中Cl-浓度与150mL_______ mol/LKCl溶液中Cl-浓度相等。
(3)标准状况下,3.4gNH3的体积为_______ L;它与标准状况下_______ LH2S含有相同数目的氢原子。
(4)已知ag氢气中含有b个氢原子,则阿伏加 德罗常数的数值可表示为_______ 。
(5)由于金属钠具有很强的_______ 性(填“氧化”或“还原”),很容易跟空气中的_______ 、_______ 等物质反应,通常将它保存在_______ 里。
(2)50mL1mol/LMgCl2溶液中Cl-浓度与150mL
(3)标准状况下,3.4gNH3的体积为
(4)已知ag氢气中含有b个氢原子,则阿伏加 德罗常数的数值可表示为
(5)由于金属钠具有很强的
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】1.15g金属钠跟水反应:2Na+2H2O==2NaOH+H2↑,得到100mL溶液,试计算:
⑴生成的气体在标准状况下是多少升?____________
⑵反应后所得溶液的物质的量浓度是多少______________
⑶若把1.15g金属钠在氧气中燃烧,得到产物过氧化钠(Na2O2)的质量是多少?__________
⑴生成的气体在标准状况下是多少升?
⑵反应后所得溶液的物质的量浓度是多少
⑶若把1.15g金属钠在氧气中燃烧,得到产物过氧化钠(Na2O2)的质量是多少?
您最近一年使用:0次




