(1)下列五个反应
A.5Cl2+I2+6H2O=10HCl+2HIO3
B.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
C.2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O
D.2NaCl+2H2O 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
E.MnO2+4HCl MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
上述反应中氯元素只被氧化的是_____________ ,(填字母,下同)只被还原的是_____________ ,部分被氧化的是_____________ ,C中被氧化与被还原的物质的量之比为_____________ 。
(2)在反应4(NH4)2SO4 N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为
N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为___________ ,生成56gN2转移的电子___________ mol。
(3)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。上述反应中,若产生2mol N2,转移电子数为_________ (用NA表示阿伏伽德罗常数);用“双线桥”表示反应中电子转移,化合价的变化,反应类型:______________ 。
(4)将等质量的两份镁、铝合金分别投入足量的NaOH和HCl中,在相同的情况下测得生成气体的体积之比为1:2,求合金中镁、铝的物质的量之比为___________ 。
A.5Cl2+I2+6H2O=10HCl+2HIO3
B.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
C.2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O
D.2NaCl+2H2O
 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑ E.MnO2+4HCl
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O 上述反应中氯元素只被氧化的是
(2)在反应4(NH4)2SO4
 N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为
N2↑+6NH3↑+3SO2↑+SO3↑+7H2O中,氧化产物与还原产物的物质的量之比为(3)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10A1+6NaNO3+4NaOH==10NaA1O2+3N2↑+2H2O。上述反应中,若产生2mol N2,转移电子数为
(4)将等质量的两份镁、铝合金分别投入足量的NaOH和HCl中,在相同的情况下测得生成气体的体积之比为1:2,求合金中镁、铝的物质的量之比为
17-18高一上·贵州遵义·阶段练习 查看更多[3]
贵州省遵义市第四中学2017-2018学年高一上学期第二次月考化学试题(已下线)黄金30题系列 高一化学 大题好拿分【基础版】【全国百强校】贵州省贵阳市第一中学2018-2019学年高二上学期第一次月考化学试题
更新时间:2017-12-28 14:56:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下图是已破损的维生素C(简写作VC)说明书部分信息。已知维生素C由碳、氢、氧三种元素组成。回答下列问题:

(1)VC的化学式为_______ ,摩尔质量为_______ 。
(2)VC中碳、氢元素的质量比为_______ ,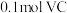 中含氧原子数为
中含氧原子数为_______ 。
(3)小王妈妈每天按上述用法与用量服用该VC片剂,小王建议妈妈食用西红柿来代替VC片,若100g西红柿含 ,则小王妈妈每天需食用西红柿
,则小王妈妈每天需食用西红柿_____ g才可达到服用上述VC片的效果。

(1)VC的化学式为
(2)VC中碳、氢元素的质量比为
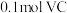 中含氧原子数为
中含氧原子数为(3)小王妈妈每天按上述用法与用量服用该VC片剂,小王建议妈妈食用西红柿来代替VC片,若100g西红柿含
 ,则小王妈妈每天需食用西红柿
,则小王妈妈每天需食用西红柿
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)设NA代表阿伏加德罗常数,某晶体的化学式为Na0.35CoO2·1.3H2O,已知1 mol该晶体的质量是122.45g,则该晶体的相对分子质量是__________ ;钴原子与氧原子的物质的量之比是________ (比值可以用小数表示);1 mol该晶体中含有的氧原子数目为______________
(2)在相同条件下,体积均相等的 CH4、N2、CO2、O2四种气体中,含有原子数目最多的是________ ,质量最大的是________________
(3)将27.8gFeSO4·7H2O溶于水配成100mL FeSO4溶液,从中取出20mL,此20mL溶液中C(Fe2+)为______ ,m(FeSO4) 为__________ ,将取出的20mL溶液加水稀释到100mL,则稀释后溶液中C(FeSO4)为________
(4)完全中和相同体积、相同物质的量浓度的Ba(OH)2溶液,需要相同物质的量浓度的盐酸、硫酸溶液的体积比为_____________ 。
(5)在体积为V L的密闭容器中通入x mol CO和y mol O2,在一定条件下反应后,测得此时容器中的C和O的个数之比为__________ 。
(2)在相同条件下,体积均相等的 CH4、N2、CO2、O2四种气体中,含有原子数目最多的是
(3)将27.8gFeSO4·7H2O溶于水配成100mL FeSO4溶液,从中取出20mL,此20mL溶液中C(Fe2+)为
(4)完全中和相同体积、相同物质的量浓度的Ba(OH)2溶液,需要相同物质的量浓度的盐酸、硫酸溶液的体积比为
(5)在体积为V L的密闭容器中通入x mol CO和y mol O2,在一定条件下反应后,测得此时容器中的C和O的个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】实验室用 与浓盐酸共热制备
与浓盐酸共热制备 ,反应如下:
,反应如下:
(1)该反应中被氧化的元素是___________ ,还原产物是___________ ;
(2)用单线桥标明电子转移的方向与数目___________ 。
(3)该反应中,氧化剂与还原剂的物质的量之比为___________ (前者比后者);盐酸在反应中表现出来的性质是___________ 。
(4)当生成标准状况下 时,转移的电子数目为
时,转移的电子数目为___________ ,被氧化的还原剂的物质的量为___________ 。
(5)也可以用 和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用
和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用 的原因:
的原因:___________ 。
(6)举例说明氯气的氧化性比硫单质强,___________ 。
 与浓盐酸共热制备
与浓盐酸共热制备 ,反应如下:
,反应如下:
(1)该反应中被氧化的元素是
(2)用单线桥标明电子转移的方向与数目
(3)该反应中,氧化剂与还原剂的物质的量之比为
(4)当生成标准状况下
 时,转移的电子数目为
时,转移的电子数目为(5)也可以用
 和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用
和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用 的原因:
的原因:(6)举例说明氯气的氧化性比硫单质强,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氢氧化钠是白色固体,易潮解,具有强腐蚀性,所以又叫火碱、烧碱、苛性钠。是常用的碱性干燥剂,是重要的化工原料。
工业制法:氯碱工业2NaCl+2H2O Cl2↑+H2↑+2NaOH
Cl2↑+H2↑+2NaOH
苛化法:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
在实验室,钠、氧化钠(Na2O)、过氧化钠(Na2O2)分别与水反应都生成NaOH。回答下列问题:
(1)在“氯碱工业”反应中,反应前后氯元素的化合价变化是____ (填“升高”、“降低”、“不变”)。
(2)Ca(OH)2可拆写,苛化法的离子方程式为____ 。
(3)写出Na2O与水反应的化学方程式____ 。
(4)补项:过氧化钠与水反应为:2Na2O2+2H2O=4NaOH+____ ↑。
(5)NaOH固体不能干燥酸性气体。能用NaOH固体干燥的气体是____ (填序号)。
a.HCl b.H2 c.NH3(碱性气体) d.CO2
工业制法:氯碱工业2NaCl+2H2O
 Cl2↑+H2↑+2NaOH
Cl2↑+H2↑+2NaOH苛化法:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
在实验室,钠、氧化钠(Na2O)、过氧化钠(Na2O2)分别与水反应都生成NaOH。回答下列问题:
(1)在“氯碱工业”反应中,反应前后氯元素的化合价变化是
(2)Ca(OH)2可拆写,苛化法的离子方程式为
(3)写出Na2O与水反应的化学方程式
(4)补项:过氧化钠与水反应为:2Na2O2+2H2O=4NaOH+
(5)NaOH固体不能干燥酸性气体。能用NaOH固体干燥的气体是
a.HCl b.H2 c.NH3(碱性气体) d.CO2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据要求,回答下列问题:
(1)已知下列反应:① ②
②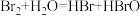 ③
③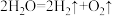 ④
④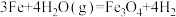 ⑤
⑤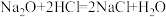
反应①的基本反应类型为:______ ,属于置换反应的有_____ (填序号,下同),上述反应中不属于氧化还原反应的有____ ;H2O被氧化的是_____ ,H2O被还原的是_____ ;属于氧化还原反应,但其中的H2O既不被氧化又不被还原的是_____ 。
(2)将下列五种物质:KMnO4、MnSO4、FeSO4、Fe2(SO4)3、K2SO4分别填入下列对应的横线上,组成一个未配平的化学方程式:
____ ;该反应中的氧化产物是__ (填化学式),被还原的是____ (填化学式)中的______ (填元素符号)元素。
(3)用双线桥法表示反应 的电子转移方向与数目
的电子转移方向与数目______ 。
(1)已知下列反应:①
 ②
②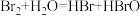 ③
③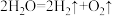 ④
④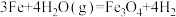 ⑤
⑤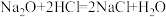
反应①的基本反应类型为:
(2)将下列五种物质:KMnO4、MnSO4、FeSO4、Fe2(SO4)3、K2SO4分别填入下列对应的横线上,组成一个未配平的化学方程式:

(3)用双线桥法表示反应
 的电子转移方向与数目
的电子转移方向与数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)书写下列反应的离子方程式
①NaOH溶液和HCl溶液:_________________ ;
②NaCl溶液和AgNO3溶液:___________ ;
③Na2CO3溶液和氢氧化钙溶液:______________ 。
(2)在2KMnO4+16HCl(浓)═2MnCl2+2KCl+5Cl2↑+8H2O反应中:
①______ 被氧化,氧化剂_______ ,氧化产物是______ ; 还原剂__________ ,还原产物是____ 。
②用双线桥法表示该反应的电子转移情况__________
①NaOH溶液和HCl溶液:
②NaCl溶液和AgNO3溶液:
③Na2CO3溶液和氢氧化钙溶液:
(2)在2KMnO4+16HCl(浓)═2MnCl2+2KCl+5Cl2↑+8H2O反应中:
①
②用双线桥法表示该反应的电子转移情况
您最近一年使用:0次
【推荐2】Cu2S和稀HNO3反应生成Cu(NO3)2、H2SO4、NO和H2O,试解答下列各题
(1)配平上述反应方程式并标出电子转移的方向和总数___________________________
(2)当产生0.1mol NO时,转移电子总数为______________ ,被还原的物质为_____ mol,共耗HNO3________ mol。
(3)被1mol Cu2S中+1价亚铜离子还原的HNO3的物质的量是_______ mol
(1)配平上述反应方程式并标出电子转移的方向和总数
(2)当产生0.1mol NO时,转移电子总数为
(3)被1mol Cu2S中+1价亚铜离子还原的HNO3的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)配平并用“双线桥”表示电子转移的方向和数目___ 。
____FeSO4+____KMnO4+____H2SO4=____Fe2(SO4)3+____K2SO4+____MnSO4+____H2O
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑,还原产物是___ ,每生成0.5molN2转移电子的物质的量为_____ 。
(3)某同学写出以下三个化学方程式(未配平),其中你认为一定不可能实现的是___ 。
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
(4)印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列后果不可能出现的是___ 。
(1)配平并用“双线桥”表示电子转移的方向和数目
____FeSO4+____KMnO4+____H2SO4=____Fe2(SO4)3+____K2SO4+____MnSO4+____H2O
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑,还原产物是
(3)某同学写出以下三个化学方程式(未配平),其中你认为一定不可能实现的是
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
(4)印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2。向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列后果不可能出现的是
| A.烧杯中有铜无铁 | B.烧杯中有铁无铜 |
| C.烧杯中铁、铜都有 | D.烧杯中铁、铜都无 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Cl2、SO2、NOx都是化工生产中的重要气体,均可用氨水或NaOH溶液处理,防止污染空气。请回答下列问题:
(1)以上气体所含元素原子中,未成对电子最多的原子是_______ (填元素符号),S原子中能量最高电子的电子云形状为_______ 。
(2)化工厂可用浓氨水来检验Cl2是否泄漏(已知3Cl2+8NH3→6NH4Cl+N2),当有少量Cl2泄漏时,可以观察到的现象是_______ ,若反应中有0.08mol的氨气被氧化,则有_______ mol电子发生转移。
(3)①若用热烧碱溶液吸收Cl2气反应后的混合溶液中,含NaCl、NaClO和NaClO3物质的量比值为n:1:1,则n=_______ 。
②SO2是形成酸雨的主要原因,取某化工区空气样本用蒸馏水处理,检测所得溶液,所含离子及其浓度如下:
根据表中数据计算,检测的溶液pH=_______ 。
(4)NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:_______ 。
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH→NaNO2+NaNO3+H2O,NO2+NO+2NaOH→2NaNO2+H2O),当消耗100mL0.5mol⋅L-1的烧碱溶液时,共吸收混合气体_______ L(标准状态)。
(1)以上气体所含元素原子中,未成对电子最多的原子是
(2)化工厂可用浓氨水来检验Cl2是否泄漏(已知3Cl2+8NH3→6NH4Cl+N2),当有少量Cl2泄漏时,可以观察到的现象是
(3)①若用热烧碱溶液吸收Cl2气反应后的混合溶液中,含NaCl、NaClO和NaClO3物质的量比值为n:1:1,则n=
②SO2是形成酸雨的主要原因,取某化工区空气样本用蒸馏水处理,检测所得溶液,所含离子及其浓度如下:
| 离子 | Na+ | K+ | NH | H+ | SO | NO | Cl- |
| 浓度/(mol·L-1) | 6×10-6 | 4×10-6 | 2×10-5 | a | 4×10-5 | 2×10-5 | 3×10-5 |
(4)NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH→NaNO2+NaNO3+H2O,NO2+NO+2NaOH→2NaNO2+H2O),当消耗100mL0.5mol⋅L-1的烧碱溶液时,共吸收混合气体
您最近一年使用:0次
【推荐2】阅读下面科普信息,回答问题:
一个体重50kg的健康人含铁2g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是_________
A.Fe B.Fe2+ C.Fe3+
(2)工业盐中毒后,可以服用维生素C来缓解中毒状况,这说明维生素C具有______ 性。
(3)在Fe+4HNO3(稀)═Fe(NO3)3+NO+H2O↑的反应中,用双线桥法表示电子的转移____________ ,反应中HNO3表现出了______ 性和______ 性,则1molFe参加反应时,被还原的HNO3为_________ mol,转移电子数为________ mol。
一个体重50kg的健康人含铁2g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)工业盐中毒后,可以服用维生素C来缓解中毒状况,这说明维生素C具有
(3)在Fe+4HNO3(稀)═Fe(NO3)3+NO+H2O↑的反应中,用双线桥法表示电子的转移
您最近一年使用:0次
【推荐3】化学与生产、生活息息相关。请回答下列问题:
(1)小苏打是常用的食品添加剂,烘焙面包时可用它做膨松剂,还可以调节酸度,写出调领闹节酸度时的离子反应方程式__________ 。
(2)汽车尾气的主要成分是CO和NO,加入适当催化剂,可使两者反应生成 和另种无毒的气体,写出反应的化学方程式
和另种无毒的气体,写出反应的化学方程式__________ ,做还原剂的是__________ 。
(3)工业上常用稀盐酸清洗锅炉内壁的水垢(主要成份是碳酸钙和氢氧化镁),请写出反应的离子方程式__________ (写出一个即可)。
(4)工业废水中含有的重铬酸根离子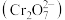 有毒,必须处理达标后才能排放。工业上常用绿矾
有毒,必须处理达标后才能排放。工业上常用绿矾 做处理剂,反应的离子方程式如下:
做处理剂,反应的离子方程式如下:
该离子方程式中的X应为__________ (填微粒符号),当反应转移了 电子时,生成
电子时,生成 的物质的量为
的物质的量为__________ (保留两位有效数字)。
(1)小苏打是常用的食品添加剂,烘焙面包时可用它做膨松剂,还可以调节酸度,写出调领闹节酸度时的离子反应方程式
(2)汽车尾气的主要成分是CO和NO,加入适当催化剂,可使两者反应生成
 和另种无毒的气体,写出反应的化学方程式
和另种无毒的气体,写出反应的化学方程式(3)工业上常用稀盐酸清洗锅炉内壁的水垢(主要成份是碳酸钙和氢氧化镁),请写出反应的离子方程式
(4)工业废水中含有的重铬酸根离子
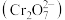 有毒,必须处理达标后才能排放。工业上常用绿矾
有毒,必须处理达标后才能排放。工业上常用绿矾 做处理剂,反应的离子方程式如下:
做处理剂,反应的离子方程式如下:
该离子方程式中的X应为
 电子时,生成
电子时,生成 的物质的量为
的物质的量为
您最近一年使用:0次

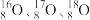 ②
②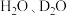 ③石墨、金刚石④
③石墨、金刚石④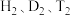 ⑤H、D、T⑥
⑤H、D、T⑥ ,回答下列问题:
,回答下列问题: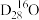 的摩尔质量为
的摩尔质量为

