按要求完成下列各题。
(1)向澄清石灰水中通入过量CO2(写出离子方程式)___________________________________
(2)用稀硫酸洗铁锈(Fe2O3)(写出离子方程式)____________________________________
(3)2Al + 6H+= 2Al3++ 3H2↑(写出对应的化学方程式并用双线桥法标出电子转移情况)__________________
(4)在一定条件下,某化合物W受热分解:2W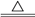 A↑+2B↑+4C↑,测得反应后生成的混合气体的密度是相同条件下H2密度的12倍,则W的摩尔质量是
A↑+2B↑+4C↑,测得反应后生成的混合气体的密度是相同条件下H2密度的12倍,则W的摩尔质量是_______
(1)向澄清石灰水中通入过量CO2(写出离子方程式)
(2)用稀硫酸洗铁锈(Fe2O3)(写出离子方程式)
(3)2Al + 6H+= 2Al3++ 3H2↑(写出对应的化学方程式并用双线桥法标出电子转移情况)
(4)在一定条件下,某化合物W受热分解:2W
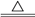 A↑+2B↑+4C↑,测得反应后生成的混合气体的密度是相同条件下H2密度的12倍,则W的摩尔质量是
A↑+2B↑+4C↑,测得反应后生成的混合气体的密度是相同条件下H2密度的12倍,则W的摩尔质量是
更新时间:2018-01-02 08:33:01
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】计算。
(1)0.3molNH3分子中所含原子数与___________ 个H2O分子中所含原子数相等。
(2)标准状况下1.12LNH3所含氨分子物质的量为_______ ,电子数为_________ 。
(3)3.9gNa2X含有Na+0.1mol,则Na2X的摩尔质量为___________ ,X的相对原子质量为___________ 。
(4)同温同压下,O2、SO2、SO3的质量之比为1∶2∶5,则它们所含的氧原子数之比为___ ,密度之比为_______ 。
(5)amLKAl(SO4)2溶液中含有Al3+xg,加水稀释至bmL,则稀释后所得溶液中c( )为
)为______ mol·L-1。
(6)14gC2H4与C4H8的混合物所含质子的物质的量为___________ 。
(1)0.3molNH3分子中所含原子数与
(2)标准状况下1.12LNH3所含氨分子物质的量为
(3)3.9gNa2X含有Na+0.1mol,则Na2X的摩尔质量为
(4)同温同压下,O2、SO2、SO3的质量之比为1∶2∶5,则它们所含的氧原子数之比为
(5)amLKAl(SO4)2溶液中含有Al3+xg,加水稀释至bmL,则稀释后所得溶液中c(
 )为
)为(6)14gC2H4与C4H8的混合物所含质子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】通过计算,回答下列问题:
(1)标况下 分子中所含原子数与
分子中所含原子数与______ 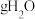 分子中所含原子数相等。
分子中所含原子数相等。
(2)一定条件下, 和
和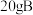 恰好完全反应生成
恰好完全反应生成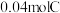 和
和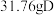 ,则C的摩尔质量为
,则C的摩尔质量为______ 。
(3)等质量的 和
和 中所含有的电子数之比为
中所含有的电子数之比为______ 。
(4)标准状况下, 与足量
与足量 反应转移的电子数为
反应转移的电子数为______ 。
(1)标况下
 分子中所含原子数与
分子中所含原子数与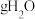 分子中所含原子数相等。
分子中所含原子数相等。(2)一定条件下,
 和
和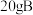 恰好完全反应生成
恰好完全反应生成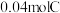 和
和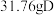 ,则C的摩尔质量为
,则C的摩尔质量为(3)等质量的
 和
和 中所含有的电子数之比为
中所含有的电子数之比为(4)标准状况下,
 与足量
与足量 反应转移的电子数为
反应转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)下列物质:①CO2②盐酸 ③烧碱晶体 ④酒精 ⑤铁 ⑥纯醋酸(用编号回答)其中能导电的是______ ,属于电解质的有____ ;属非电解质的是_______ 。
(2)0.270kg质量分数为10%的CuCl2溶液中CuCl2的物质的量___________ ,(带单位)
溶液中Cu2+和Cl-的物质的量分别为__________ ,___________ 。(带单位)
(3)标准状况下,224ml某气体的质量为0.32克,则该气体的相对分子质量__________ 。
(2)0.270kg质量分数为10%的CuCl2溶液中CuCl2的物质的量
溶液中Cu2+和Cl-的物质的量分别为
(3)标准状况下,224ml某气体的质量为0.32克,则该气体的相对分子质量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在某反应体系中存在六种物质:Cr3+、 、
、 、H+、H2O和
、H+、H2O和 。已知在该反应中氧化反应只有Cr3+→
。已知在该反应中氧化反应只有Cr3+→ ,反应过程中需要Ag+作催化剂,并加热。请回答下列问题:
,反应过程中需要Ag+作催化剂,并加热。请回答下列问题:
(1)已知 中存在一个过氧键(-O-O-),则
中存在一个过氧键(-O-O-),则 中硫元素的化合价为
中硫元素的化合价为_______ 价。
(2)写出该反应体系中发生反应的离子方程式:_______ 。
(3)催化剂往往参加反应,改变反应途径。用两个离子方程式表示Ag+的催化过程:_______ ;_______ 。
 、
、 、H+、H2O和
、H+、H2O和 。已知在该反应中氧化反应只有Cr3+→
。已知在该反应中氧化反应只有Cr3+→ ,反应过程中需要Ag+作催化剂,并加热。请回答下列问题:
,反应过程中需要Ag+作催化剂,并加热。请回答下列问题:(1)已知
 中存在一个过氧键(-O-O-),则
中存在一个过氧键(-O-O-),则 中硫元素的化合价为
中硫元素的化合价为(2)写出该反应体系中发生反应的离子方程式:
(3)催化剂往往参加反应,改变反应途径。用两个离子方程式表示Ag+的催化过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应在生产生活中应用十分广泛。
Ⅰ.人体正常的血红蛋白含有 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 ),则导致血红蛋白中的
),则导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可解毒。
而中毒,服用维生素C可解毒。
(1)关于上述过程,下列叙述正确的是___________(填字母)。
(2)金属加工后的废切削液中含2%~3%的 ,它是环境污染物,人们用
,它是环境污染物,人们用 溶液来处理,使
溶液来处理,使 转化为无毒物质,该反应分两步进行:
转化为无毒物质,该反应分两步进行:
第一步: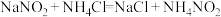
第二步: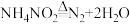
下列对第二步反应说法正确的是___________ 。
①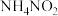 只是氧化剂 ②
只是氧化剂 ②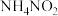 只是还原剂 ③
只是还原剂 ③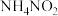 发生了分解反应
发生了分解反应
④只有氮元素的化合价发生了变化 ⑤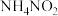 既是氧化剂又是还原剂
既是氧化剂又是还原剂
Ⅱ.高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾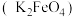 在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
(3)方法一: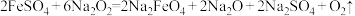 ,该反应中的氧化剂是
,该反应中的氧化剂是___________ ,氧化产物是___________ 。
(4)方法二: (未配平)
(未配平)
①配平离子反应方程式:_____ ____ _____
_____ _____
_____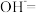 ______
______ _____
_____ ___
___
②若反应过程中转移了1.5mol电子,则还原产物的物质的量为______ mol。
(5)向 溶液中加入适量饱和的KOH溶液,有
溶液中加入适量饱和的KOH溶液,有 析出,请写出该反应的离子方程式:
析出,请写出该反应的离子方程式:___________ 。
Ⅰ.人体正常的血红蛋白含有
 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 ),则导致血红蛋白中的
),则导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可解毒。
而中毒,服用维生素C可解毒。(1)关于上述过程,下列叙述正确的是___________(填字母)。
| A.亚硝酸盐被还原 | B.维生素C是还原剂 |
C.维生素C还原性比 强 强 | D.亚硝酸盐是还原剂 |
 ,它是环境污染物,人们用
,它是环境污染物,人们用 溶液来处理,使
溶液来处理,使 转化为无毒物质,该反应分两步进行:
转化为无毒物质,该反应分两步进行:第一步:
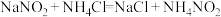
第二步:
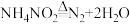
下列对第二步反应说法正确的是
①
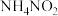 只是氧化剂 ②
只是氧化剂 ②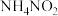 只是还原剂 ③
只是还原剂 ③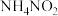 发生了分解反应
发生了分解反应④只有氮元素的化合价发生了变化 ⑤
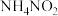 既是氧化剂又是还原剂
既是氧化剂又是还原剂Ⅱ.高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾
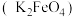 在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。(3)方法一:
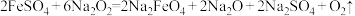 ,该反应中的氧化剂是
,该反应中的氧化剂是(4)方法二:
 (未配平)
(未配平)①配平离子反应方程式:
 _____
_____ _____
_____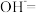 ______
______ _____
_____ ___
___
②若反应过程中转移了1.5mol电子,则还原产物的物质的量为
(5)向
 溶液中加入适量饱和的KOH溶液,有
溶液中加入适量饱和的KOH溶液,有 析出,请写出该反应的离子方程式:
析出,请写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】对于反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(1)写出上述反应的离子方程式_________________________ ;
(2)用双线桥法分析该反应的电子转移情况________________________ ;
(3)在该反应中氧化剂是_________ 被________________ 发生______ 反应;还原剂是_________ 被________ 发生______ 反应;氧化产物是_________ 还原产物是_________ 。
(1)写出上述反应的离子方程式
(2)用双线桥法分析该反应的电子转移情况
(3)在该反应中氧化剂是
您最近一年使用:0次
【推荐2】实验室可用KMnO4和浓盐酸反应制取氯气: KMnO4+HCl(浓)-KCl+MnCl2+Cl2↑+H2O
(1)配平上述离子方程式______ ,此反应中,氧化产物是_______ ,氧化性KMnO4_______ Cl2(选填“大于”或“小于”)
(2)若转移2 mol电子,则在标况下生成气体的体积_______
(3)浓盐酸在反应中显示出来的性质是_______
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)氧化剂与还原剂的物质的量之比为_______ 。
(5)用单线桥法表示下列反应的电子转移方向和数目。_______

(1)配平上述离子方程式
(2)若转移2 mol电子,则在标况下生成气体的体积
(3)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)氧化剂与还原剂的物质的量之比为
(5)用单线桥法表示下列反应的电子转移方向和数目。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)下列三组物质中,均有一种物质的类别与其它三种不同
A.MgO、Na2O、CO2、CuO B.HCl、H2O、H2SO4、HNO3 C.NaOH、Ca(ClO)2 、KOH、Cu(OH)2
三种物质依次是(填化学式):A______ 、B__________ 、C__________ 。
(2)在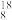 O中,中子数为
O中,中子数为____________ ;该原子与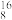 O是
O是____________ 关系。
(3)氯气与水反应的化学方程式:_________________ 。
(4)2Na+2H2O=2NaOH+H2↑,其中氧化剂为____________ ;还原剂为____________ ;氧化产物为____________ ;还原产物为为____________ ;并且用双线桥法标出当中的电子方向和数目____________________________________ 。
A.MgO、Na2O、CO2、CuO B.HCl、H2O、H2SO4、HNO3 C.NaOH、Ca(ClO)2 、KOH、Cu(OH)2
三种物质依次是(填化学式):A
(2)在
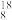 O中,中子数为
O中,中子数为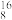 O是
O是(3)氯气与水反应的化学方程式:
(4)2Na+2H2O=2NaOH+H2↑,其中氧化剂为
您最近一年使用:0次



