铁、铜混合粉末20.0g加入到100mL 5.0 mol·L-1FeCl3溶液中,剩余固体质量为5.2g(忽略反应前后溶液体积变化)。求:
(1)反应后溶液中FeCl2的物质的量浓度_____________ mol·L-1
(2)原固体混合物中铜的质量分数是_____________
(1)反应后溶液中FeCl2的物质的量浓度
(2)原固体混合物中铜的质量分数是
更新时间:2017-02-23 23:31:31
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】Fe和Al是两种常用的金属,将它们按一定的质量比组成混合物。
(1)取一定质量的该混合物,向其中加入足量的NaOH溶液,生成气体的体积在标准状况下为n L,则反应的离子方程式为__________________ ,混合物中的Al的物质的量为___________ 。(用含字母的数学式表示)
(2)另取相同质量的该混合物,向其中加入足量的稀硫酸,固体全部溶解,生成气体的体积在标准状况下为m L,则反应中转移电子的物质的量为_________ ,混合物中Fe的质量为___________________ 。(用含字母的数学式表示)
(3)向(2)所得的溶液中加入过量的氢氧化钠溶液,将产生的沉淀过滤出来,经洗涤、干燥、灼烧后得到一种固体, 经称量发现该固体的质量和原混合物的质量恰好相等,则原混合物中铝的质量分数为______________ 。
(1)取一定质量的该混合物,向其中加入足量的NaOH溶液,生成气体的体积在标准状况下为n L,则反应的离子方程式为
(2)另取相同质量的该混合物,向其中加入足量的稀硫酸,固体全部溶解,生成气体的体积在标准状况下为m L,则反应中转移电子的物质的量为
(3)向(2)所得的溶液中加入过量的氢氧化钠溶液,将产生的沉淀过滤出来,经洗涤、干燥、灼烧后得到一种固体, 经称量发现该固体的质量和原混合物的质量恰好相等,则原混合物中铝的质量分数为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】有一稀硫酸和硝酸铁的混合溶液,向其中加入铁粉,溶液中的 Fe2+浓度如图所示(不考虑溶液体积的变化):
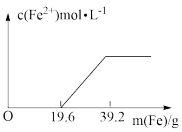
(1)铁离子和铁粉会反应,请写出反应的离子方程式_______
(2)溶液中H2SO4与 Fe(NO3)3的物质的量之比为_______

(1)铁离子和铁粉会反应,请写出反应的离子方程式
(2)溶液中H2SO4与 Fe(NO3)3的物质的量之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】铁在热的稀 中反应,其主要还原产物为
中反应,其主要还原产物为 ,而在冷的稀
,而在冷的稀 中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为
中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为 。请分析如图,回答有关问题。
。请分析如图,回答有关问题。
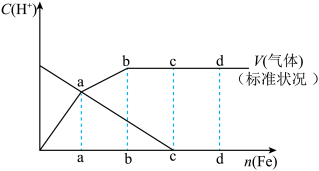
(1)假设在任一气体产生的曲线段内只有一种还原产物,试配平由b点到c点时的化学反应方程式:_____ Fe+____ HNO3—____ Fe(NO3)3+_________ +____ H2O
(2)判断从o点到a点时的还原产物,应是___________
(3)a点到b点时产生还原产物为_________ ,其原因是______________
(4)已知达到d点时反应完全结束,此时溶液中的主要阳离子为____________ 。
 中反应,其主要还原产物为
中反应,其主要还原产物为 ,而在冷的稀
,而在冷的稀 中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为
中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为 。请分析如图,回答有关问题。
。请分析如图,回答有关问题。 
(1)假设在任一气体产生的曲线段内只有一种还原产物,试配平由b点到c点时的化学反应方程式:
(2)判断从o点到a点时的还原产物,应是
(3)a点到b点时产生还原产物为
(4)已知达到d点时反应完全结束,此时溶液中的主要阳离子为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】向 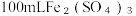 和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
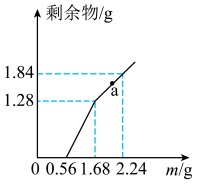
(1)加入少量铁粉时,发生的离子反应______________ 。
(2)原溶液中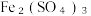 和CuSO4的物质的量之比为
和CuSO4的物质的量之比为_______ 。
(3)a点时溶液中溶质的物质的量浓度为____________ 。
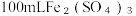 和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入铁粉的质量如图所示。(忽略溶液体积的变化)
(1)加入少量铁粉时,发生的离子反应
(2)原溶液中
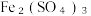 和CuSO4的物质的量之比为
和CuSO4的物质的量之比为(3)a点时溶液中溶质的物质的量浓度为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】氯化铁是常见的水处理剂,无水FeCl3 的熔点为282℃,沸点为315℃。工业上制备无水FeCl3 的一种工艺流程如下:

(1)氯化铁能用作水处理剂的原因是_________________ (用必要的文字和化学方程式说明)。
(2)吸收塔中吸收剂X 是_______ 。
(3)温度超过400℃时,捕集器中捕集到的物质的相对分子质量为325,该物质的分子式为________ 。
(4)从副产物FeCl3溶液中获得FeCl3·6H2O 的方法是在滴加浓盐酸后,________ 、________ 、过滤,洗涤、晾干。
(5)用FeCl3溶液(32%~35%)腐蚀印刷线路板的废液中含FeCl3、FeCl2和CuCl2。用化学方法回收废液中铜的方法是______________ (用反应式表示并简述操作要点)。

(1)氯化铁能用作水处理剂的原因是
(2)吸收塔中吸收剂X 是
(3)温度超过400℃时,捕集器中捕集到的物质的相对分子质量为325,该物质的分子式为
(4)从副产物FeCl3溶液中获得FeCl3·6H2O 的方法是在滴加浓盐酸后,
(5)用FeCl3溶液(32%~35%)腐蚀印刷线路板的废液中含FeCl3、FeCl2和CuCl2。用化学方法回收废液中铜的方法是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】一个体重50kg的健康人含铁元素2g,这2g铁元素以Fe2+和Fe3+形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4).服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收.
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+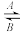 Fe3+.在过程A中,Fe2+作
Fe3+.在过程A中,Fe2+作____________ 剂;
(2)维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有__________ 性;
(3)某同学要检验Fe3+,向溶液中加入_________________ (写化学式)溶液变成红色.要除去FeCl3溶液中少量的氯化亚铁,可行的办法是 _________________ (填字母).
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式________________ ;
(4)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式_____________ ;
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+
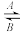 Fe3+.在过程A中,Fe2+作
Fe3+.在过程A中,Fe2+作(2)维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有
(3)某同学要检验Fe3+,向溶液中加入
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式
(4)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】Ⅰ.请回答:
(1)将硫化钠溶液与氯化铝溶液混合,有白色沉淀和气体生成,但此沉淀不是硫化铝。写出该反应的离子反应方程式:__________________________ 。
(2)将NH3通过灼热的CuO,有无色无味的难溶于水的气体生成,写出该反应的化学方程式:__________________________________ 。
(3)CoCl2常用作多彩水泥的添加剂,可用钴的某种氧化物与盐酸反应制备(其中Co的化合价为+2、+3)。现取适量这种钴的氧化物,可与480 mL 5 mol·L-1盐酸恰好完全反应,得到CoCl2溶液和6.72 L黄绿色气体(标准状况)。则该反应的化学反应方程式为______________________ 。
Ⅱ.下表给出五种元素的相关信息,其中A、B、C、D为短周期元素。根据以下信息填空:
(4)C与A形成的某一化合物能和C与B形成的另一无色化合物(这两种化合物分子中原子个数比皆为1∶2)一起用作火箭助推剂,两者发生反应生成无毒物质,写出上述化学反应方程式:_________________ 。
(5)化合物X是元素D的最高价氧化物的水化物,X在水中的电离方程为_____________ ;常温下,E的单质与化合物X稀溶液反应生成盐Y,Y的化学式是___________ 。化合物Z仅由元素D和E组成, Z+H2O+O2→X+Y,产物中n(X):n(Y)=1:1,写出并配平上述方程式:______________________ 。
(6)盐Y受强热会发生分解反应,其气体产物由元素D的氧化物组成,请设计一个可行的定性实验,验证其气体产物中所含元素D的氧化物的组成____________________ 。
(1)将硫化钠溶液与氯化铝溶液混合,有白色沉淀和气体生成,但此沉淀不是硫化铝。写出该反应的离子反应方程式:
(2)将NH3通过灼热的CuO,有无色无味的难溶于水的气体生成,写出该反应的化学方程式:
(3)CoCl2常用作多彩水泥的添加剂,可用钴的某种氧化物与盐酸反应制备(其中Co的化合价为+2、+3)。现取适量这种钴的氧化物,可与480 mL 5 mol·L-1盐酸恰好完全反应,得到CoCl2溶液和6.72 L黄绿色气体(标准状况)。则该反应的化学反应方程式为
Ⅱ.下表给出五种元素的相关信息,其中A、B、C、D为短周期元素。根据以下信息填空:
| 元素 | 相关信息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化。该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 它在地壳中储量丰富,是人体不可缺少的微量元素之一。其单质为银白色固体,是工农业生产中不可或缺的金属材料,常用于机械制备、建筑等行业 |
(4)C与A形成的某一化合物能和C与B形成的另一无色化合物(这两种化合物分子中原子个数比皆为1∶2)一起用作火箭助推剂,两者发生反应生成无毒物质,写出上述化学反应方程式:
(5)化合物X是元素D的最高价氧化物的水化物,X在水中的电离方程为
(6)盐Y受强热会发生分解反应,其气体产物由元素D的氧化物组成,请设计一个可行的定性实验,验证其气体产物中所含元素D的氧化物的组成
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】在100mL稀HNO3和稀H2SO4组成的混合溶液中,两种酸的物质的量浓度之和为0.4mol•L-1。向该溶液中加入足量的铜粉后加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为_____ (反应前后溶液体积变化忽略不计)。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】氨和硝酸都是重要的化学品。
(1)画出采用氨催化氧化法合成硝酸的反应原理流程图:(要求注明试剂、反应条件)___
(示例: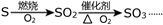 )
)
(2)向饱和氯化钠和浓氨水的混合溶液中通入过量CO2从而析出NaHCO3晶体,是侯氏制碱法的关键步骤,用一个化学方程式表示该反应原理_________________________________ 。在0.1 mol/L的稀氨水中,下列式子成立的是____________ 。
(3)A是中学化学常见气体,打开装有A的集气瓶,瓶口出现白雾,将A与氨气混合,立即出现大量白烟,生成物质B,则A的分子式为_________ ,物质B中所含的化学键类型有____________ 。
(4)将6.4 g铜粉投入一定量的浓硝酸中,铜完全溶解,产生标准状况下的混合气体3.36 L,其中两种成分气体的体积比为__________ ,反应中总共消耗的硝酸_______________ mol。
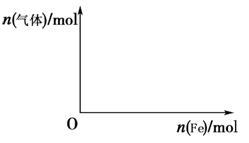
(5)向含4 mol HNO3的稀溶液中,逐渐加入铁粉至过量。假设生成的气体只有一种,请在坐标系中画出n(气体)随n(Fe)变化的示意图,并标出n(气体)的最大值_______ 。
(6)氨气和硝酸生产的氮肥硝酸铵受热或受撞击容易分解,若分解时只生成两种氧化物,写出该反应的化学方程式_________________________ 。
(1)画出采用氨催化氧化法合成硝酸的反应原理流程图:(要求注明试剂、反应条件)
(示例:
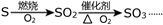 )
)(2)向饱和氯化钠和浓氨水的混合溶液中通入过量CO2从而析出NaHCO3晶体,是侯氏制碱法的关键步骤,用一个化学方程式表示该反应原理
| A.c(NH3·H2O) + c(NH3) + c(NH4+) =0.1 mol/L |
| B.c(NH3·H2O) > c(NH3) + c(NH4+) |
| C.c(H+) > c(OH-) |
| D.c(NH4+) + c(H+) = c(OH-) |
(3)A是中学化学常见气体,打开装有A的集气瓶,瓶口出现白雾,将A与氨气混合,立即出现大量白烟,生成物质B,则A的分子式为
(4)将6.4 g铜粉投入一定量的浓硝酸中,铜完全溶解,产生标准状况下的混合气体3.36 L,其中两种成分气体的体积比为
(5)向含4 mol HNO3的稀溶液中,逐渐加入铁粉至过量。假设生成的气体只有一种,请在坐标系中画出n(气体)随n(Fe)变化的示意图,并标出n(气体)的最大值

(6)氨气和硝酸生产的氮肥硝酸铵受热或受撞击容易分解,若分解时只生成两种氧化物,写出该反应的化学方程式
您最近一年使用:0次



