回答下列问题
(1)目前已开发出用电解法制取ClO2的新工艺。
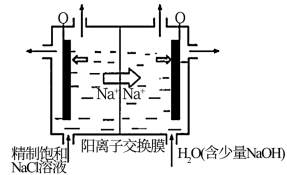
① 图中用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为_______ 。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为_______ mol。
(2)某研究性学习小组根据反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4 + 8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为 1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。
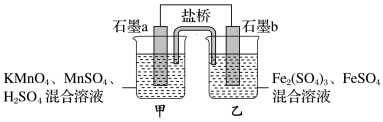
回答下列问题:
③ 此原电池的正极是石墨_______ (填“a”或“b”)。
④电池工作时,盐桥中的SO 移向
移向_______ (填“甲”或“乙”)烧杯。
⑤ 甲烧杯中的电极反应式为_______ 。
⑥ 若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为_______ mol。
(1)目前已开发出用电解法制取ClO2的新工艺。

① 图中用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为
(2)某研究性学习小组根据反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4 + 8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为 1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。

回答下列问题:
③ 此原电池的正极是石墨
④电池工作时,盐桥中的SO
 移向
移向⑤ 甲烧杯中的电极反应式为
⑥ 若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为
更新时间:2018-01-19 20:30:47
|
相似题推荐
【推荐1】使用可再生能源,如太阳能、潮汐能等产生的电能,通过电化学的方式将二氧化碳转化为高附加值的化学产品,如甲烷、乙烯、乙醇等是一种非常有前景的课题。
请回答下列问题:
(1)已知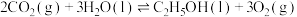
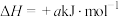 ,则
,则 的摩尔燃烧焓(
的摩尔燃烧焓( )为
)为____________ 。若已知 的摩尔燃烧焓(
的摩尔燃烧焓( )为
)为 ,
, 转化为乙醇的原理为
转化为乙醇的原理为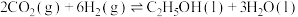

__________  (用含a、b的代数式表示)。
(用含a、b的代数式表示)。
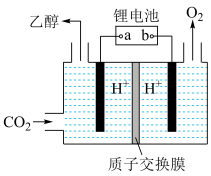
(2)以锂电池为电源,其电池总反应为 ,可将
,可将 转化为乙醇,其原理如图所示,电解池所用电极材料均为惰性电极,每消耗32g
转化为乙醇,其原理如图所示,电解池所用电极材料均为惰性电极,每消耗32g ,理论上会生成标准状况下
,理论上会生成标准状况下 的体积为
的体积为___________ L,装置中产生乙醇的电极反应式为__________________ ,若给锂电池充电,锂电池阳极的电极反应式为__________ 。
(3)若采用乙醇燃料电池作为电源探究氢氧化钾的制备和粗铜的精炼,装置如图所示。

①甲装置中左侧 电极的电极反应式为
电极的电极反应式为___________________ ,若9.2g乙醇参与反应,乙装置中铁电极上产生___________  气体。
气体。
②乙装置中X为阳离子交换膜,已知饱和氯化钾溶液中含有的溶质为1 ,若收集到气体的物质的量之比为3∶2,则乙装置中碳电极上产生气体的质量为
,若收集到气体的物质的量之比为3∶2,则乙装置中碳电极上产生气体的质量为___________ g。
请回答下列问题:
(1)已知
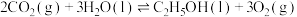
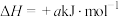 ,则
,则 的摩尔燃烧焓(
的摩尔燃烧焓( )为
)为 的摩尔燃烧焓(
的摩尔燃烧焓( )为
)为 ,
, 转化为乙醇的原理为
转化为乙醇的原理为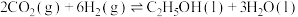

 (用含a、b的代数式表示)。
(用含a、b的代数式表示)。(2)以锂电池为电源,其电池总反应为
 ,可将
,可将 转化为乙醇,其原理如图所示,电解池所用电极材料均为惰性电极,每消耗32g
转化为乙醇,其原理如图所示,电解池所用电极材料均为惰性电极,每消耗32g ,理论上会生成标准状况下
,理论上会生成标准状况下 的体积为
的体积为
(3)若采用乙醇燃料电池作为电源探究氢氧化钾的制备和粗铜的精炼,装置如图所示。

①甲装置中左侧
 电极的电极反应式为
电极的电极反应式为 气体。
气体。②乙装置中X为阳离子交换膜,已知饱和氯化钾溶液中含有的溶质为1
 ,若收集到气体的物质的量之比为3∶2,则乙装置中碳电极上产生气体的质量为
,若收集到气体的物质的量之比为3∶2,则乙装置中碳电极上产生气体的质量为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】氨是重要的无机化工产品之一,在国民经济中占有重要地位。请回答下列问题:
(1)已知几种共价键的键能如下表:
则氨气发生分解反应2NH3(g) N2(g)+3H2(g)的ΔH为
N2(g)+3H2(g)的ΔH为_______ kJ·mol-1(用含a、b、c的代数式表示)。
(2)已知:2NH3·H2O(aq)+H2SO4(aq)=(NH4)2SO4(aq)+2H2O(l) ΔH=-24.2 kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.5 kJ·mol-1,则:NH3·H2O(aq) NH
NH (aq)+OH-(aq)的ΔH为
(aq)+OH-(aq)的ΔH为_______ kJ·mol-1。
(3)目前合成氨最主要的途径是1913年创立的传统的热催化Haber−Bosch过程(N2+3H2 2NH3),该反应需要高温高压苛刻条件,消耗大量化石能源,经过积极探索,科学家研制出Ti-H-Fe双温区催化剂(Ti-H区与Fe区温差可超过100℃)。其反应历程如图,吸附在催化剂表面的物种用“*”标注。
2NH3),该反应需要高温高压苛刻条件,消耗大量化石能源,经过积极探索,科学家研制出Ti-H-Fe双温区催化剂(Ti-H区与Fe区温差可超过100℃)。其反应历程如图,吸附在催化剂表面的物种用“*”标注。
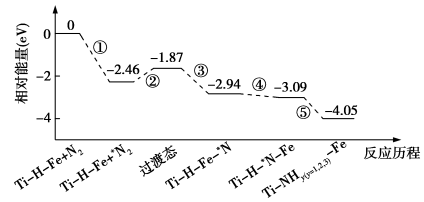
试分析:_______ 区是高温区(填“Fe”或“Ti-H”);高温区的反应历程有_______ (填序号),N原子的传递发生在第_______ 步(填序号),使用Ti-H-Fe双温区催化剂_______ 改变合成氨的反应热(填“能”或“不能”)。
(4)科研人员发现利用低温固体质子导体作电解质,催化合成NH3,与传统的热催化合成氨相比,催化效率较高。其合成原理如图所示。
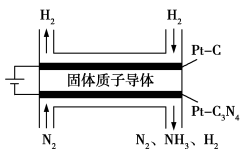
①Pt−C3N4是_______ (填电极名称),电极反应式为_______ 。
②实验过程中发现,其他条件不变时,逐渐增大电压,氨生成速率加快,当电压高于1.2eV时,氨生成速率下降,其可能的原因是_______ 。(用电极反应式表示)
(1)已知几种共价键的键能如下表:
| 化学键 | N≡N | H—H | N—H |
| 键能/kJ·mol-1 | a | b | c |
则氨气发生分解反应2NH3(g)
 N2(g)+3H2(g)的ΔH为
N2(g)+3H2(g)的ΔH为(2)已知:2NH3·H2O(aq)+H2SO4(aq)=(NH4)2SO4(aq)+2H2O(l) ΔH=-24.2 kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.5 kJ·mol-1,则:NH3·H2O(aq)
 NH
NH (aq)+OH-(aq)的ΔH为
(aq)+OH-(aq)的ΔH为(3)目前合成氨最主要的途径是1913年创立的传统的热催化Haber−Bosch过程(N2+3H2
 2NH3),该反应需要高温高压苛刻条件,消耗大量化石能源,经过积极探索,科学家研制出Ti-H-Fe双温区催化剂(Ti-H区与Fe区温差可超过100℃)。其反应历程如图,吸附在催化剂表面的物种用“*”标注。
2NH3),该反应需要高温高压苛刻条件,消耗大量化石能源,经过积极探索,科学家研制出Ti-H-Fe双温区催化剂(Ti-H区与Fe区温差可超过100℃)。其反应历程如图,吸附在催化剂表面的物种用“*”标注。
试分析:
(4)科研人员发现利用低温固体质子导体作电解质,催化合成NH3,与传统的热催化合成氨相比,催化效率较高。其合成原理如图所示。

①Pt−C3N4是
②实验过程中发现,其他条件不变时,逐渐增大电压,氨生成速率加快,当电压高于1.2eV时,氨生成速率下降,其可能的原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】一种从废电池正极材料(含铝箔、LiCoO2、Fe2O3及少量不溶于酸碱的导电剂中回收各种金属的工艺流程如图:
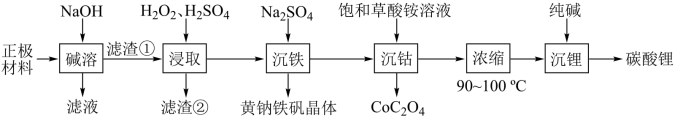
已知:①黄钠铁矾晶体颗粒粗大,沉淀速度快,易于过滤。
②钴酸锂难溶于水,碳酸锂的溶解度随温度升高而降低。
③Ksp(CoC2O4)=6.3×10-8,Ksp[Co(OH)2]=6.3×10-4。
回答下列问题:
(1)为了提高“碱溶”效率,可以采取的措施是___ (写出一条即可)。
(2)“浸取”时有无色气体产生,发生反应的离子方程式为___ 。
(3)“沉钴”时采用饱和草酸铵溶液将钴元素转化为CoC2O4,与草酸钠溶液相比效果更好,原因是___ 。
(4)“沉锂”后得到碳酸锂固体的实验操作为___ 。
(5)“沉铁”时所得黄钠铁矾的化学式可表示为NaxFey(SO4)m(OH)n。采用滴定法测定黄钠铁矾样品的组成,实验步骤如下:
I.称取4.850g样品,加盐酸完全溶解后,配成100.00mL溶液。
II.量取25.00mL溶液,加入足量的KI,用0.2500mol·L-1Na2S2O3溶液进行滴定至终点(I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00mLNa2S2O3溶液。
III.另取25.00mL溶液,加入足量BaCl2溶液,充分反应后过滤、洗涤、干燥,得到沉淀1.165g。
用Na2S2O3溶液进行滴定时,使用的指示剂为___ ;黄钠铁矾的化学式为___ 。
(6)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。
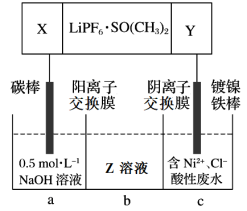
①电极X的反应材料是___ (填化学式);中间隔室b可以得到的主要物质Z是___ (填化式)。
②电解总反应的离子方程式为___ 。
已知F=96500C/mol,Q=It=n(e-)·F。若电池工作tmin,维持电流强度为IA,理论回收Ni___ g(写出计算表达式即可)。

已知:①黄钠铁矾晶体颗粒粗大,沉淀速度快,易于过滤。
②钴酸锂难溶于水,碳酸锂的溶解度随温度升高而降低。
③Ksp(CoC2O4)=6.3×10-8,Ksp[Co(OH)2]=6.3×10-4。
回答下列问题:
(1)为了提高“碱溶”效率,可以采取的措施是
(2)“浸取”时有无色气体产生,发生反应的离子方程式为
(3)“沉钴”时采用饱和草酸铵溶液将钴元素转化为CoC2O4,与草酸钠溶液相比效果更好,原因是
(4)“沉锂”后得到碳酸锂固体的实验操作为
(5)“沉铁”时所得黄钠铁矾的化学式可表示为NaxFey(SO4)m(OH)n。采用滴定法测定黄钠铁矾样品的组成,实验步骤如下:
I.称取4.850g样品,加盐酸完全溶解后,配成100.00mL溶液。
II.量取25.00mL溶液,加入足量的KI,用0.2500mol·L-1Na2S2O3溶液进行滴定至终点(I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00mLNa2S2O3溶液。
III.另取25.00mL溶液,加入足量BaCl2溶液,充分反应后过滤、洗涤、干燥,得到沉淀1.165g。
用Na2S2O3溶液进行滴定时,使用的指示剂为
(6)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。

①电极X的反应材料是
②电解总反应的离子方程式为
已知F=96500C/mol,Q=It=n(e-)·F。若电池工作tmin,维持电流强度为IA,理论回收Ni
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】应用电化学原理,回答问题。
(1)现有甲、乙、丙三个电化学装置。
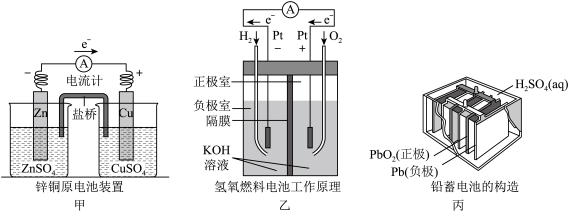
①甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中Cl-移动的方向是_____ (填左或右)。
②乙中正极反应式为_____ ;若将H2换成CH4,则负极反应式为_____ 。
③丙中正极的电极反应式为_____ 。
(2)应用原电池反应可以探究氧化还原反应进行的方向和程度。按下面丁图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:
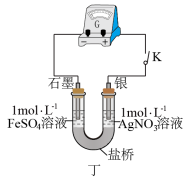
i.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ii.随后向U型管左侧逐渐加入浓Fe2(SO4)3溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
综合实验i、ii的现象,得出Ag+和Fe2+反应的离子方程式是_____ 。
(3)差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如戊图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。
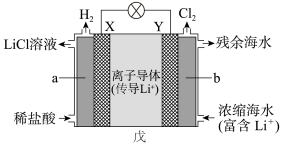
X为_____ 极,Y极生成1molCl2时有_____ molLi+移向_____ (填“X”或“Y”)极。
(1)现有甲、乙、丙三个电化学装置。

①甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中Cl-移动的方向是
②乙中正极反应式为
③丙中正极的电极反应式为
(2)应用原电池反应可以探究氧化还原反应进行的方向和程度。按下面丁图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:

i.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ii.随后向U型管左侧逐渐加入浓Fe2(SO4)3溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
综合实验i、ii的现象,得出Ag+和Fe2+反应的离子方程式是
(3)差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如戊图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。

X为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】某油脂厂废弃的催化剂主要含有金属Pb、Al、Fe及其氧化物,采用如图工艺流程回收其中的铝并制备绿矾晶体( )。
)。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)废催化剂“酸浸”前,先用热的 溶液除去表面的油污,然后粉碎,用离子方程式表示
溶液除去表面的油污,然后粉碎,用离子方程式表示 溶液显碱性的原因:
溶液显碱性的原因:_______ 。粉碎的主要目的为_______ 。
(2)滤渣1的主要成分为_______ (填化学式),加入M发生反应的离子方程式为_______ 。
(3)“沉铝”时pH应该控制的范围为_______ ,若“沉铝”时用 溶液代替NaOH溶液,则滤渣2为碱式碳酸铝[
溶液代替NaOH溶液,则滤渣2为碱式碳酸铝[ ],同时有
],同时有 逸出,写出该反应的离子方程式:
逸出,写出该反应的离子方程式:_______ 。
(4)“控制pH”后从溶液中得到绿矾晶体,包含的操作是_______ 、过滤、洗涤及干燥。
(5)铝电池有广泛应用前景,一种可充放电的铝离子电池工作原理如图所示,电解质为 离子液体,CuS在电池反应后转化为
离子液体,CuS在电池反应后转化为 和
和 。
。

放电时,负极每消耗 ,有
,有_______ g Al溶解。该电池充电时,阳极反应式为_______ 。
 )。
)。
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |
| 开始沉淀时(c=0.01mol/L)的pH | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol/L)的pH | 4.7 | 3.2 | 9.0 |
(1)废催化剂“酸浸”前,先用热的
 溶液除去表面的油污,然后粉碎,用离子方程式表示
溶液除去表面的油污,然后粉碎,用离子方程式表示 溶液显碱性的原因:
溶液显碱性的原因:(2)滤渣1的主要成分为
(3)“沉铝”时pH应该控制的范围为
 溶液代替NaOH溶液,则滤渣2为碱式碳酸铝[
溶液代替NaOH溶液,则滤渣2为碱式碳酸铝[ ],同时有
],同时有 逸出,写出该反应的离子方程式:
逸出,写出该反应的离子方程式:(4)“控制pH”后从溶液中得到绿矾晶体,包含的操作是
(5)铝电池有广泛应用前景,一种可充放电的铝离子电池工作原理如图所示,电解质为
 离子液体,CuS在电池反应后转化为
离子液体,CuS在电池反应后转化为 和
和 。
。
放电时,负极每消耗
 ,有
,有
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】甲醇是重要的基本有机化工原料之一,在化工、医药、轻工、纺织及运输业等方面具有广泛的用途。关于甲醇制备和用途的研究一直是化学工业热门研究方向。
I.煤间接液化法合成甲醇
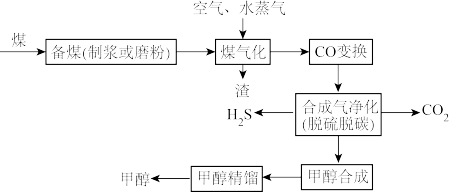
请回答下列问题:
(1)备煤时制浆或磨粉的目的是___________ 。
(2)写出煤气化时有关化学方程式(注明反应条件): ,
,___________ 。
(3)已知:①CO变换反应为: ;②甲醇合成的主要反应为:
;②甲醇合成的主要反应为: ,煤气化后,将部分CO变换成
,煤气化后,将部分CO变换成 的目的是
的目的是___________ 。
(4)下列说法可以表明甲醇合成反应达到化学平衡状态的是___________。
II.甲醇的用途
直接甲醇燃料电池属于低温燃料电池,采用质子交换膜做固体电解质。其工作原理如下图所示。

(5)b处通入的是___________ ,正极的电极反应式为___________ 。
(6)工作一段时间后,当6.4g甲醇完全反应生成 时,外电路通过
时,外电路通过___________  。
。
I.煤间接液化法合成甲醇

请回答下列问题:
(1)备煤时制浆或磨粉的目的是
(2)写出煤气化时有关化学方程式(注明反应条件):
 ,
,(3)已知:①CO变换反应为:
 ;②甲醇合成的主要反应为:
;②甲醇合成的主要反应为: ,煤气化后,将部分CO变换成
,煤气化后,将部分CO变换成 的目的是
的目的是(4)下列说法可以表明甲醇合成反应达到化学平衡状态的是___________。
A.单位时间内消耗 ,同时生成 ,同时生成 | B. 的体积分数不再发生变化 的体积分数不再发生变化 |
C. | D.容器内气体密度不再改变 |
II.甲醇的用途
直接甲醇燃料电池属于低温燃料电池,采用质子交换膜做固体电解质。其工作原理如下图所示。

(5)b处通入的是
(6)工作一段时间后,当6.4g甲醇完全反应生成
 时,外电路通过
时,外电路通过 。
。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】某化学研究性小组采用如下装置(夹持和加热仪器已略去)电解饱和食盐水一段时间,并通过实验测定产物的量来判断饱和食盐水的电离率。饱和食盐水的电解率=(电解的氯化钠质量/总的氯化钠质量)×100%

甲方案:利用甲、乙装置测定饱和食盐水的电解率
(1)若饱和食盐水中滴有酚酞,则电解过程中甲装置中的U形管左端的实验现象为_____ ; 该电解池总反应的化学方程式为_______ ;
(2)若洗气瓶a中盛放的为足量的氢氧化钠溶液,通过测定洗气瓶a在电解前后的质量变化来计算饱和食盐水的电解率,则正确的连接顺序为________ 连______ (填A、B、C、D、E等导管口),则洗气瓶a中发生反应的离子方程式为_______ ;
乙方案:利用甲、丙装置测定饱和食盐水的电解率
(3)对于乙方案,有同学提出有两种方法都可测得饱和食盐水的电解率
Ⅰ.通过测定硬质玻璃管中氧化铜固体前后质量差来计算饱和食盐水的电解率。
Ⅱ.通过测定丙装置中除硬质玻璃管外的某装置前后质量差来计算饱和食盐水的电解率
①一同学认为可以在乙方案方法Ⅱ中的装置中添加一干燥装置防止外界空气中的水蒸气的干扰,则该干燥装置应与______ 口连接(填A、B、C、D、E等导管口)。
②另一同学认为乙方案的方法Ⅰ、Ⅱ测得的实验结论都不正确,你是否同意?_____ (填“同意”或“不同意”)请说明理由 ____ 。
丙方案:只利用甲装置测定饱和食盐水的电解率
(4)若电解150mL饱和食盐水一段时间,测得溶液的pH为14,求饱和食盐水的电解率_______ (保留一位小数,假设电解前后溶液体积不变,饱和食盐水密度约为1.33g/mL,溶解度为36.0g)。

甲方案:利用甲、乙装置测定饱和食盐水的电解率
(1)若饱和食盐水中滴有酚酞,则电解过程中甲装置中的U形管左端的实验现象为
(2)若洗气瓶a中盛放的为足量的氢氧化钠溶液,通过测定洗气瓶a在电解前后的质量变化来计算饱和食盐水的电解率,则正确的连接顺序为
乙方案:利用甲、丙装置测定饱和食盐水的电解率
(3)对于乙方案,有同学提出有两种方法都可测得饱和食盐水的电解率
Ⅰ.通过测定硬质玻璃管中氧化铜固体前后质量差来计算饱和食盐水的电解率。
Ⅱ.通过测定丙装置中除硬质玻璃管外的某装置前后质量差来计算饱和食盐水的电解率
①一同学认为可以在乙方案方法Ⅱ中的装置中添加一干燥装置防止外界空气中的水蒸气的干扰,则该干燥装置应与
②另一同学认为乙方案的方法Ⅰ、Ⅱ测得的实验结论都不正确,你是否同意?
丙方案:只利用甲装置测定饱和食盐水的电解率
(4)若电解150mL饱和食盐水一段时间,测得溶液的pH为14,求饱和食盐水的电解率
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】氮的化合物在生产和生活中广泛存在。请回答下列有关问题:
(1)氯胺(NH2Cl)是一种长效缓释消毒剂,可通过反应NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g)
△H=+12kJ·mol-1来制取。

已知部分化学键的键能如上表所示(假定不同物质中同种化学键的键能一样),则a=______ 。
(2)2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
(a)2NO(g) N2O2(g)(快) Va正=Ka正c2(NO),Va逆=Ka逆c2(N2O2),△H1<0
N2O2(g)(快) Va正=Ka正c2(NO),Va逆=Ka逆c2(N2O2),△H1<0
(b)N2O2(g)+ O2(g)=2N02(g) (慢) Vb正=Kb正c2(N2O2)·c2(O2),Vb逆=Kb逆c2(NO2),△H2<0
①一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,其平衡常数K=
2NO2(g)达到平衡状态,其平衡常数K=______ (用ka正、Ka逆、Kb正、Kb逆表示)。
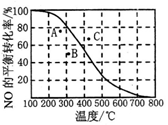
②100KPa时,密闭容器中发生反应2NO(g)+O2(g) 2NO2(g), NO的平衡转化率与温度的关系曲线如右图所示:图中A、B、C三点表示不同温度、压强下达到平衡时NO的转化率,则
2NO2(g), NO的平衡转化率与温度的关系曲线如右图所示:图中A、B、C三点表示不同温度、压强下达到平衡时NO的转化率,则__ 点对应的压强最大,原因是______________ 。
③反应2NO(g)+O2(g) 2NO2(g)在密闭恒容绝热容器中进行,若氧气中混有氮气,容器中还发生了反应:N2(g)+O2(g)
2NO2(g)在密闭恒容绝热容器中进行,若氧气中混有氮气,容器中还发生了反应:N2(g)+O2(g) 2NO(g) △H=+180kJ/mol,则此反应对NO的转化率的影响是
2NO(g) △H=+180kJ/mol,则此反应对NO的转化率的影响是____ (填“增大”、“减小”或“无法判断”)。
④某温度下,反应2NO(g)+O2(g) 2NO2(g)中,在保证O2浓度不变的情况下,增大容器的体积.平衡将
2NO2(g)中,在保证O2浓度不变的情况下,增大容器的体积.平衡将_____ (填“正反应方向”、“逆反应方向”或“不”)称动。判断的依据是_____ 。
(3)工业上可通过电解NO制备NH4NO3,其工作原理如图所示。
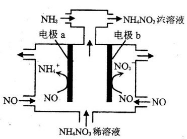
①该装置的阳极是_____ (填“电极a”、“电极b”)。
②电解过程总反应的化学方程式为___________ 。
③若维持电流强度为6A,电解5小时,理论上可制祠NH4NO3的最大质量为_____ g。(已知F=96500C/mol,保留小数点后l位)。
(1)氯胺(NH2Cl)是一种长效缓释消毒剂,可通过反应NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g)
△H=+12kJ·mol-1来制取。

已知部分化学键的键能如上表所示(假定不同物质中同种化学键的键能一样),则a=
(2)2NO(g)+O2(g)
 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:(a)2NO(g)
 N2O2(g)(快) Va正=Ka正c2(NO),Va逆=Ka逆c2(N2O2),△H1<0
N2O2(g)(快) Va正=Ka正c2(NO),Va逆=Ka逆c2(N2O2),△H1<0(b)N2O2(g)+ O2(g)=2N02(g) (慢) Vb正=Kb正c2(N2O2)·c2(O2),Vb逆=Kb逆c2(NO2),△H2<0
①一定温度下,反应2NO(g)+O2(g)
 2NO2(g)达到平衡状态,其平衡常数K=
2NO2(g)达到平衡状态,其平衡常数K=②100KPa时,密闭容器中发生反应2NO(g)+O2(g)
 2NO2(g), NO的平衡转化率与温度的关系曲线如右图所示:图中A、B、C三点表示不同温度、压强下达到平衡时NO的转化率,则
2NO2(g), NO的平衡转化率与温度的关系曲线如右图所示:图中A、B、C三点表示不同温度、压强下达到平衡时NO的转化率,则
③反应2NO(g)+O2(g)
 2NO2(g)在密闭恒容绝热容器中进行,若氧气中混有氮气,容器中还发生了反应:N2(g)+O2(g)
2NO2(g)在密闭恒容绝热容器中进行,若氧气中混有氮气,容器中还发生了反应:N2(g)+O2(g) 2NO(g) △H=+180kJ/mol,则此反应对NO的转化率的影响是
2NO(g) △H=+180kJ/mol,则此反应对NO的转化率的影响是④某温度下,反应2NO(g)+O2(g)
 2NO2(g)中,在保证O2浓度不变的情况下,增大容器的体积.平衡将
2NO2(g)中,在保证O2浓度不变的情况下,增大容器的体积.平衡将(3)工业上可通过电解NO制备NH4NO3,其工作原理如图所示。

①该装置的阳极是
②电解过程总反应的化学方程式为
③若维持电流强度为6A,电解5小时,理论上可制祠NH4NO3的最大质量为
您最近一年使用:0次
【推荐3】 可作大型船舶的绿色燃料,可由CO或
可作大型船舶的绿色燃料,可由CO或 制备。工业上用
制备。工业上用 催化加氢制备
催化加氢制备 的原理如下:
的原理如下:
反应1:
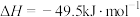
反应2:
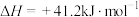
回答下列问题:
(1)反应

___________  。
。
(2)将 和
和 按1∶3通入密闭容器中发生反应1和反应2,分别在1MPa、3MPa、5MPa下改变反应温度,测得
按1∶3通入密闭容器中发生反应1和反应2,分别在1MPa、3MPa、5MPa下改变反应温度,测得 的平衡转化率
的平衡转化率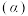 以及生成
以及生成 、CO选择性(S)的变化如图(选择性为目标产物的物质的量在转化的
、CO选择性(S)的变化如图(选择性为目标产物的物质的量在转化的 的总物质的量中的比率)。
的总物质的量中的比率)。 随温度变化趋势的是曲线
随温度变化趋势的是曲线___________ (填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
② ℃时,
℃时, 、
、 、
、 三条曲线接近重合的原因是
三条曲线接近重合的原因是___________ 。
③P点对应的反应2的平衡常数
___________ (保留两位有效数字)。
④T℃时,在催化剂作用下 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为40%。不改变反应时间和温度,一定能提高
的选择性为40%。不改变反应时间和温度,一定能提高 选择性的措施有
选择性的措施有___________ (写出一种即可)。
⑤实际生产中,投料往往在 的基础上适当增大
的基础上适当增大 用量,其目的是
用量,其目的是_____ 。
(3)利用电催化可将 同时转化为多种燃料,装置如图所示。铜电极上产生HCOOH的电极反应式为
同时转化为多种燃料,装置如图所示。铜电极上产生HCOOH的电极反应式为________ 。若用甲醇燃料电池为此电解池供电,生成138gHCOOH时,理论上需要消耗________ g甲醇。
 可作大型船舶的绿色燃料,可由CO或
可作大型船舶的绿色燃料,可由CO或 制备。工业上用
制备。工业上用 催化加氢制备
催化加氢制备 的原理如下:
的原理如下:反应1:

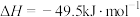
反应2:

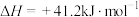
回答下列问题:
(1)反应


 。
。(2)将
 和
和 按1∶3通入密闭容器中发生反应1和反应2,分别在1MPa、3MPa、5MPa下改变反应温度,测得
按1∶3通入密闭容器中发生反应1和反应2,分别在1MPa、3MPa、5MPa下改变反应温度,测得 的平衡转化率
的平衡转化率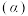 以及生成
以及生成 、CO选择性(S)的变化如图(选择性为目标产物的物质的量在转化的
、CO选择性(S)的变化如图(选择性为目标产物的物质的量在转化的 的总物质的量中的比率)。
的总物质的量中的比率)。
 随温度变化趋势的是曲线
随温度变化趋势的是曲线 ”、“
”、“ ”或“
”或“ ”)。
”)。②
 ℃时,
℃时, 、
、 、
、 三条曲线接近重合的原因是
三条曲线接近重合的原因是③P点对应的反应2的平衡常数

④T℃时,在催化剂作用下
 与
与 反应一段时间后,测得
反应一段时间后,测得 的选择性为40%。不改变反应时间和温度,一定能提高
的选择性为40%。不改变反应时间和温度,一定能提高 选择性的措施有
选择性的措施有⑤实际生产中,投料往往在
 的基础上适当增大
的基础上适当增大 用量,其目的是
用量,其目的是(3)利用电催化可将
 同时转化为多种燃料,装置如图所示。铜电极上产生HCOOH的电极反应式为
同时转化为多种燃料,装置如图所示。铜电极上产生HCOOH的电极反应式为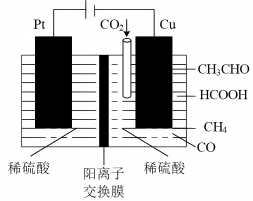
您最近一年使用:0次



