下列叙述正确的是( )
| A.△H>0的化学反应一定不能自发进行 |
B.反应2NO2(g) N2O4(l)的熵(体系的混乱度)增大(即△S>0) N2O4(l)的熵(体系的混乱度)增大(即△S>0) |
| C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 |
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s) Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 |
更新时间:2018-01-27 12:31:58
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】我国学者结合实验与计算机模拟结果,研究了均相NO-CO的反应历程,该反应经历了I、II、III三个过渡态。下图中显示的是反应路径中每一个阶段内各驻点的能量相对于此阶段内反应物能量的能量之差,则下列说法中正确的是


A. 比 比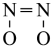 更容易与CO发生反应 更容易与CO发生反应 |
B.  |
| C.整个反应分为三个基元反应阶段,其中第二个反应阶段活化能最大 |
| D.其他条件不变,增大压强或使用催化剂均可以增大反应速率同时提高反应物的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】乙烯在酸催化下与水制乙醇的反应机理及反应进程中能量的变化如图甲、乙所示.下列叙述错误的是
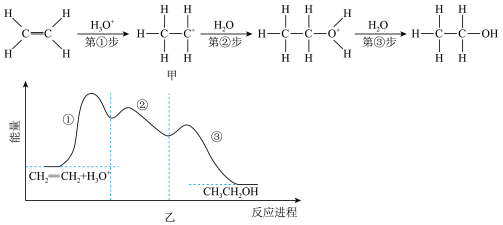

| A.乙烯中既含有极性共价键又含有非极性共价键 |
| B.第①步反应的活化能最大 |
| C.酸催化剂加快了化学反应速率,降低了该反应的反应热 |
D.第③步反应为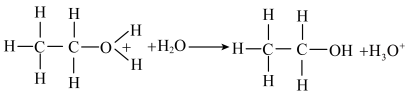 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列反应的焓变和熵变与冰融化为水的变化一致的是
A.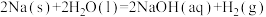 |
B.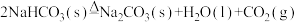 |
C.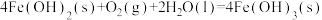 |
D.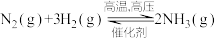 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学反应进行的方向和限度是化学反应原理所要研究的两个重要问题,下列有关化学反应进行的方向和限度的说法中正确的是
A.反应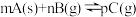 ,达到平衡时增加A的物质的量,平衡不移动,是因为A是固体,而分子间的碰撞只能在固体表面进行,固体的物质的量浓度对平衡没有影响 ,达到平衡时增加A的物质的量,平衡不移动,是因为A是固体,而分子间的碰撞只能在固体表面进行,固体的物质的量浓度对平衡没有影响 |
B.将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中,在恒定温度下使其分解达到平衡: , , 的体积分数不变可以作为平衡判断的依据 的体积分数不变可以作为平衡判断的依据 |
C.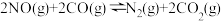 在常温下能自发进行,则该反应的 在常温下能自发进行,则该反应的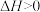 |
D.对于反应 ,起始充入等物质的量的A和B,达到平衡时A的体积分数为 ,起始充入等物质的量的A和B,达到平衡时A的体积分数为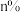 ,此时若给体系加压则A的体积分数一定会发生改变 ,此时若给体系加压则A的体积分数一定会发生改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
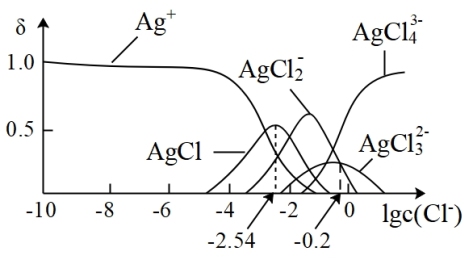
【推荐1】湿法提银工艺中,浸出的Ag+需加入Cl-进行沉淀。25℃时,平衡体系中含Ag微粒的分布系数δ[如δ(AgCl2-)=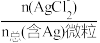 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgC1)]=-9.75。下列叙述正确的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgC1)]=-9.75。下列叙述正确的是
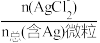 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgC1)]=-9.75。下列叙述正确的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgC1)]=-9.75。下列叙述正确的是
| A.沉淀最彻底时,溶液中c(Ag+)=10-7.21mol/L |
| B.AgCl溶解程度随c(Cl-)增大而不断减小 |
C.当c(Cl-)=10-2mol·L-1时,溶液中c(AgCl )>c(AgC1 )>c(AgC1 )>c(Ag+) )>c(Ag+) |
D.25℃时,AgCl +Cl- +Cl- AgCl AgCl 的平衡常数K=10-0.2 的平衡常数K=10-0.2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25 ℃时,在氢氧化镁悬浊液中存在沉淀溶解平衡:Mg(OH)2(s) Mg2+(aq)+2OH−(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20。下列说法错误的是
Mg2+(aq)+2OH−(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20。下列说法错误的是
 Mg2+(aq)+2OH−(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20。下列说法错误的是
Mg2+(aq)+2OH−(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10−11,Ksp[Cu(OH)2]=2.2×10−20。下列说法错误的是| A.若向Mg(OH)2悬浊液中加入少量NH4Cl(s),c(Mg2+)会增大 |
| B.若向Mg(OH)2悬浊液中滴加CuSO4溶液,沉淀将由白色逐渐变为蓝色 |
| C.若向Mg(OH)2悬浊液中加入适量蒸馏水,Ksp保持不变,故上述平衡不发生移动 |
| D.若向Mg(OH)2悬浊液中加入少量Na2S(s),固体质量将增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知Ksp(AgCl)=1.8×10-10。向盛有0.1 mol/L AgNO3溶液的试管中滴加等体积0.1 mol/L NaCl溶液,静置沉降,取上层清液和下层悬浊液分别进行实验。下列判断正确的是
| A.上层清液为AgCl的饱和溶液 |
| B.向清液中滴加0.1 mol/L AgNO3溶液,c(Cl-)不变 |
| C.向悬浊液中滴加0.1 mol/L KI溶液,不会有明显变化 |
| D.向悬浊液中加入适量浓氨水,混合液变澄清,说明AgCl可溶于强碱 |
您最近一年使用:0次

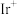 可消除大气污染物
可消除大气污染物 ,反应过程中相对能量变化如图所示。下列说法错误的是(
,反应过程中相对能量变化如图所示。下列说法错误的是(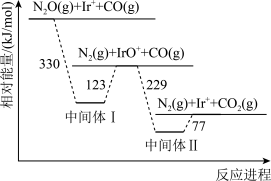
 为放热反应
为放热反应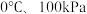 的室内存放,它会不会变成灰锡而不能再继续使用?已知:在
的室内存放,它会不会变成灰锡而不能再继续使用?已知:在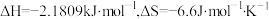 。
。

