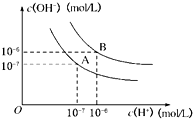
水的电离平衡曲线如图所示:
(1)若A点、B点分别表示25℃和100℃时水的电离平衡时离子的浓度,则表示25℃的是______ (填“A”或“B”),100℃时水的离子积为__________ 。
(2)100℃,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,若所得混合溶液pH=7,则NaOH溶液与盐酸溶液的体积比为_____ 。
(3)氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001mol/L酸性KMnO4和未知浓度的无色NaHSO3溶液,反应离子方程式是2MnO4-+ 5HSO3- + H+=2Mn2+ + 5SO42- + 3H2O 填空回答问题:

①滴定时,将酸性KMnO4标准液装在图中的___________ (填“甲”或“乙”) 滴定管中。
②本实验___________ (填“需要”或“不需要”)指示剂。
③下列操作会使测定结果偏高的是_____
A.锥形瓶洗净后还留有蒸馏水
B.部分KMnO4溶液滴到锥形瓶外
C.盛装KMnO4溶液的滴定管滴定前读数正确,滴定后仰视读数
(1)若A点、B点分别表示25℃和100℃时水的电离平衡时离子的浓度,则表示25℃的是
(2)100℃,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,若所得混合溶液pH=7,则NaOH溶液与盐酸溶液的体积比为

(3)氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.001mol/L酸性KMnO4和未知浓度的无色NaHSO3溶液,反应离子方程式是2MnO4-+ 5HSO3- + H+=2Mn2+ + 5SO42- + 3H2O 填空回答问题:

①滴定时,将酸性KMnO4标准液装在图中的
②本实验
③下列操作会使测定结果偏高的是
A.锥形瓶洗净后还留有蒸馏水
B.部分KMnO4溶液滴到锥形瓶外
C.盛装KMnO4溶液的滴定管滴定前读数正确,滴定后仰视读数
更新时间:2018-02-02 16:23:51
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】化学与社会、生产、生活息息相关,请回答下列问题:
(1)用热的纯碱水刷洗餐具上的油污,试解释原因___________ (用必要的语言和离子方程式作答)。
(2)已知:①2Zn(s)+O2(g)=2ZnO(s) ΔH=-702.2 kJ·mol-1
②2Hg(l)+O2(g)=2HgO(s) ΔH=-181.4 kJ·mol-1。
则Zn(s)+HgO(s)=ZnO(s)+Hg(l) ΔH=___________ kJ·mol-1
(3)常温下,V1 mL pH=1的盐酸与V2 mL 0.05 mol·L-1Ba(OH)2溶液混合,所得混合溶液的pH=2,则V1︰V2等于___________ (忽略混合前后溶液体积变化)。
(4)某反应过程中的能量变化如下图所示:
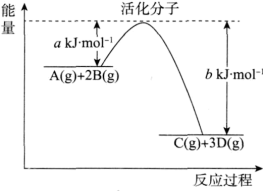
①该反应的ΔH___________ (填“>”或“<”)0。
②该反应的热化学方程式为___________ 。
③加入催化剂,b___________ (填“增大”“减小”或“不变”,下同),ΔH______ 。
(1)用热的纯碱水刷洗餐具上的油污,试解释原因
(2)已知:①2Zn(s)+O2(g)=2ZnO(s) ΔH=-702.2 kJ·mol-1
②2Hg(l)+O2(g)=2HgO(s) ΔH=-181.4 kJ·mol-1。
则Zn(s)+HgO(s)=ZnO(s)+Hg(l) ΔH=
(3)常温下,V1 mL pH=1的盐酸与V2 mL 0.05 mol·L-1Ba(OH)2溶液混合,所得混合溶液的pH=2,则V1︰V2等于
(4)某反应过程中的能量变化如下图所示:

①该反应的ΔH
②该反应的热化学方程式为
③加入催化剂,b
您最近一年使用:0次
【推荐2】回答下列问题:
(1)航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用 、
、 、CO、
、CO、 等可燃物质与
等可燃物质与 一起构成的电池装置。它可直接将化学能转化为电能,氢氧燃料电池以KOH溶液为电解质,其总反应的化学方程式为
一起构成的电池装置。它可直接将化学能转化为电能,氢氧燃料电池以KOH溶液为电解质,其总反应的化学方程式为 。
。
①负极上的电极反应为___________ 。
②消耗标准状况下的5.6L 时,有
时,有___________ mol电子发生转移。
③工作过程中时,溶液的
___________ (填“增大”、“减小”或“不变”)。
(2)①已知:
 则反应
则反应
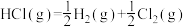 的
的 为
为___________ 。
②由 和
和 合成1mol
合成1mol 时可放出46.2kJ/mol的热量。从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436.0kJ/mol,则N-H键的键能是
时可放出46.2kJ/mol的热量。从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436.0kJ/mol,则N-H键的键能是___________ kJ/mol。
③黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:


已知碳的燃烧热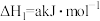

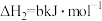


则 为
为___________ kJ/mol。
④火箭推进器中盛有强还原剂液态肼( )和强氧化剂液态过氧化氢。当把0.4mol液态肼和0.8mol
)和强氧化剂液态过氧化氢。当把0.4mol液态肼和0.8mol 混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量)。反应的热化学方程式为
混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量)。反应的热化学方程式为___________ 。
(3)某温度( ℃)时,测得
℃)时,测得 的NaOH溶液的pH=13,请回答下列问题:
的NaOH溶液的pH=13,请回答下列问题:
①该温度下水的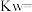
___________ 。
②此温度下,将 的NaOH溶液
的NaOH溶液 与
与 的
的 溶液
溶液 混合(忽略体积变化),若所得混合液为中性,且
混合(忽略体积变化),若所得混合液为中性,且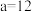 ,
,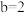 ,则
,则
___________ 。
(4)已知25℃时 ,为除去某食盐溶液中的
,为除去某食盐溶液中的 ,可用NaOH为除杂试剂,当控制溶液pH=12时,可确保
,可用NaOH为除杂试剂,当控制溶液pH=12时,可确保 除尽,此时溶液中
除尽,此时溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(1)航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用
 、
、 、CO、
、CO、 等可燃物质与
等可燃物质与 一起构成的电池装置。它可直接将化学能转化为电能,氢氧燃料电池以KOH溶液为电解质,其总反应的化学方程式为
一起构成的电池装置。它可直接将化学能转化为电能,氢氧燃料电池以KOH溶液为电解质,其总反应的化学方程式为 。
。①负极上的电极反应为
②消耗标准状况下的5.6L
 时,有
时,有③工作过程中时,溶液的

(2)①已知:

 则反应
则反应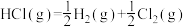 的
的 为
为②由
 和
和 合成1mol
合成1mol 时可放出46.2kJ/mol的热量。从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436.0kJ/mol,则N-H键的键能是
时可放出46.2kJ/mol的热量。从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436.0kJ/mol,则N-H键的键能是③黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:


已知碳的燃烧热
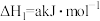

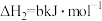


则
 为
为④火箭推进器中盛有强还原剂液态肼(
 )和强氧化剂液态过氧化氢。当把0.4mol液态肼和0.8mol
)和强氧化剂液态过氧化氢。当把0.4mol液态肼和0.8mol 混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量)。反应的热化学方程式为
混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量)。反应的热化学方程式为(3)某温度(
 ℃)时,测得
℃)时,测得 的NaOH溶液的pH=13,请回答下列问题:
的NaOH溶液的pH=13,请回答下列问题:①该温度下水的
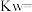
②此温度下,将
 的NaOH溶液
的NaOH溶液 与
与 的
的 溶液
溶液 混合(忽略体积变化),若所得混合液为中性,且
混合(忽略体积变化),若所得混合液为中性,且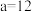 ,
,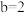 ,则
,则
(4)已知25℃时
 ,为除去某食盐溶液中的
,为除去某食盐溶液中的 ,可用NaOH为除杂试剂,当控制溶液pH=12时,可确保
,可用NaOH为除杂试剂,当控制溶液pH=12时,可确保 除尽,此时溶液中
除尽,此时溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】生活中常用到酸和碱,已知常温下, 的
的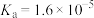 ,
, 的
的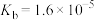 。回答下列问题:
。回答下列问题:
(1)冰醋酸加水稀释过程中溶液的导电能力变化趋势如图所示。

①加水前冰醋酸的导电能力几乎为零,原因是_______ 。
②a、b、c三点中水的电离程度最小的是_______ (用a、b、c表示)。
(2)体积均为100mL、pH均为2的 溶液与一元弱酸HX溶液,分别加水稀释过程中pH与加入水的体积的关系如图所示,则HX的电离平衡常数
溶液与一元弱酸HX溶液,分别加水稀释过程中pH与加入水的体积的关系如图所示,则HX的电离平衡常数_______ (填“大于”“小于”或“等于”) 的电离平衡常数,理由是
的电离平衡常数,理由是_______ 。

(3)常温下,在 的
的 溶液和
溶液和 的
的 溶液中:
溶液中:
① 的
的 溶液中
溶液中 约为
约为_______  (保留两位有效数字)。
(保留两位有效数字)。
②常温下, 溶液的
溶液的
_______ (填具体数字)。
(4)某温度时,测得 溶液的pH为11,在此温度下,将
溶液的pH为11,在此温度下,将 的NaOH溶液
的NaOH溶液 与
与 的硫酸
的硫酸 混合,若所得混合溶液为中性,则
混合,若所得混合溶液为中性,则
_______ (写比值)。
 的
的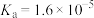 ,
, 的
的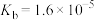 。回答下列问题:
。回答下列问题:(1)冰醋酸加水稀释过程中溶液的导电能力变化趋势如图所示。

①加水前冰醋酸的导电能力几乎为零,原因是
②a、b、c三点中水的电离程度最小的是
(2)体积均为100mL、pH均为2的
 溶液与一元弱酸HX溶液,分别加水稀释过程中pH与加入水的体积的关系如图所示,则HX的电离平衡常数
溶液与一元弱酸HX溶液,分别加水稀释过程中pH与加入水的体积的关系如图所示,则HX的电离平衡常数 的电离平衡常数,理由是
的电离平衡常数,理由是
(3)常温下,在
 的
的 溶液和
溶液和 的
的 溶液中:
溶液中:①
 的
的 溶液中
溶液中 约为
约为 (保留两位有效数字)。
(保留两位有效数字)。②常温下,
 溶液的
溶液的
(4)某温度时,测得
 溶液的pH为11,在此温度下,将
溶液的pH为11,在此温度下,将 的NaOH溶液
的NaOH溶液 与
与 的硫酸
的硫酸 混合,若所得混合溶液为中性,则
混合,若所得混合溶液为中性,则
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】已知水在25℃和95℃的电离平衡曲线如图所示:___________ (选填“A”或“B”),并说明理由___________ 。
(2)在25℃时,将 的NaOH溶液与
的NaOH溶液与 的硫酸溶液混合,所得混合溶液的
的硫酸溶液混合,所得混合溶液的 ,则NaOH溶液与硫酸溶液的体积比为
,则NaOH溶液与硫酸溶液的体积比为___________ 。
(3)在曲线A所对应的温度下, 的HCl溶液和
的HCl溶液和 的某BOH溶液中,若水的电离度分别用
的某BOH溶液中,若水的电离度分别用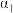 、
、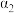 表示,则
表示,则
___________  (选填“大于”“小于”“等于”“无法确定”),原因是
(选填“大于”“小于”“等于”“无法确定”),原因是___________ 。
(4)在曲线B对应温度下,将 溶液与等物质的量浓度的
溶液与等物质的量浓度的 溶液等体积混合后,混合后溶液的
溶液等体积混合后,混合后溶液的
___________ 。
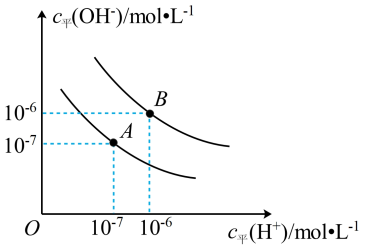
(2)在25℃时,将
 的NaOH溶液与
的NaOH溶液与 的硫酸溶液混合,所得混合溶液的
的硫酸溶液混合,所得混合溶液的 ,则NaOH溶液与硫酸溶液的体积比为
,则NaOH溶液与硫酸溶液的体积比为(3)在曲线A所对应的温度下,
 的HCl溶液和
的HCl溶液和 的某BOH溶液中,若水的电离度分别用
的某BOH溶液中,若水的电离度分别用 、
、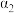 表示,则
表示,则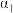
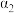 (选填“大于”“小于”“等于”“无法确定”),原因是
(选填“大于”“小于”“等于”“无法确定”),原因是(4)在曲线B对应温度下,将
 溶液与等物质的量浓度的
溶液与等物质的量浓度的 溶液等体积混合后,混合后溶液的
溶液等体积混合后,混合后溶液的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】雪碧是常见的碳酸型饮料。其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。 时,上述三种酸的电离常数如表所示:
时,上述三种酸的电离常数如表所示:
(1)三种酸的酸性由强到弱的顺序为_______ 。
(2)水存在电离平衡,下列能促进水的电离,且溶液显碱性的是_______ (填标号)。
a.通入氨气 b.加入 固体 c.加入苯甲酸钠
固体 c.加入苯甲酸钠 固体 d.加热至
固体 d.加热至
(3) 时,等物质的量浓度的苯甲酸
时,等物质的量浓度的苯甲酸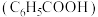 和苯甲酸钠
和苯甲酸钠 的混合溶液的
的混合溶液的
_______ (填“>”“<”或“=”)7,溶液中离子浓度由大到小的顺序是_______ 。
(4) 时,
时, 的柠檬酸与
的柠檬酸与 溶液中由水电离出的
溶液中由水电离出的 之比是
之比是_______ 。
(5)可乐含有比雪碧更刺激的酸性物质——磷酸(化学式为 ,沸点高、难挥发)。长期过量饮用可乐会破坏牙釉质(羟基磷酸钙
,沸点高、难挥发)。长期过量饮用可乐会破坏牙釉质(羟基磷酸钙 ),造成龋齿。牙齿表面存在平衡:
),造成龋齿。牙齿表面存在平衡: 。
。
①结合平衡移动原理解释造成龋齿的原因是_______ 。
②室温下,向磷酸溶液中滴加 溶液,含磷各微粒在溶液中的物质的量分数与
溶液,含磷各微粒在溶液中的物质的量分数与 的关系如图示。
的关系如图示。
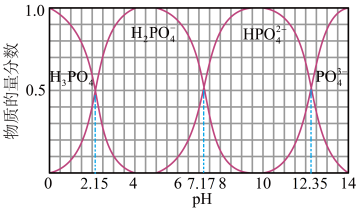
 的电离平衡常数
的电离平衡常数
_______ 。 ,溶液中
,溶液中
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
 时,上述三种酸的电离常数如表所示:
时,上述三种酸的电离常数如表所示:| 化学式 | 苯甲酸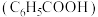 | 碳酸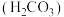 | 柠檬酸(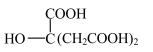 ) ) |
| 电离常数 | 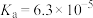 | 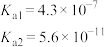 |  |
(1)三种酸的酸性由强到弱的顺序为
(2)水存在电离平衡,下列能促进水的电离,且溶液显碱性的是
a.通入氨气 b.加入
 固体 c.加入苯甲酸钠
固体 c.加入苯甲酸钠 固体 d.加热至
固体 d.加热至
(3)
 时,等物质的量浓度的苯甲酸
时,等物质的量浓度的苯甲酸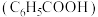 和苯甲酸钠
和苯甲酸钠 的混合溶液的
的混合溶液的
(4)
 时,
时, 的柠檬酸与
的柠檬酸与 溶液中由水电离出的
溶液中由水电离出的 之比是
之比是(5)可乐含有比雪碧更刺激的酸性物质——磷酸(化学式为
 ,沸点高、难挥发)。长期过量饮用可乐会破坏牙釉质(羟基磷酸钙
,沸点高、难挥发)。长期过量饮用可乐会破坏牙釉质(羟基磷酸钙 ),造成龋齿。牙齿表面存在平衡:
),造成龋齿。牙齿表面存在平衡: 。
。①结合平衡移动原理解释造成龋齿的原因是
②室温下,向磷酸溶液中滴加
 溶液,含磷各微粒在溶液中的物质的量分数与
溶液,含磷各微粒在溶液中的物质的量分数与 的关系如图示。
的关系如图示。
 的电离平衡常数
的电离平衡常数
 ,溶液中
,溶液中
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)在一定温度下,有a.盐酸;b.硫酸;c.醋酸三种酸:
a.若三者 相同时,溶质物质的量浓度由大到小的顺序是
相同时,溶质物质的量浓度由大到小的顺序是___________ (填字母,下同)。
b.将 相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积由大到小为
相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积由大到小为___________ 。
c.将体积均为10毫升pH均为3的a和c溶液加入水稀释至pH均为6,则加入水的体积a___________ c(填“>”“<”或“=”)。
(2)当 浓度较低时常用纯碱溶液进行吸收。表为
浓度较低时常用纯碱溶液进行吸收。表为 、
、 的电离平衡常数。
的电离平衡常数。
纯碱溶液吸收少量 的离子方程式为
的离子方程式为___________ 。
(3)磷酸是三元弱酸,常温下三级电离常数分别是 ,
,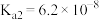 ,
, ,解答下列问题:
,解答下列问题:
a.常温下将相同物质的量浓度的氢氧化钠溶液与磷酸溶液按1:1的体积比混合,所得的溶液中 、
、 、
、 的浓度从大到小的顺序为
的浓度从大到小的顺序为___________ ;
b.常温下,将相同物质的量浓度的磷酸二氢钠溶液与磷酸钠溶液按1:1的体积比混合,所得的溶液中离子浓度位于前三位的从大到小依次是___________ 。
(4)在新制氯水中加入少量的NaCl固体,水的电离平衡___________ 移动(填“向右”、“向左”、或“不”)。
(5)某温度下,纯水中的 。若温度不变,滴入稀硫酸使
。若温度不变,滴入稀硫酸使 ,则由水电离出的
,则由水电离出的 为
为___________ mol/L。
(1)在一定温度下,有a.盐酸;b.硫酸;c.醋酸三种酸:
a.若三者
 相同时,溶质物质的量浓度由大到小的顺序是
相同时,溶质物质的量浓度由大到小的顺序是b.将
 相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积由大到小为
相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液液的体积由大到小为c.将体积均为10毫升pH均为3的a和c溶液加入水稀释至pH均为6,则加入水的体积a
(2)当
 浓度较低时常用纯碱溶液进行吸收。表为
浓度较低时常用纯碱溶液进行吸收。表为 、
、 的电离平衡常数。
的电离平衡常数。| 电离平衡常数 | 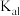 | 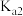 |
 |  | 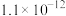 |
 | 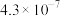 | 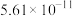 |
 的离子方程式为
的离子方程式为(3)磷酸是三元弱酸,常温下三级电离常数分别是
 ,
,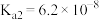 ,
, ,解答下列问题:
,解答下列问题:a.常温下将相同物质的量浓度的氢氧化钠溶液与磷酸溶液按1:1的体积比混合,所得的溶液中
 、
、 、
、 的浓度从大到小的顺序为
的浓度从大到小的顺序为b.常温下,将相同物质的量浓度的磷酸二氢钠溶液与磷酸钠溶液按1:1的体积比混合,所得的溶液中离子浓度位于前三位的从大到小依次是
(4)在新制氯水中加入少量的NaCl固体,水的电离平衡
(5)某温度下,纯水中的
 。若温度不变,滴入稀硫酸使
。若温度不变,滴入稀硫酸使 ,则由水电离出的
,则由水电离出的 为
为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氰化钠是一种剧毒物质,工业上常用硫代硫酸钠溶液处理废水中的氰化钠.硫代硫酸钠的工业制备原理为: .某化学兴趣小组拟用该原理在实验室制备硫代硫酸钠,并使用硫代硫酸钠溶液对氰化钠溶液进行统一解毒销毁.
.某化学兴趣小组拟用该原理在实验室制备硫代硫酸钠,并使用硫代硫酸钠溶液对氰化钠溶液进行统一解毒销毁.

实验Ⅰ.实验室通过如图所示装置制备 晶体
晶体
(1)盛装浓硫酸的仪器名称是______ .
(2)a装置中发生的化学反应方程式为______ .
(3)反应开始后,c中先有淡黄色浑浊产生,后又变为澄清,此浑浊物可能是______ 。(填化学式)
(4)实验结束后,在e处最好连接盛______ (填“NaOH溶液”、“水”、“ ”中的一种)的注射器.
”中的一种)的注射器.
实验Ⅱ.产品纯度的检测
(5)滴定过程中可能造成实验结果偏高的是______(填字母).
 .某化学兴趣小组拟用该原理在实验室制备硫代硫酸钠,并使用硫代硫酸钠溶液对氰化钠溶液进行统一解毒销毁.
.某化学兴趣小组拟用该原理在实验室制备硫代硫酸钠,并使用硫代硫酸钠溶液对氰化钠溶液进行统一解毒销毁.
实验Ⅰ.实验室通过如图所示装置制备
 晶体
晶体(1)盛装浓硫酸的仪器名称是
(2)a装置中发生的化学反应方程式为
(3)反应开始后,c中先有淡黄色浑浊产生,后又变为澄清,此浑浊物可能是
(4)实验结束后,在e处最好连接盛
 ”中的一种)的注射器.
”中的一种)的注射器.实验Ⅱ.产品纯度的检测
(5)滴定过程中可能造成实验结果偏高的是______(填字母).
A.锥形瓶未用 溶液润洗 溶液润洗 | B.锥形瓶中溶液变蓝后立刻停止滴定,进行读数 |
| C.滴定到终点时仰视读数 | D.滴定管尖嘴内滴定前无气泡,滴定到终点出现气泡 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.中和反应反应热的测定。
测定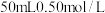 盐酸和
盐酸和 溶液中和反应时放出的热量。
溶液中和反应时放出的热量。
(1)采用稍过量的 溶液的原因是
溶液的原因是_______ 。
(2)若两种溶液的密度均为 ,反应后生成溶液的比热容
,反应后生成溶液的比热容 ,反应过程中测得体系温度升高
,反应过程中测得体系温度升高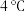 ,则该反应放出
,则该反应放出_______  热量。
热量。
Ⅱ.简易原电池反应。
(3)培养皿内装有含 饱和溶液的琼脂,再滴入5~6滴酚酞溶液和
饱和溶液的琼脂,再滴入5~6滴酚酞溶液和 溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生蓝色的
溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生蓝色的_______ (填化学式)沉淀;铜丝周围的现象是_______ ,发生的电极反应式为_______ 。

Ⅲ.某同学用中和滴定法测定某烧碱溶液的浓度。
(4)实验步骤:用图1中仪器_______ (填“A”或“B”)取待测烧碱溶液 于锥形瓶中,滴加2滴酚酞作指示剂。记录盛装
于锥形瓶中,滴加2滴酚酞作指示剂。记录盛装 盐酸标准溶液的酸式滴定管的初始读数。如果某时刻液面位置如图2所示,则此时的读数为
盐酸标准溶液的酸式滴定管的初始读数。如果某时刻液面位置如图2所示,则此时的读数为_______  。
。

(5)滴定。滴定过程中,眼睛应始终注视锥形瓶内溶液颜色变化,滴定终点的现象是_______ 。
(6)数据记录与处理
计算该烧碱溶液的浓度
_______  (精确到小数点后4位)。
(精确到小数点后4位)。
(7)误差分析。以下操作会导致测定结果偏高的是_______(填字母)。
Ⅰ.中和反应反应热的测定。
测定
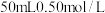 盐酸和
盐酸和 溶液中和反应时放出的热量。
溶液中和反应时放出的热量。(1)采用稍过量的
 溶液的原因是
溶液的原因是(2)若两种溶液的密度均为
 ,反应后生成溶液的比热容
,反应后生成溶液的比热容 ,反应过程中测得体系温度升高
,反应过程中测得体系温度升高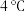 ,则该反应放出
,则该反应放出 热量。
热量。Ⅱ.简易原电池反应。
(3)培养皿内装有含
 饱和溶液的琼脂,再滴入5~6滴酚酞溶液和
饱和溶液的琼脂,再滴入5~6滴酚酞溶液和 溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生蓝色的
溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生蓝色的
Ⅲ.某同学用中和滴定法测定某烧碱溶液的浓度。
(4)实验步骤:用图1中仪器
 于锥形瓶中,滴加2滴酚酞作指示剂。记录盛装
于锥形瓶中,滴加2滴酚酞作指示剂。记录盛装 盐酸标准溶液的酸式滴定管的初始读数。如果某时刻液面位置如图2所示,则此时的读数为
盐酸标准溶液的酸式滴定管的初始读数。如果某时刻液面位置如图2所示,则此时的读数为 。
。
(5)滴定。滴定过程中,眼睛应始终注视锥形瓶内溶液颜色变化,滴定终点的现象是
(6)数据记录与处理
| 实验编号 | 烧碱待测液体 | 盐酸标准液体积(消耗) |
| 1 | 25.00 | 18.05 |
| 2 | 25.00 | 18.00 |
| 3 | 25.00 | 17.95 |
| 4 | 25.00 | 18.95 |
计算该烧碱溶液的浓度

 (精确到小数点后4位)。
(精确到小数点后4位)。(7)误差分析。以下操作会导致测定结果偏高的是_______(填字母)。
| A.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失 |
| B.装待测液前,锥形瓶中有少量蒸馏水 |
| C.未用盐酸标准溶液润洗滴定管 |
| D.观察读数时,滴定前仰视,滴定后俯视 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】Ⅰ.次氯酸钠溶液和二氯异氰尿酸钠(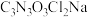 )都是常用的杀菌消毒剂。NaClO可用于制备二氯异氰尿酸钠。
)都是常用的杀菌消毒剂。NaClO可用于制备二氯异氰尿酸钠。
(1)NaClO溶液可由低温下将 缓慢通入NaOH溶液中而制得。制备NaClO的化学方程式为
缓慢通入NaOH溶液中而制得。制备NaClO的化学方程式为______ ;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会导致消毒作用减弱,其原因是______ 。
(2)有研究显示,南极臭氧空洞中的污染物硝酸氯(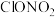 )与次氯酸钠在结构上有类似之处。下列推测有一项
)与次氯酸钠在结构上有类似之处。下列推测有一项不合理 ,该选项是______。
Ⅱ.二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为: ;
;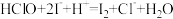 ;
;  。
。
准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗 溶液20.00mL。
溶液20.00mL。
(3)滴定达到终点的现象为:溶液由______ 色变______ 色,且半分钟内不再改变。
(4)通过计算判断该样品是否为优质品______ 。(写出计算过程 )
该样品的有效氯= ×100%
×100%
(5)若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值______ (填“偏高”或“偏低”)。
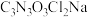 )都是常用的杀菌消毒剂。NaClO可用于制备二氯异氰尿酸钠。
)都是常用的杀菌消毒剂。NaClO可用于制备二氯异氰尿酸钠。(1)NaClO溶液可由低温下将
 缓慢通入NaOH溶液中而制得。制备NaClO的化学方程式为
缓慢通入NaOH溶液中而制得。制备NaClO的化学方程式为(2)有研究显示,南极臭氧空洞中的污染物硝酸氯(
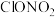 )与次氯酸钠在结构上有类似之处。下列推测有一项
)与次氯酸钠在结构上有类似之处。下列推测有一项| A.具有强氧化性 | B.与NaOH溶液反应可生成两种钠盐 |
| C.与盐酸作用能产生氯气 | D.水解生成盐酸和硝酸 |
Ⅱ.二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到优质品标准。实验检测原理为:
 ;
;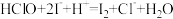 ;
;  。
。准确称取1.1200g样品,用容量瓶配成250.0mL溶液;取25.00mL上述溶液于碘量瓶中,加入适量稀硫酸和过量KI溶液,密封在暗处静置5min;用
 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂继续滴定至终点,消耗 溶液20.00mL。
溶液20.00mL。(3)滴定达到终点的现象为:溶液由
(4)通过计算判断该样品是否为优质品
该样品的有效氯=
 ×100%
×100%(5)若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值
您最近一年使用:0次



