铅酸蓄电池是常见的化学电源,其电极材料分别是Pb和PbO2,电解质溶液为一定浓度的硫酸。充放电的总反应是: Pb+PbO2+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
(1)该蓄电池放电工作时电解质溶液中SO42-移向________ (填“正极”或“负极”,下同)充电时,该极接直流电源的_________ 。
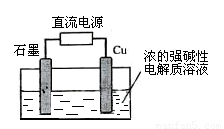
(2)Cu2O是一种半导体材料,可通过右图的电解装置制取,电解总反应为:2Cu+H2O Cu2O+H2↑
Cu2O+H2↑
阴极的电极反应式是__________________________ 。 若用铅酸蓄电池作为电源进行电解,当蓄电池中有0.2mol H+被消耗时,Cu2O的理论产量为_______ g。
(3)为防止钢闸门在水中被腐蚀,可将其与铅酸蓄电池的_______ 极相连(填Pb或PbO2)。
(4)用铅蓄电池电解500mL饱和食盐水(足量)。电解一段时间后,共收集到气体1120mL(已折算成标准状况下),则所得溶液的pH=_________ (不考虑气体的溶解及电解前后溶液体积的变化)
 2PbSO4+2H2O
2PbSO4+2H2O
(1)该蓄电池放电工作时电解质溶液中SO42-移向
(2)Cu2O是一种半导体材料,可通过右图的电解装置制取,电解总反应为:2Cu+H2O
 Cu2O+H2↑
Cu2O+H2↑阴极的电极反应式是
(3)为防止钢闸门在水中被腐蚀,可将其与铅酸蓄电池的
(4)用铅蓄电池电解500mL饱和食盐水(足量)。电解一段时间后,共收集到气体1120mL(已折算成标准状况下),则所得溶液的pH=
更新时间:2018-02-26 10:06:05
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池,外电路电子移动的方向为___ 。(填“a到b”或者“b到a”)
②氢氧燃料电池的正极的电极反应方程式为:___ 。
③电池工作一段时间后硫酸溶液的浓度____ (填增大、减小或不变)。
(2)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
①该电池放电时负极反应式为___ 。
②放电时每转移3mol电子,正极有__ molK2FeO4被还原。
③充电时电池上标有“-”的电极应与外接电源的___ 极相连。(填“正”,“负”,“阴”,“阳”)

①氢氧燃料电池,外电路电子移动的方向为
②氢氧燃料电池的正极的电极反应方程式为:
③电池工作一段时间后硫酸溶液的浓度
(2)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。①该电池放电时负极反应式为
②放电时每转移3mol电子,正极有
③充电时电池上标有“-”的电极应与外接电源的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】一种简单的原电池装置如图所示。据图回答下列问题。
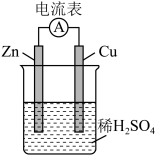
(1)锌是该电池的_______ (填“正”或“负”)极。Zn片上发生的电极反应为___________ 。Cu片上发生的电极反应为_________ 。能证明化学能转化为电能的实验现象为___________ 。
(2)装置中稀硫酸的作用是___________。
(3)某原电池的总反应是Zn+Cu2+=Zn2+ +Cu,该原电池的正确组成是______ 。
(4)下列反应通过原电池装置,不能实现把化学能直接转化为电能的是___________ (填序号)。
a.CH4+2O2=CO2+2H2O b.H2+Cl2=2HCl
c.NaOH+HCl=NaCl+H2O d.C6H12O6+6O2=6CO2+6H2O

(1)锌是该电池的
(2)装置中稀硫酸的作用是___________。
| A.电极材料 | B.电极反应物 | C.电子导体 | D.离子导体 |
(3)某原电池的总反应是Zn+Cu2+=Zn2+ +Cu,该原电池的正确组成是
| A | B | C | D |
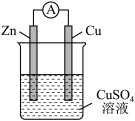 | 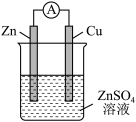 |  | 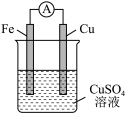 |
(4)下列反应通过原电池装置,不能实现把化学能直接转化为电能的是
a.CH4+2O2=CO2+2H2O b.H2+Cl2=2HCl
c.NaOH+HCl=NaCl+H2O d.C6H12O6+6O2=6CO2+6H2O
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】 三种强电解质,它们在水中电离出的离子如下表所示:
三种强电解质,它们在水中电离出的离子如下表所示:
如图1所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C作为溶质的三种溶液,电极均为石墨电极,接通电源,经过一段时间后,测得乙中 电极质量增加了
电极质量增加了 。常温下各烧杯中溶液的
。常温下各烧杯中溶液的 与电解时间
与电解时间 的关系如图2所示,据此回答下列问题:
的关系如图2所示,据此回答下列问题:
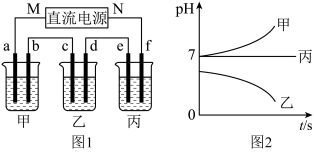
(1) 为电源的
为电源的_____ (填写“正”或“负”)极,f电极的电极反应式为_____ 。
(2)写出乙烧杯中电解反应的离子方程式_____ 。
(3)要使甲恢复到原来的状态,理论上应通入标准状态下的_____ 气体(填化学式)_____ L。
(4)若直流电源使用的是铅酸蓄电池,则放电时 极的电极反应式为
极的电极反应式为_____ , 极附近溶液的
极附近溶液的
_____ (填“升高”或“降低”或“不变”)。铅酸蓄电池充电时,若阳极和阴极之间用质子交换膜隔开,当外电路通过 电子时,则有
电子时,则有_____  阳离子由阳极室转移到阴极室。
阳离子由阳极室转移到阴极室。
 三种强电解质,它们在水中电离出的离子如下表所示:
三种强电解质,它们在水中电离出的离子如下表所示:| 阳离子 |  、 、 |
| 阴离子 |  、 、 、 、 |
 电极质量增加了
电极质量增加了 。常温下各烧杯中溶液的
。常温下各烧杯中溶液的 与电解时间
与电解时间 的关系如图2所示,据此回答下列问题:
的关系如图2所示,据此回答下列问题:
(1)
 为电源的
为电源的(2)写出乙烧杯中电解反应的离子方程式
(3)要使甲恢复到原来的状态,理论上应通入标准状态下的
(4)若直流电源使用的是铅酸蓄电池,则放电时
 极的电极反应式为
极的电极反应式为 极附近溶液的
极附近溶液的
 电子时,则有
电子时,则有 阳离子由阳极室转移到阴极室。
阳离子由阳极室转移到阴极室。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】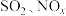 (主要指
(主要指 和
和 )是大气主要污染物之一。
)是大气主要污染物之一。
(1)用水吸收 的相关热化学方程式如下:
的相关热化学方程式如下:

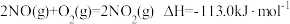
在上述吸收过程中调整 与
与 的比例进行反应可以达到最大程度的吸收,反应
的比例进行反应可以达到最大程度的吸收,反应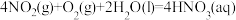 的
的
_______  。
。
(2)NH3的选择性催化还原法是应用最为广泛的脱硝技术,反应原理: ,当生成1molN2时,转移的电子为
,当生成1molN2时,转移的电子为_______ mol。
(3)用间接电化学法同时去除烟气中 和
和 ,装置如下图所示。
,装置如下图所示。

①电极M上的电极反应式为_______ 。
②写出吸收池中NO被吸收的离子方程式_______ 。
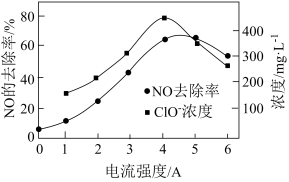
(4)电解氧化法可将废气中NO转变为硝态氮。电解 溶液,NO的去除率、溶液中相关成的浓度与电流强度的关系如图所示。电流强度在
溶液,NO的去除率、溶液中相关成的浓度与电流强度的关系如图所示。电流强度在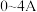 时,随着电流强度的增大,NO的去除率升高的原因是
时,随着电流强度的增大,NO的去除率升高的原因是_______
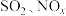 (主要指
(主要指 和
和 )是大气主要污染物之一。
)是大气主要污染物之一。(1)用水吸收
 的相关热化学方程式如下:
的相关热化学方程式如下:
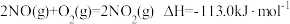
在上述吸收过程中调整
 与
与 的比例进行反应可以达到最大程度的吸收,反应
的比例进行反应可以达到最大程度的吸收,反应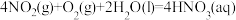 的
的
 。
。(2)NH3的选择性催化还原法是应用最为广泛的脱硝技术,反应原理:
 ,当生成1molN2时,转移的电子为
,当生成1molN2时,转移的电子为(3)用间接电化学法同时去除烟气中
 和
和 ,装置如下图所示。
,装置如下图所示。
①电极M上的电极反应式为
②写出吸收池中NO被吸收的离子方程式
(4)电解氧化法可将废气中NO转变为硝态氮。电解
 溶液,NO的去除率、溶液中相关成的浓度与电流强度的关系如图所示。电流强度在
溶液,NO的去除率、溶液中相关成的浓度与电流强度的关系如图所示。电流强度在 时,随着电流强度的增大,NO的去除率升高的原因是
时,随着电流强度的增大,NO的去除率升高的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某研究小组以TiCl4为原料制备新型耐热材料TiN。
步骤一:TiCl4水解制备TiO2(实验装置如图A,夹持装置省略):滴入TiCl4,边搅拌边加热,使混合液升温至80℃,保温3小时.离心分离白色沉淀TiO2·xH2O并洗涤,煅烧制得TiO2

(1)装置A中冷凝水的入口为____________ (填“a”或“b”)。
(2)三颈烧瓶中预置的稀盐酸可抑制胶体形成、促进白色沉淀生成,TiCl4水解生成的胶体主要成分为__________ (填化学式)。
(3)判断 沉淀是否洗涤干净,可使用的检验试剂有
沉淀是否洗涤干净,可使用的检验试剂有__________ 。
步骤二:由 制备
制备 并测定产率(实验装置如图,夹持装置省略)。
并测定产率(实验装置如图,夹持装置省略)。
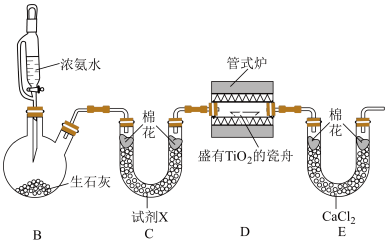
(4)装置C中试剂X为____________ 。
(5)装置D中反应生成 、
、 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_____________ 。
(6)装置E的作用是__________ 。
(7)实验中部分操作如下:
a.反应前,称取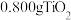 样品;
样品;
b.打开装置B中恒压滴液漏斗旋塞;
c.关闭装置B中恒压滴液漏斗旋塞;
d.打开管式炉加热开关,加热至800℃左右;
e.关闭管式炉加热开关,待装置冷却;
f.反应后,称得瓷舟中固体质量为0.496g。
①正确的操作顺序为:a→____________ →f(填标号)。
② 的产率为
的产率为_______________ 。
(8)一种电解法制钛的工艺如下图所示,CaCl2/CaO共熔体为介质,在阴极被还原的钙进一步还原TiO2,得到钛,在阴极制取钛的相关反应方程式为__________ 。

步骤一:TiCl4水解制备TiO2(实验装置如图A,夹持装置省略):滴入TiCl4,边搅拌边加热,使混合液升温至80℃,保温3小时.离心分离白色沉淀TiO2·xH2O并洗涤,煅烧制得TiO2

(1)装置A中冷凝水的入口为
(2)三颈烧瓶中预置的稀盐酸可抑制胶体形成、促进白色沉淀生成,TiCl4水解生成的胶体主要成分为
(3)判断
 沉淀是否洗涤干净,可使用的检验试剂有
沉淀是否洗涤干净,可使用的检验试剂有步骤二:由
 制备
制备 并测定产率(实验装置如图,夹持装置省略)。
并测定产率(实验装置如图,夹持装置省略)。
(4)装置C中试剂X为
(5)装置D中反应生成
 、
、 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(6)装置E的作用是
(7)实验中部分操作如下:
a.反应前,称取
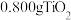 样品;
样品;b.打开装置B中恒压滴液漏斗旋塞;
c.关闭装置B中恒压滴液漏斗旋塞;
d.打开管式炉加热开关,加热至800℃左右;
e.关闭管式炉加热开关,待装置冷却;
f.反应后,称得瓷舟中固体质量为0.496g。
①正确的操作顺序为:a→
②
 的产率为
的产率为(8)一种电解法制钛的工艺如下图所示,CaCl2/CaO共熔体为介质,在阴极被还原的钙进一步还原TiO2,得到钛,在阴极制取钛的相关反应方程式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】(1)碳与水蒸气反应制取 H2的相关反应如下 :
Ⅰ:C(s)+H2O(g)═CO(g)+H2(g) △H=+ 131.0 kJ/mol
Ⅱ:CO(g)+H2O(g)═CO2(g)+H2(g) △H=﹣43 kJ/mol
Ⅲ:CaO(s)+CO2(g)═CaCO3(S) △H=﹣178.3 kJ/mol
计算反应 C(s)+2H2O(g)+CaO(s) CaCO3(s)+ 2H2(g)的△H=
CaCO3(s)+ 2H2(g)的△H=_____ kJ/mol;
(2)如图所示,常温下通电 5 min 后,发现铜电极的质量增加,试回答:

①电源电极 X 的名称为____ (填“正极”或“负极”)。
②电解池 B 中阳极的电极反应式是_______ 。
③若 KCl 溶液的体积是 200 mL,则当铜电极的质量增加2.16g 时 A 中溶液的 pH=_____ (忽略电解前后溶液体积的变化),若要使电解后的溶液恢复到与电解前完全相同的状态,则应加入_______ (填物质的种类及数量)
Ⅰ:C(s)+H2O(g)═CO(g)+H2(g) △H=+ 131.0 kJ/mol
Ⅱ:CO(g)+H2O(g)═CO2(g)+H2(g) △H=﹣43 kJ/mol
Ⅲ:CaO(s)+CO2(g)═CaCO3(S) △H=﹣178.3 kJ/mol
计算反应 C(s)+2H2O(g)+CaO(s)
 CaCO3(s)+ 2H2(g)的△H=
CaCO3(s)+ 2H2(g)的△H=(2)如图所示,常温下通电 5 min 后,发现铜电极的质量增加,试回答:

①电源电极 X 的名称为
②电解池 B 中阳极的电极反应式是
③若 KCl 溶液的体积是 200 mL,则当铜电极的质量增加2.16g 时 A 中溶液的 pH=
您最近一年使用:0次
【推荐1】青铜是金属冶炼史上最早的合金,我国出土了大量青铜器,体现了古代中国对人类文明的巨大贡献。青铜器在埋藏过程中会逐渐生锈,其修复工作是文物保护的重要环节。
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿。铜绿在一定程度上可以提升青铜器的艺术价值。青铜器生锈过程中,参与形成铜绿的物质有Cu和_______ 。
(2)继续查阅资料,了解到铜锈的成分很复杂,主要成分有 和
和 。结构如图所示:
。结构如图所示:
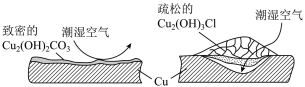
考古学家将铜锈分为“无害锈”和“有害锈”,“无害锈”形成后可阻止内部金属继续腐蚀,而“有害锈”则无法阻止腐蚀的深入。结合两种铜锈的结构推测,“有害锈”的主要成分为:_______ 。
(3) 的形成过程中会通过原电池反应产生
的形成过程中会通过原电池反应产生 (难溶于水的固体),请结合下图回答:
(难溶于水的固体),请结合下图回答:
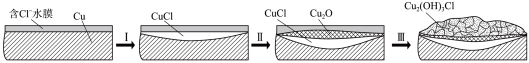
①过程的正极反应物是_______ 。
②过程Ⅰ负极的电极反应式是_______ 。
(4)青铜器的修复追求“修旧如旧”,即在尽量不破坏“无害锈”的情况下阻止青铜器继续被腐蚀,保护青铜器的艺术价值。青铜器除锈有以下三种常见方法:
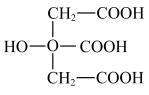
ⅰ.柠檬酸浸法:将腐蚀文物直接放在 的柠檬酸溶液中浸泡除锈(柠檬酸的结构如图所示):
的柠檬酸溶液中浸泡除锈(柠檬酸的结构如图所示):
ⅱ.碳酸钠法:将文物置于含 的溶液中浸泡,使
的溶液中浸泡,使 转化为
转化为 ;
;
ⅲ.BTA保护法:利用BTA(一种有机成膜剂)与 价Cu(如
价Cu(如 )反应,形成一层透明的高聚物薄膜。
)反应,形成一层透明的高聚物薄膜。
请回答下列问题:
①柠檬酸浸法利用了其结构中_______ (填官能团名称)的性质。
②写出碳酸钠法的离子方程式_______ 。
③相比于酸浸法,BTA保护法的优点是_______ 。
(5)陕西历史博物馆展出了许多鎏金工艺青铜器。鎏金是古代常用的镀金工艺,将金汞合金涂于器物表面,加热使汞挥发,便形成一层光亮的金镀层。下列关于青铜器鎏金工艺的说法正确的是_______ (填序号)。

A.鎏金工艺的镀金过程是一种化学变化
B.鎏金除了改善外观,还可保护青铜器,使其不易生锈
C.若表面的金镀层破损,暴露出的青铜表面会更易生锈
(1)查阅高中教材得知铜锈为Cu2(OH)2CO3,俗称铜绿。铜绿在一定程度上可以提升青铜器的艺术价值。青铜器生锈过程中,参与形成铜绿的物质有Cu和
(2)继续查阅资料,了解到铜锈的成分很复杂,主要成分有
 和
和 。结构如图所示:
。结构如图所示:
考古学家将铜锈分为“无害锈”和“有害锈”,“无害锈”形成后可阻止内部金属继续腐蚀,而“有害锈”则无法阻止腐蚀的深入。结合两种铜锈的结构推测,“有害锈”的主要成分为:
(3)
 的形成过程中会通过原电池反应产生
的形成过程中会通过原电池反应产生 (难溶于水的固体),请结合下图回答:
(难溶于水的固体),请结合下图回答:
①过程的正极反应物是
②过程Ⅰ负极的电极反应式是
(4)青铜器的修复追求“修旧如旧”,即在尽量不破坏“无害锈”的情况下阻止青铜器继续被腐蚀,保护青铜器的艺术价值。青铜器除锈有以下三种常见方法:
ⅰ.柠檬酸浸法:将腐蚀文物直接放在
 的柠檬酸溶液中浸泡除锈(柠檬酸的结构如图所示):
的柠檬酸溶液中浸泡除锈(柠檬酸的结构如图所示):
ⅱ.碳酸钠法:将文物置于含
 的溶液中浸泡,使
的溶液中浸泡,使 转化为
转化为 ;
;ⅲ.BTA保护法:利用BTA(一种有机成膜剂)与
 价Cu(如
价Cu(如 )反应,形成一层透明的高聚物薄膜。
)反应,形成一层透明的高聚物薄膜。请回答下列问题:
①柠檬酸浸法利用了其结构中
②写出碳酸钠法的离子方程式
③相比于酸浸法,BTA保护法的优点是
(5)陕西历史博物馆展出了许多鎏金工艺青铜器。鎏金是古代常用的镀金工艺,将金汞合金涂于器物表面,加热使汞挥发,便形成一层光亮的金镀层。下列关于青铜器鎏金工艺的说法正确的是

A.鎏金工艺的镀金过程是一种化学变化
B.鎏金除了改善外观,还可保护青铜器,使其不易生锈
C.若表面的金镀层破损,暴露出的青铜表面会更易生锈
您最近一年使用:0次
【推荐2】I.电化学与我们的生活有着密切的联系,请结合电化学知识回答下列有关问题:
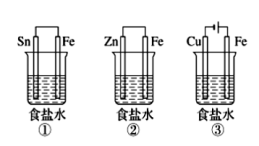
(1)如图所示的三种探究钢铁的腐蚀与防护的装置中,采用牺牲阳极保护法进行金属Fe防护的是_______ (填装置序号)。
(2)已知铅蓄电池的工作原理为:Pb + PbO2 + 2H2SO4 2PbSO4 + 2H2O,现用如图装置进行电解(电解液足量),一段时间后铁电极质量减少并测得装置中转移了0.4 mol电子。请回答下列问题。
2PbSO4 + 2H2O,现用如图装置进行电解(电解液足量),一段时间后铁电极质量减少并测得装置中转移了0.4 mol电子。请回答下列问题。

①B是铅蓄电池的_______ 极,电极反应式为:_______ 。
②Ag电极的电极产物共_______ g,CuSO4溶液的浓度_______ (填“减小”“增大”或“不变”)。
Ⅱ.下表是常温下几种弱酸和弱碱的电离平衡常数
请回答下列问题:
(3)所给的四种酸中,酸性最弱的是_______ (填化学式)。物质的量浓度为0.1mol·L-1的下列四种溶液,pH由大到小的顺序是_______ (填标号)。
a.Na2CO3 b.NaCN c.CH3COONa d.NaHCO3
(4)CH3COONH4溶液中存在的各离子浓度大小关系为_______ 。
(1)如图所示的三种探究钢铁的腐蚀与防护的装置中,采用牺牲阳极保护法进行金属Fe防护的是

(2)已知铅蓄电池的工作原理为:Pb + PbO2 + 2H2SO4
 2PbSO4 + 2H2O,现用如图装置进行电解(电解液足量),一段时间后铁电极质量减少并测得装置中转移了0.4 mol电子。请回答下列问题。
2PbSO4 + 2H2O,现用如图装置进行电解(电解液足量),一段时间后铁电极质量减少并测得装置中转移了0.4 mol电子。请回答下列问题。
①B是铅蓄电池的
②Ag电极的电极产物共
Ⅱ.下表是常温下几种弱酸和弱碱的电离平衡常数
| 化学式 | CH3COOH | H2CO3 | HCN | HClO | NH3•H2O |
| 电离常数(Ka或Kb) | 1.8×10-5 | K1:4.4×10-7 K2:4.7×10-11 | 6.2×10-10 | 3×10-8 | 1.8×10-5 |
(3)所给的四种酸中,酸性最弱的是
a.Na2CO3 b.NaCN c.CH3COONa d.NaHCO3
(4)CH3COONH4溶液中存在的各离子浓度大小关系为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ、已知下面在298K时的热化学方程式:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,CH4(g)+2O2(g)=CO2(g)+2H2O (l) ΔH=-890.3 kJ·mol-1,C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1。根据上面的热化学方程式完成下列问题:
(1)通过计算说明等质量的H2、C、CH4完全燃烧时放出热量最多的是___ 。
(2)根据以上反应,则C(s)+2H2(g)=CH4(g)的焓变ΔH=___ 。
(3)已知H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:___ 。
Ⅱ、为了解金属腐蚀的原因和寻求防止金属腐蚀的方法具有重要意义。
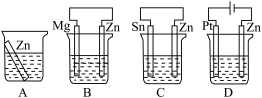
(1)分别放在以下装置(都盛有0.1mol·L-1的H2SO4溶液)中的四块相同的纯锌片,其中腐蚀最快的是___ 。
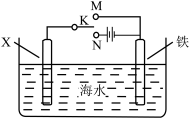
(2)利用如图装置,可以模拟铁的电化学防护。其中X为碳棒,为减缓铁的腐蚀,开关K应置于___ 处。若X为锌,开关K置于M处,该电化学防护法称为___ 。
(1)通过计算说明等质量的H2、C、CH4完全燃烧时放出热量最多的是
(2)根据以上反应,则C(s)+2H2(g)=CH4(g)的焓变ΔH=
(3)已知H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:
Ⅱ、为了解金属腐蚀的原因和寻求防止金属腐蚀的方法具有重要意义。
(1)分别放在以下装置(都盛有0.1mol·L-1的H2SO4溶液)中的四块相同的纯锌片,其中腐蚀最快的是

(2)利用如图装置,可以模拟铁的电化学防护。其中X为碳棒,为减缓铁的腐蚀,开关K应置于

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】锰酸锂离子蓄电池是第二代锂离子动力电池。一种以软锰矿浆(主要成分为MnO2,含少量Fe2O3、FeO、A12O3、SiO2等杂质)为原料制备锰酸锂的流程如图所示。
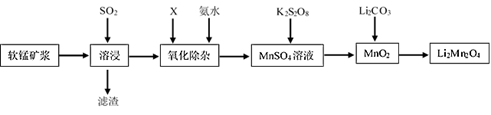
(1)溶浸生产中为提高SO2回收率可采取的措施有__ (填序号)
A.不断搅拌,使SO2和软锰矿浆充分接触
B.增大通入SO2的流速
C.减少软锰矿浆的进入量
D.减小通入SO2的流速
(2)已知:室温下,Ksp[A1(OH)3]=1×10-33,Ksp[Fe(OH)3]=l×10-39,pH=7.1时Mn(OH)2开始沉淀。氧化除杂时(室温)除去MnSO4液中的Fe3+、Al3+(使其浓度小于1×l0-6mol/L),需调节溶液pH范围为__ 。
(3)由硫酸锰与K2S2O8溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。请写出发生反应的离子方程式__ 。
(4)将MnO2和Li2CO3按4:1的物质的量比配料,混合搅拌,然后升温至600℃〜750℃,制取产品LiMn2O4。写出该反应的化学方程式__ 。
(5)锰酸锂可充电电池的总反应为:Li1-xMn2O4+LixC LiMn2O4+C(0<x<1)
LiMn2O4+C(0<x<1)
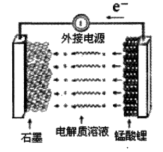
①充电时,电池的阳极反应式为__ ,若此时转移lmole-,则石墨电极将增重__ g。
②废旧锰酸锂电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是__ 。

(1)溶浸生产中为提高SO2回收率可采取的措施有
A.不断搅拌,使SO2和软锰矿浆充分接触
B.增大通入SO2的流速
C.减少软锰矿浆的进入量
D.减小通入SO2的流速
(2)已知:室温下,Ksp[A1(OH)3]=1×10-33,Ksp[Fe(OH)3]=l×10-39,pH=7.1时Mn(OH)2开始沉淀。氧化除杂时(室温)除去MnSO4液中的Fe3+、Al3+(使其浓度小于1×l0-6mol/L),需调节溶液pH范围为
(3)由硫酸锰与K2S2O8溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。请写出发生反应的离子方程式
(4)将MnO2和Li2CO3按4:1的物质的量比配料,混合搅拌,然后升温至600℃〜750℃,制取产品LiMn2O4。写出该反应的化学方程式
(5)锰酸锂可充电电池的总反应为:Li1-xMn2O4+LixC
 LiMn2O4+C(0<x<1)
LiMn2O4+C(0<x<1)
①充电时,电池的阳极反应式为
②废旧锰酸锂电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。

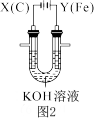
请回答:
用图1所示装置进行第一组实验(K闭合)
(1)Zn极为___ 极。实验过程中,甲中SO
___ (填“从左向右”、“从右问左”或“不”)移动;反应初期乙中N极发生的电极反应为____ 。
(2)反应一段时间后,打开K,向乙中加入0.1molCu(OH)2后恰好复原,则上述电解过程中转移的电子数为___ 。
(3)用图2所示装置进行第二组实验,实验中Y极区产生FeO ,溶液呈浅紫红色。Y极上的电极反应式为
,溶液呈浅紫红色。Y极上的电极反应式为___ 。
(4)电解过程中、X极区溶液的pH___ (填“增大”、“减小”或“不变”)。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应式为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO4,该电池正极发生的电极反应式为___ 。

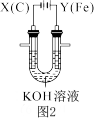
请回答:
用图1所示装置进行第一组实验(K闭合)
(1)Zn极为

(2)反应一段时间后,打开K,向乙中加入0.1molCu(OH)2后恰好复原,则上述电解过程中转移的电子数为
(3)用图2所示装置进行第二组实验,实验中Y极区产生FeO
 ,溶液呈浅紫红色。Y极上的电极反应式为
,溶液呈浅紫红色。Y极上的电极反应式为(4)电解过程中、X极区溶液的pH
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应式为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO4,该电池正极发生的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】五氧化二钒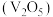 在冶金、催化剂、磁性材料等领域有重要作用。实验室以含钥废料(含
在冶金、催化剂、磁性材料等领域有重要作用。实验室以含钥废料(含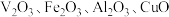 等)来制备
等)来制备 的一种工艺流程如下图:
的一种工艺流程如下图:

已知:I.含钒离子在溶液中的主要存在形式与溶液 的关系:
的关系:
II.25℃时,难溶电解质的溶度积常数如下表所示:
当金属离子浓度小于 时,沉淀完全。
时,沉淀完全。
请回答下列问题:
(1)基态钒原子的价电子轨道表示式为___________
(2)“焙烧”时, 生成
生成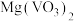 的反应中,氧化剂与还原剂物质的量之比为
的反应中,氧化剂与还原剂物质的量之比为___________
(3)“调 净化I”的步骤中,金属阳离子完全沉淀顺序依次是
净化I”的步骤中,金属阳离子完全沉淀顺序依次是___________ ,该步骤除了沉淀某些金属阳离子外,还有的作用是___________ 。
(4)“煅烧”时,除生成 外,还生成参与大气循环的气体,该反应的化学方程式为
外,还生成参与大气循环的气体,该反应的化学方程式为________
(5)全钒液流电池是一种新型储能转化装置,该电池是将不同价态的含钥离子溶液分别作为正极和负极的活性物质,储存在各自的酸性电解质储罐中。其结构原理如图所示:
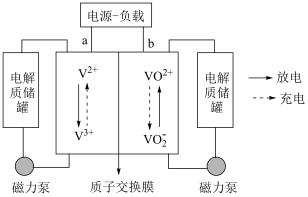
①放电时,正极的电极反应式为___________
②充电时,理论上电路中转移 电子时,右侧电解质储罐中
电子时,右侧电解质储罐中 变化的数目为
变化的数目为___________ 。
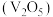 在冶金、催化剂、磁性材料等领域有重要作用。实验室以含钥废料(含
在冶金、催化剂、磁性材料等领域有重要作用。实验室以含钥废料(含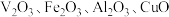 等)来制备
等)来制备 的一种工艺流程如下图:
的一种工艺流程如下图:
已知:I.含钒离子在溶液中的主要存在形式与溶液
 的关系:
的关系: | 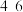 |  |  |
| 主要离子 |  |  | 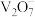 |
| 难溶电解质 |  |  |  |  |
 | 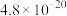 |  |  | 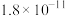 |
 时,沉淀完全。
时,沉淀完全。请回答下列问题:
(1)基态钒原子的价电子轨道表示式为
(2)“焙烧”时,
 生成
生成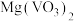 的反应中,氧化剂与还原剂物质的量之比为
的反应中,氧化剂与还原剂物质的量之比为(3)“调
 净化I”的步骤中,金属阳离子完全沉淀顺序依次是
净化I”的步骤中,金属阳离子完全沉淀顺序依次是(4)“煅烧”时,除生成
 外,还生成参与大气循环的气体,该反应的化学方程式为
外,还生成参与大气循环的气体,该反应的化学方程式为(5)全钒液流电池是一种新型储能转化装置,该电池是将不同价态的含钥离子溶液分别作为正极和负极的活性物质,储存在各自的酸性电解质储罐中。其结构原理如图所示:

①放电时,正极的电极反应式为
②充电时,理论上电路中转移
 电子时,右侧电解质储罐中
电子时,右侧电解质储罐中 变化的数目为
变化的数目为
您最近一年使用:0次



