(1)通常把pH小于_________ 的降雨称为酸雨。
(2)0.6mol H2SO4 的质量是_________ g,含_______ 个分子,该硫酸所含氢元素的质量与_________ g HCl中所含氢元素的质量相同。
(3)“比较”是化学研究物质性质的基本方法之一,请运用比较法解答下列问题:已知在一定条件下,过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:
2Na2O2+2CO2=2Na2CO3+O2, Na2O2+CO=Na2CO3。
①试分别写出Na2O2与SO2、SO3反应的化学方程式。
___________________________ ;__________________ 。
②通过比较可知:在氧化物中,当非金属元素处于______ 价时,其氧化物与过氧化钠反应就有O2生成。
(2)0.6mol H2SO4 的质量是
(3)“比较”是化学研究物质性质的基本方法之一,请运用比较法解答下列问题:已知在一定条件下,过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:
2Na2O2+2CO2=2Na2CO3+O2, Na2O2+CO=Na2CO3。
①试分别写出Na2O2与SO2、SO3反应的化学方程式。
②通过比较可知:在氧化物中,当非金属元素处于
更新时间:2018-04-13 12:37:15
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】NA为阿伏加德罗常数的值。下列说法错误的是___________ 。
A.25℃、101kPa下,28L氢气中质子的数目为2.5NA
B.1L1mol/LHCl溶液中,HCl分子的数目为NA
C.标准状况下,2.24LC2H5OH所含氢原子数为0.6NA
D.pH=12的Na2CO3溶液中OH-数目为0.01NA
E.1.12LC2H4所含极性共价键的数目为0.2NA
F.0.1mol·L-1HClO4溶液中含有的H+数为0.1NA
G.11.2LNO与11.2LO2混合后的分子数目为NA
H.11.2L乙烷和丙烯的混合气体中所含碳氢键数为3NA
A.25℃、101kPa下,28L氢气中质子的数目为2.5NA
B.1L1mol/LHCl溶液中,HCl分子的数目为NA
C.标准状况下,2.24LC2H5OH所含氢原子数为0.6NA
D.pH=12的Na2CO3溶液中OH-数目为0.01NA
E.1.12LC2H4所含极性共价键的数目为0.2NA
F.0.1mol·L-1HClO4溶液中含有的H+数为0.1NA
G.11.2LNO与11.2LO2混合后的分子数目为NA
H.11.2L乙烷和丙烯的混合气体中所含碳氢键数为3NA
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】标准状况下,1.12 L CH4和C2H4的混合气体通入足量溴水中,溴水增重0.28克,则乙烯占混合气体的体积分数为___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献.该法利用的原理为 。根据要求回答下列问题:
。根据要求回答下列问题:
(1)同温同压下,等物质的量的 和
和 ,前者与后者的分子数之比为
,前者与后者的分子数之比为_______ ,原子总数之比为_______ ,密度之比为_______ 。
(2)与标准状况下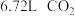 中所含的氧原子数相等的
中所含的氧原子数相等的 的质量为
的质量为_______ g,与该质量的水中所含的氢原子数相等的 在标准状况下的体积为
在标准状况下的体积为_______ L。
(3)将一定量 和
和 混合测得混合气体中碳元素与氮元素的质量之比为
混合测得混合气体中碳元素与氮元素的质量之比为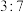 ,则该混合气体中
,则该混合气体中 与
与 物质的量之比为
物质的量之比为_______ ,该混合气体的密度是同温同压下氢气密度的_______ 倍。
 。根据要求回答下列问题:
。根据要求回答下列问题:(1)同温同压下,等物质的量的
 和
和 ,前者与后者的分子数之比为
,前者与后者的分子数之比为(2)与标准状况下
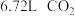 中所含的氧原子数相等的
中所含的氧原子数相等的 的质量为
的质量为 在标准状况下的体积为
在标准状况下的体积为(3)将一定量
 和
和 混合测得混合气体中碳元素与氮元素的质量之比为
混合测得混合气体中碳元素与氮元素的质量之比为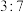 ,则该混合气体中
,则该混合气体中 与
与 物质的量之比为
物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】酸雨的pH______ (>,<,=)5.6,写出形成硫酸型酸雨的相关的化学方程式:
二氧化硫与雨水反应___________________________ ,再被氧化成硫酸 ________________ .
二氧化硫与雨水反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】简要回答下列问题。
(1)铝制器具不宜存放酸、碱溶液的原因是_____________________________ 。
(2)钢铁腐蚀给生活生产带来很多不便,并造成巨大的经济损失。请你提出一种防止钢铁腐蚀的合理措施:______________________________________________ 。
(3)工业燃煤常进行脱硫处理,其目的是________________________________________ ;
(1)铝制器具不宜存放酸、碱溶液的原因是
(2)钢铁腐蚀给生活生产带来很多不便,并造成巨大的经济损失。请你提出一种防止钢铁腐蚀的合理措施:
(3)工业燃煤常进行脱硫处理,其目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氮的氧化物是主要的大气污染物,必须脱除才能排放。
(1)臭氧与空气中的氮氧化物和_______ (填字母)在紫外线照射下产生光化学烟雾。
a.二氧化硫 b.碳氢化合物 c.二氧化碳
(2)汽车排气管内的催化剂能将CO和 转化为无害气体,发生的反应方程式为
转化为无害气体,发生的反应方程式为_______ 。
(3)工业上在催化剂作用下用 还原废气中
还原废气中 生成
生成 和
和 达到脱除目的,但当温度高于400℃时,
达到脱除目的,但当温度高于400℃时, 脱除率下降,原因可能是
脱除率下降,原因可能是_______ 。
(4)工业上氮的氧化物通常是用碱性溶液吸收。
①用 溶液吸收硝酸工业尾气中的
溶液吸收硝酸工业尾气中的 ,生成等物质的量的两种钠盐(一种为
,生成等物质的量的两种钠盐(一种为 )及一种气体,反应的离子方程式为
)及一种气体,反应的离子方程式为_______ 。
②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收 (混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量
(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量_______ (填:“大于”、“小于”、“等于”) 物质的量:当NaOH溶液浓度高于
物质的量:当NaOH溶液浓度高于 后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是_______ 。

(1)臭氧与空气中的氮氧化物和
a.二氧化硫 b.碳氢化合物 c.二氧化碳
(2)汽车排气管内的催化剂能将CO和
 转化为无害气体,发生的反应方程式为
转化为无害气体,发生的反应方程式为(3)工业上在催化剂作用下用
 还原废气中
还原废气中 生成
生成 和
和 达到脱除目的,但当温度高于400℃时,
达到脱除目的,但当温度高于400℃时, 脱除率下降,原因可能是
脱除率下降,原因可能是(4)工业上氮的氧化物通常是用碱性溶液吸收。
①用
 溶液吸收硝酸工业尾气中的
溶液吸收硝酸工业尾气中的 ,生成等物质的量的两种钠盐(一种为
,生成等物质的量的两种钠盐(一种为 )及一种气体,反应的离子方程式为
)及一种气体,反应的离子方程式为②NaOH溶液浓度越大黏稠度越高,用不同浓度的NaOH溶液吸收
 (混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量
(混有NO)含量不同的工业尾气,氮氧化物的吸收率随NaOH溶液浓度的变化如题图所示,曲线II表示NO的物质的量 物质的量:当NaOH溶液浓度高于
物质的量:当NaOH溶液浓度高于 后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
后,氮氧化物的吸收率随NaOH溶液浓度的升高而降低的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.中和热测定是中学化学重要的定量实验
(1)实验中需要的玻璃仪器有__________________________ ;
(2)现通过相同体积(100mL),相同物质的量浓度(0.2mol·L-1)的硫酸和氢氧化钠溶液反应,测定中和热,实验测得反应时,溶液温度平均升高t℃,计算中和热的表达式ΔH=___________ (假设溶液的密度,比热容与水的相同)。
II.过氧化钠是一种重要的氧化剂
(1)过氧化钠的电子式是______ ,其中含有的化学键类型是______ ;
(2)在氯化亚铁的溶液中加入与其等物质的量的Na2O2,恰好使氯化亚铁转化为氢氧化铁写出该反应的离子方程式:___________________________ 。
(1)实验中需要的玻璃仪器有
(2)现通过相同体积(100mL),相同物质的量浓度(0.2mol·L-1)的硫酸和氢氧化钠溶液反应,测定中和热,实验测得反应时,溶液温度平均升高t℃,计算中和热的表达式ΔH=
II.过氧化钠是一种重要的氧化剂
(1)过氧化钠的电子式是
(2)在氯化亚铁的溶液中加入与其等物质的量的Na2O2,恰好使氯化亚铁转化为氢氧化铁写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用脱脂棉包住0.78 g Na2O2粉末,置于石棉网上,往脱脂棉上滴1 mL水,可观察到脱脂棉剧烈燃烧起来。
(1)由实验现象可得出的结论是:Na2O2与H2O反应有氧气生成且反应为________ 反应。
(2)如果用嘴通过细管向脱脂棉中吹气,脱脂棉也能燃烧起来,试写出反应的化学方程式___________ ;若向脱脂棉中吹入的是SO2气体,脱脂棉________ (填“能”或“不能”)燃烧起来。
(3)H2和CO的混合气体0.02 g通入一盛有0.78 g Na2O2的密闭容器中,再通入过量O2,并用电火花引燃使其充分反应,容器中固体增加的质量为________ g。
(1)由实验现象可得出的结论是:Na2O2与H2O反应有氧气生成且反应为
(2)如果用嘴通过细管向脱脂棉中吹气,脱脂棉也能燃烧起来,试写出反应的化学方程式
(3)H2和CO的混合气体0.02 g通入一盛有0.78 g Na2O2的密闭容器中,再通入过量O2,并用电火花引燃使其充分反应,容器中固体增加的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)Na2O2__________ (填“是”或“否”)属于碱性氧化物,Na2O2是______ 色固体粉末。向包有Na2O2固体的棉花上滴几滴水,棉花很快燃烧起来,原因是该反应有氧气生成且该反应为__________ (填”吸热”或者“放热”)反应;
(2)Na2O2作为在潜水艇和消防员呼吸面具中的供氧剂,写出其中一个反应的化学方程式_________ ,某潜水艇中有50人,若每人每小时消耗O2在标准状况下的体积为44.8L,假设所需要的O2全由Na2O2所提供,则每小时所需Na2O2的质量为________ kg。
(3)3.1gNa2O溶于水配成1L溶液,溶液中Na+离子物质的量浓度为________
(4)制备Fe(OH)3胶体:用洁净的烧杯取一定量蒸馏水,用酒精灯加热至沸腾,向烧杯中加入几滴饱和FeCl3溶液继续加热至液体呈透明的红褐色。
①写出制备Fe(OH)3胶体反应的离子方程式______________________________
②验证制得的分散系是胶体的方法为_________________________________
(2)Na2O2作为在潜水艇和消防员呼吸面具中的供氧剂,写出其中一个反应的化学方程式
(3)3.1gNa2O溶于水配成1L溶液,溶液中Na+离子物质的量浓度为
(4)制备Fe(OH)3胶体:用洁净的烧杯取一定量蒸馏水,用酒精灯加热至沸腾,向烧杯中加入几滴饱和FeCl3溶液继续加热至液体呈透明的红褐色。
①写出制备Fe(OH)3胶体反应的离子方程式
②验证制得的分散系是胶体的方法为
您最近一年使用:0次



