实验室用下列仪器和药品制取干燥纯净的氯气.
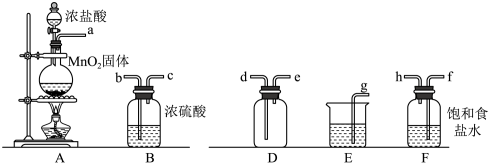
(1)按气流从左到右,装置正确的连接顺序:a接 接 接 接 接 接 接 (填各接口字母)____________
(2)装置F的作用是____ ,装置E的作用是____ .
(3)装置A和E中的反应化学方程式为(每空2分):A___ .E____ .
(4)若有8.7gMnO2参加了反应,将产生的氯气通入足量的KI溶液中能产生单质碘的质量____ g

(1)按气流从左到右,装置正确的连接顺序:a接 接 接 接 接 接 接 (填各接口字母)
(2)装置F的作用是
(3)装置A和E中的反应化学方程式为(每空2分):A
(4)若有8.7gMnO2参加了反应,将产生的氯气通入足量的KI溶液中能产生单质碘的质量
更新时间:2018-04-22 20:06:09
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图是一个实验室制取氯气并以氯气为原料进行特定反应的装置:
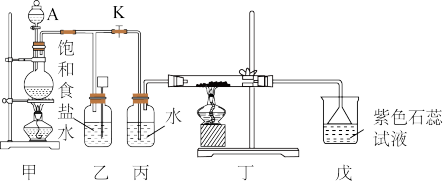
(1)仪器A的名称为__________ 。
(2)甲是氯气发生装置,其中反应的化学方程式为_________________ 。
(3)实验开始时,先点燃甲处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃丁处酒精灯,连接上戊装置。Cl2通过丙瓶后再进入丁。丁装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为CO2和HCl。试写出丁中反应的化学方程式:_______________ 。装置丙的主要作用是______________ 。
(4)若将戊处烧杯中溶液改为澄清石灰水,反应过程现象为_____ (选填标号)。
A.无明显变化 B.有白色沉淀生成 C.先生成白色沉淀,而后白色沉淀消失
(5)丁处反应完毕后,关闭旋塞K,移去酒精灯。但由于余热的作用,甲处仍有Cl2产生,此时乙中的现象是_________ ,此时,乙的作用是___________ 。

(1)仪器A的名称为
(2)甲是氯气发生装置,其中反应的化学方程式为
(3)实验开始时,先点燃甲处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃丁处酒精灯,连接上戊装置。Cl2通过丙瓶后再进入丁。丁装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为CO2和HCl。试写出丁中反应的化学方程式:
(4)若将戊处烧杯中溶液改为澄清石灰水,反应过程现象为
A.无明显变化 B.有白色沉淀生成 C.先生成白色沉淀,而后白色沉淀消失
(5)丁处反应完毕后,关闭旋塞K,移去酒精灯。但由于余热的作用,甲处仍有Cl2产生,此时乙中的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】四氯化锡(SnCl4)是合成有机锡化合物的原料,其熔点为﹣33℃,沸点为114℃,在潮湿的空气中强烈水解产生有刺激性的白色烟雾,产物之一为SnO2。实验室制备四氯化锡的操作是:将金属锡熔融,然后泼入冷水,制成锡花,将干燥的锡花加入反应器中;再向反应器中缓慢地通入干燥的氯气。

(1)I.图1是实验室制备干燥氯气的实验装置(夹持装置已略)
(1)a的仪器名称_________________ 该装置制备氯气选用的药品为漂粉精固体[主要成分Ca(ClO)2]和浓盐酸,B中发生反应的化学方程式为________________________________________
(2)装置C中饱和食盐水的作用____________________________________ 同时装置C亦是安全瓶,能检测实验进行时D中是否发生堵塞,请写出发生堵塞时C中的现象_______________________________________
(3)试剂X可能为______________ (填写字母)
A.无水氯化钙 B.浓硫酸 C.碱石灰 D.五氧化二磷
(4)四氯化锡在潮湿空气中水解的化学方程式__________________________________
(5)用锡花代替锡粒的目的是__________________________________
(2)II.(6)图2是蒸馏SnCl4的装置
①蒸馏前若发现烧瓶中液体呈黄色,可采取的措施是________________________
②该装置尚有两处不当之处,它们分别是______________ ,___________________
③写出III中发生反应的离子方程式_______________________________________

(1)I.图1是实验室制备干燥氯气的实验装置(夹持装置已略)
(1)a的仪器名称
(2)装置C中饱和食盐水的作用
(3)试剂X可能为
A.无水氯化钙 B.浓硫酸 C.碱石灰 D.五氧化二磷
(4)四氯化锡在潮湿空气中水解的化学方程式
(5)用锡花代替锡粒的目的是
(2)II.(6)图2是蒸馏SnCl4的装置
①蒸馏前若发现烧瓶中液体呈黄色,可采取的措施是
②该装置尚有两处不当之处,它们分别是
③写出III中发生反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】如图为实验室制取纯净、干燥的Cl2,并验证Cl2性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。

(1)写出实验室制取氯气的化学方程式:_______ 。
(2)装置C中盛装的溶液是_______ ,D中试剂的作用是_______ 。
(3)E中红色布条是否褪色?_______ ,F中的反应产物为_______ 。
(4)向新制氯水中滴加紫色石蕊,能观察到紫色石蕊先变红后褪色,由此可判断新制氯水的成分中含有_______ 和_______ 。
(5)若H中选用NaOH溶液进行尾气处理,则发生反应的离子方程式表示_______ 。

(1)写出实验室制取氯气的化学方程式:
(2)装置C中盛装的溶液是
(3)E中红色布条是否褪色?
(4)向新制氯水中滴加紫色石蕊,能观察到紫色石蕊先变红后褪色,由此可判断新制氯水的成分中含有
(5)若H中选用NaOH溶液进行尾气处理,则发生反应的离子方程式表示
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学小组为了研究 和
和 的漂白性,设计了如图所示的实验
的漂白性,设计了如图所示的实验

(1)盛装70%浓硫酸的仪器名称___________ 。
(2)A装置中发生反应的化学方程式是___________ 。
(3)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B试管中的液体加热,B试管中的现象是___________ ;若把B、D两个试管中的品红溶液都换为紫色石蕊溶液,B、D中的现象分别为___________ ; ___________
(4)利用下图所示装置探究两种气体按不同比例混合后漂白性的强弱。

①盛有浓硫酸洗气瓶除干燥气体且使气体充分混合外,另外一个作用是___________ ;
②实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其可能原因是___________ (用相应的化学方程式作答);
 和
和 的漂白性,设计了如图所示的实验
的漂白性,设计了如图所示的实验
(1)盛装70%浓硫酸的仪器名称
(2)A装置中发生反应的化学方程式是
(3)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B试管中的液体加热,B试管中的现象是
(4)利用下图所示装置探究两种气体按不同比例混合后漂白性的强弱。

①盛有浓硫酸洗气瓶除干燥气体且使气体充分混合外,另外一个作用是
②实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其可能原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】无水氯化铁固体呈棕褐色,易遇水潮解,100℃左右时升华,冷却后易凝华。如图是两名学生设计的用氯气与铁反应制备无水氯化铁的实验装置图。左边的反应装置(A、B、C、D)相同,而右边的产品收集(E、F)装置则不同,分别如(Ⅰ)和(Ⅱ)所示。试回答:
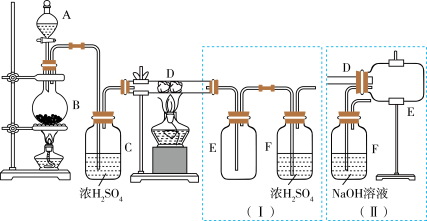
(1)B仪器的名称是___________ 。B中反应的化学方程式为___________ 。
(2)实验中点燃___________ (填“B”或“D”)下方酒精灯后,需要等到___________ 后再点燃另一处酒精灯。
(3)装置(Ⅰ)的主要缺点:___________ 、___________ ;装置(Ⅱ)F中发生反应的化学方程式为___________ 。
(4)如果选用(Ⅱ)装置来完成实验,则必须采取的改进措施是___________ 。

(1)B仪器的名称是
(2)实验中点燃
(3)装置(Ⅰ)的主要缺点:
(4)如果选用(Ⅱ)装置来完成实验,则必须采取的改进措施是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和 ,探究其氧化还原性质。回答下列问题:
,探究其氧化还原性质。回答下列问题:
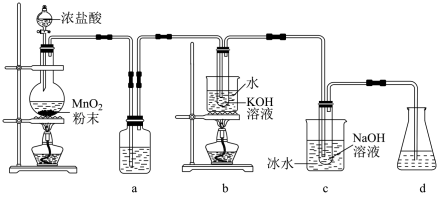
(1)盛放MnO2粉末的仪器名称是_______ ,若用含有0.2molHCl的浓盐酸与足量MnO2反应制取Cl2,制得的Cl2体积(标况)总是小于1.12L,原因可能是HCl挥发以及_______ ,利用该装置制备Cl2的离子方程式为_______ 。
(2)a中的试剂为_______ ,c中化学反应的离子方程式是_______ 。
(3)d的作用是_______ ,可选用试剂_______ (填标号)。
A. H2O B. NaCl C. Ca(OH)2 D. H2SO4
(4)在硫酸溶液中,KClO3和K2SO3能按粒子个数比1∶2完全反应,生成一种棕黄色气体Cl2O,同时K2SO3转化为K2SO4,则该反应的离子方程式为_______ 。
 ,探究其氧化还原性质。回答下列问题:
,探究其氧化还原性质。回答下列问题:
(1)盛放MnO2粉末的仪器名称是
(2)a中的试剂为
(3)d的作用是
A. H2O B. NaCl C. Ca(OH)2 D. H2SO4
(4)在硫酸溶液中,KClO3和K2SO3能按粒子个数比1∶2完全反应,生成一种棕黄色气体Cl2O,同时K2SO3转化为K2SO4,则该反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学小组制取氯酸钾并进行有关探究实验。
I.制取氯酸钾
利用如图所示的实验装置进行实验。回答下列问题:
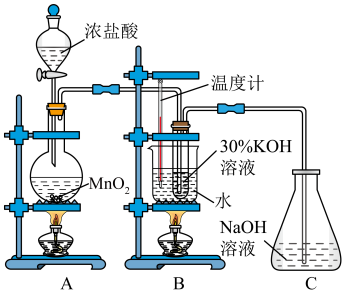
(1)装置C中盛装NaOH溶液仪器的名称是___________ 。
(2)装置A中发生反应的化学方程式为___________ 。
(3)若装置B中加热温度过低,所得主要氧化产物为___________ (填化学式)。已知氯酸钾和氯化钾的溶解度曲线如图所示,反应结束后,从装置B所得溶液中提取氯酸钾晶体的实验操作是___________ 、___________ 、过滤、干燥。

II.探究氯酸钾与碘化钾的反应
(4)在不同条件下KClO3可将KI氧化为I2或KIO3。室温下,该小组设计了系列实验研究硫酸浓度对反应产物的影响,实验记录如下表:
①3号试管实验中x的值为___________ ;1号试管实验的作用是___________ 。
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为___________ 。
③由该系列实验可得出的结论是___________ 。
I.制取氯酸钾
利用如图所示的实验装置进行实验。回答下列问题:

(1)装置C中盛装NaOH溶液仪器的名称是
(2)装置A中发生反应的化学方程式为
(3)若装置B中加热温度过低,所得主要氧化产物为

II.探究氯酸钾与碘化钾的反应
(4)在不同条件下KClO3可将KI氧化为I2或KIO3。室温下,该小组设计了系列实验研究硫酸浓度对反应产物的影响,实验记录如下表:
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol·L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol·L-1H2SO4/mL | 0 | 3.0 | x | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 4.0 | 0 |
| 取少量反应后溶液滴加淀粉溶液 | 无现象 | 变蓝 | 变蓝 | 无现象 |
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为
③由该系列实验可得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】如图为实验室制取纯净、干燥的Cl2,并验证Cl2性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。

(1)写出实验室制取氯气的化学方程式:_______ 。
(2)装置C中盛装的溶液是_______ ,D中试剂的作用是_______ 。
(3)E中红色布条是否褪色?_______ ,F中的反应产物为_______ 。
(4)向新制氯水中滴加紫色石蕊,能观察到紫色石蕊先变红后褪色,由此可判断新制氯水的成分中含有_______ 和_______ 。
(5)若H中选用NaOH溶液进行尾气处理,则发生反应的离子方程式表示_______ 。

(1)写出实验室制取氯气的化学方程式:
(2)装置C中盛装的溶液是
(3)E中红色布条是否褪色?
(4)向新制氯水中滴加紫色石蕊,能观察到紫色石蕊先变红后褪色,由此可判断新制氯水的成分中含有
(5)若H中选用NaOH溶液进行尾气处理,则发生反应的离子方程式表示
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。某化学兴趣小组同学对氯气的性质进行如下探究:
(1)兴趣小组同学按下图装置进行实验,探究Cl2 的漂白性。
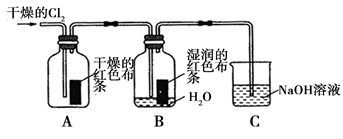
①通入Cl2 后,观察到的现象是_______ 根据现象可得出的结论是_____ 。
②集气瓶B发生反应的离子方程式是_____ 。
③C装置的作用是___________ ,若有2.24L(标准状况下)Cl2被NaOH溶液完全吸收,则反应过程中转移的电子为_______ mol。
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。
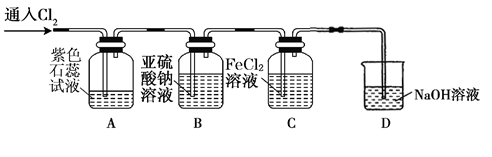
①实验开始后,观察装置A 中的现象是_____ 。
②装置C中发生反应的离子方程式是______ 。
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2 时装置B中发生 反应的离子方程式是__________ 。
(1)兴趣小组同学按下图装置进行实验,探究Cl2 的漂白性。

①通入Cl2 后,观察到的现象是
②集气瓶B发生反应的离子方程式是
③C装置的作用是
(2)兴趣小组同学按下图装置进行实验,探究Cl2的氧化性。

①实验开始后,观察装置A 中的现象是
②装置C中发生反应的离子方程式是
③停止通入氯气,取装置B中少量溶液于洁净的试管中,向其中滴加足量稀盐酸,再向其中滴加氯化钡溶液,有白色沉淀生成。则通入Cl2 时装置B中发生 反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中加热,充分应后得到溶液X并收集到气体Y。
(1)甲同学认为X中除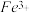 外还可能含有
外还可能含有 。若要确认其中的
。若要确认其中的 ,应选用
,应选用____ 填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液
C.浓氨水 D.酸性 溶液
丙同学认为气体Y中除 外还可能含量有
外还可能含量有 和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。
和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。
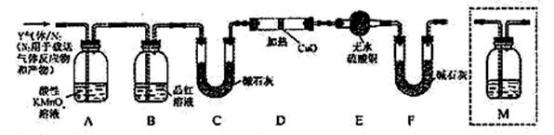
(2)装置B中试剂的作用是___________ 。
(3)认为气体Y中还含有Q的理由是___________ (用化学方程式表示)。
(4)为确认Q的存在,需在装置中添加M于____________ (选填序号)。
a. A之前 b.A-B间 c.B-C间 d.C-D间
(5)如果气体Y中含有H2,预计实验现象应是___________ 。
(1)甲同学认为X中除
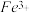 外还可能含有
外还可能含有 。若要确认其中的
。若要确认其中的 ,应选用
,应选用A.KSCN溶液和氯水 B.铁粉和KSCN溶液
C.浓氨水 D.酸性 溶液
丙同学认为气体Y中除
 外还可能含量有
外还可能含量有 和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。
和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。
(2)装置B中试剂的作用是
(3)认为气体Y中还含有Q的理由是
(4)为确认Q的存在,需在装置中添加M于
a. A之前 b.A-B间 c.B-C间 d.C-D间
(5)如果气体Y中含有H2,预计实验现象应是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氮化铝(AlN)是一种新型的无机非金属材料,工业上由氧化铝与焦炭在氮气流中高温制得。请回答下列有关问题。
(1)氮化铝(AlN)制备:Al2O3+N2+3C 2AlN+3CO,反应中氧化产物与还原产物的物质的量之比为
2AlN+3CO,反应中氧化产物与还原产物的物质的量之比为_______ 。
(2)AlN产品中常含有Al4C3、碳和Al2O3等杂质,已知Al4C3与水反应生成CH4,CH4与CuO发生反应:CH4+4CuO CO2+2H2O+4Cu。为测定产品中有关成分的含量,所需仪器如下:
CO2+2H2O+4Cu。为测定产品中有关成分的含量,所需仪器如下:
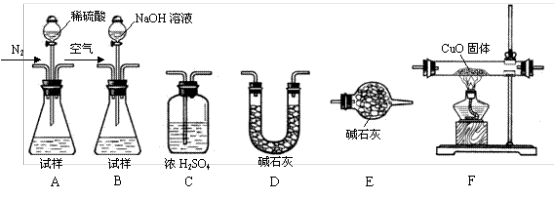
【测定样品中Al4C3的含量】
若各装置连接的顺序为:A→C→F→C→D→E,请补充操作步骤:
①称量D的质量,按顺序组装仪器,检查装置的气密性,将试样放入锥形瓶中;
②______ ;③______ ;④______ ;⑤______ ;⑥再次称量D的质量;
⑦重复步骤⑤和⑥的操作,直到D的质量基本不变。
【测定AlN的含量】
已知AlN能够水解,请选择合适的药品和装置,按气流方向连接各装置,其顺序为:
______ →______ →______ →E。若试样为mg ,测得C增重n g,则AlN的质量分数是______ 。
(1)氮化铝(AlN)制备:Al2O3+N2+3C
 2AlN+3CO,反应中氧化产物与还原产物的物质的量之比为
2AlN+3CO,反应中氧化产物与还原产物的物质的量之比为(2)AlN产品中常含有Al4C3、碳和Al2O3等杂质,已知Al4C3与水反应生成CH4,CH4与CuO发生反应:CH4+4CuO
 CO2+2H2O+4Cu。为测定产品中有关成分的含量,所需仪器如下:
CO2+2H2O+4Cu。为测定产品中有关成分的含量,所需仪器如下:
【测定样品中Al4C3的含量】
若各装置连接的顺序为:A→C→F→C→D→E,请补充操作步骤:
①称量D的质量,按顺序组装仪器,检查装置的气密性,将试样放入锥形瓶中;
②
⑦重复步骤⑤和⑥的操作,直到D的质量基本不变。
【测定AlN的含量】
已知AlN能够水解,请选择合适的药品和装置,按气流方向连接各装置,其顺序为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】碱式碳酸镍[Nix(OH)y(CO3)z·nH2O]是一种绿色粉末,常用作催化剂和陶瓷着色剂,300 ℃以上时分解生成 3 种氧化物。为确定其组成,某同学在实验室进行了有关的探究。 请回答下列问题:
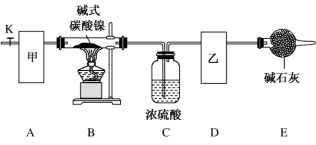
(1)装置 E 中仪器的名称是_____ 。
(2)甲、乙两装置可分别选取下列装置_____ 、_____ (填字母,装置可重复选取)。

(3) 安装好实验仪器,检查装置气密性;称取一定量的碱式碳酸镍样品,放入硬质玻璃管内; 加热硬质玻璃管,当装置 C 中_____ (填实验现象)时,停止加热;打开活塞 K,缓缓通入一段时间空气后,结束实验。
(4)装置 A 的作用是______________________________________________________________________ 。
(5)实验前后测得下表所示数据:
已知碱式碳酸镍中 Ni 化合价为+2 价,则该碱式碳酸镍的化学式为_______________________________ 。

(1)装置 E 中仪器的名称是
(2)甲、乙两装置可分别选取下列装置

(3) 安装好实验仪器,检查装置气密性;称取一定量的碱式碳酸镍样品,放入硬质玻璃管内; 加热硬质玻璃管,当装置 C 中
(4)装置 A 的作用是
(5)实验前后测得下表所示数据:
| 装置 B 中样品质量/g | 装置 C 质量/g | 装置 D 质量/g | |
| 实验前 | 3.77 | 132.00 | 41.00 |
| 实验后 | 2.25 | 133.08 | 41.44 |
已知碱式碳酸镍中 Ni 化合价为+2 价,则该碱式碳酸镍的化学式为
您最近一年使用:0次



