化学学习和研究离不开元素周期表。下表为元素周期表的一部分,表中①-⑩分别代表一种元素。回答下列问题:
(1)上述元素中,有一种元素在自然界中形成的物质种类最多,该元素在周期表中的位置是_______ 。
(2)⑧、⑨、⑩元素的离子半径由大到小的顺序为________________ (用离子符号表示)。
(3)写出由①、⑥、⑧三种元素形成的一种离子化合物的电子式__________________ 。
(4)上述元素中有一种元素的氧化物和氢氧化物都有两性,面出该元素的原子结构示意图______________ ;高温条件下,该元素的单质与铁红能发生反应,此反应常用于野外焊接钢轨,则该反应的能量变化可用图__________________ 表示。(填“甲“或“乙”)

(5)已知W+X→Y+Z,且W、X、Y、Z分别是由①、⑤、⑥三种元素中的两种形成的10电子粒子,写出并配平上述反应式_________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 3 | ⑧ | ⑨ | ⑩ |
(2)⑧、⑨、⑩元素的离子半径由大到小的顺序为
(3)写出由①、⑥、⑧三种元素形成的一种离子化合物的电子式
(4)上述元素中有一种元素的氧化物和氢氧化物都有两性,面出该元素的原子结构示意图

(5)已知W+X→Y+Z,且W、X、Y、Z分别是由①、⑤、⑥三种元素中的两种形成的10电子粒子,写出并配平上述反应式
更新时间:2018-04-27 21:40:55
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。回答下列问题:
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原产物为_____ 。
(2)Ti-Fe合金室温下吸、放氢的速率快,Ti元素在周期表中的位置是____ 。
(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成。
进行合成。
① 中涉及的元素H、B、N电负性最大的是
中涉及的元素H、B、N电负性最大的是______ 。
②键角:
_____  (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是_______ 。
(4)Fe-Mg合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
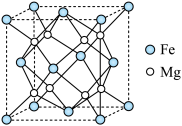
①距离Mg原子最近的Fe原子个数是___________ 。
②若该晶胞的棱长为anm,阿伏加德罗常数的值为 ,则该合金的密度为
,则该合金的密度为___________  。
。
③若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的体积约为
的体积约为___________ L。
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原产物为
(2)Ti-Fe合金室温下吸、放氢的速率快,Ti元素在周期表中的位置是
(3)
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成。
进行合成。①
 中涉及的元素H、B、N电负性最大的是
中涉及的元素H、B、N电负性最大的是②键角:

 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是(4)Fe-Mg合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离Mg原子最近的Fe原子个数是
②若该晶胞的棱长为anm,阿伏加德罗常数的值为
 ,则该合金的密度为
,则该合金的密度为 。
。③若该晶体储氢时,
 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的体积约为
的体积约为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】硼和硅在周期表中处于对角线上,有许多相似的性质。回答下列问题:
(1)①基态硅原子的价层电子排布式为___________ 。
②已知 比
比 更易水解,不能解释这一事实的是
更易水解,不能解释这一事实的是___________ (填标号)。
A. 键极性更大 B.
键极性更大 B. 的原子半径更大
的原子半径更大
C. 键键能更大 D.
键键能更大 D. 有更多的价层轨道
有更多的价层轨道
(2)硼与硅相似,也能与氢形成一类化合物——硼烷。常见的有乙硼烷( )、丁硼烷(
)、丁硼烷( )、己硼烷(
)、己硼烷( )等。
)等。
①乙硼烷的结构式如图。分子中B原子通过氢桥键( )形成一个四元环。
)形成一个四元环。

丁硼烷( )分子中存在4个氢桥键且有两个五元环,写出其结构式
)分子中存在4个氢桥键且有两个五元环,写出其结构式___________ 。
②下列说法错误的是___________ 。
A.在自然界中没有游离态的硼,它易与氧化合形成含氧矿物
B.硼烷的通式为
C.氮元素的第二电离能大于氧元素
D. 与
与 中心原子的杂化方式相同
中心原子的杂化方式相同
(3)①液氨有类似于水的性质,能发生自耦电离。已知: ,写出
,写出 在液氨中氨解的化学方程式
在液氨中氨解的化学方程式___________ 。
②氨基磺酸(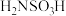 )与氨基酸类似,是两性化合物,能与酸、碱反应生成盐。预测其熔点大于
)与氨基酸类似,是两性化合物,能与酸、碱反应生成盐。预测其熔点大于 ,理由是
,理由是___________ 。
(4)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,该物质的化学式为___________ , 最近距离为
最近距离为___________ 。

(1)①基态硅原子的价层电子排布式为
②已知
 比
比 更易水解,不能解释这一事实的是
更易水解,不能解释这一事实的是A.
 键极性更大 B.
键极性更大 B. 的原子半径更大
的原子半径更大C.
 键键能更大 D.
键键能更大 D. 有更多的价层轨道
有更多的价层轨道(2)硼与硅相似,也能与氢形成一类化合物——硼烷。常见的有乙硼烷(
 )、丁硼烷(
)、丁硼烷( )、己硼烷(
)、己硼烷( )等。
)等。①乙硼烷的结构式如图。分子中B原子通过氢桥键(
 )形成一个四元环。
)形成一个四元环。
丁硼烷(
 )分子中存在4个氢桥键且有两个五元环,写出其结构式
)分子中存在4个氢桥键且有两个五元环,写出其结构式②下列说法错误的是
A.在自然界中没有游离态的硼,它易与氧化合形成含氧矿物
B.硼烷的通式为

C.氮元素的第二电离能大于氧元素
D.
 与
与 中心原子的杂化方式相同
中心原子的杂化方式相同(3)①液氨有类似于水的性质,能发生自耦电离。已知:
 ,写出
,写出 在液氨中氨解的化学方程式
在液氨中氨解的化学方程式②氨基磺酸(
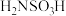 )与氨基酸类似,是两性化合物,能与酸、碱反应生成盐。预测其熔点大于
)与氨基酸类似,是两性化合物,能与酸、碱反应生成盐。预测其熔点大于 ,理由是
,理由是(4)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,该物质的化学式为
 最近距离为
最近距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】1869年俄国化学家门捷列夫制出第一张元素周期表。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。回答下列问题:
(1)元素Se在元素周期表中的位置为____________ (写明周期数和族序数),汞是80号元素,原子结构示意图如图,汞在第________________ 周期。

(2)Ge的最高正价为____________ ,Bi的最高价氧化物为____________ (填化学式)。
(3)根据元素周期律推断:
①氢化物稳定性最强的卤族元素是____________ (填元素符号)。
② 、
、 的酸性强弱:
的酸性强弱:
____________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③氢化物的还原性:
____________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)过渡元素中可以寻找到 (填序号)。
(5)① 常用作溶剂,其电子式为
常用作溶剂,其电子式为____________ ,分子空间构型为____________ 。
②镓( )的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是
)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是____________ (填序号)。
A.原子半径: B.N的非金属性比O强 C.Ga的金属性比Al弱 D.As和Sb的氧化物可能是两性氧化物
B.N的非金属性比O强 C.Ga的金属性比Al弱 D.As和Sb的氧化物可能是两性氧化物
(6)甲烷可直接应用于燃料电池,该电池采用可传导 的固体氧化物为电解质,其工作原理如图所示:
的固体氧化物为电解质,其工作原理如图所示:
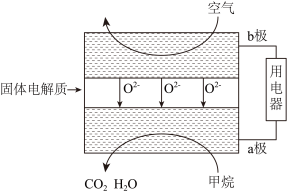
①外电路电子移动方向:__________________ (填“a极到b极”或“b极到a极”)。
②若燃料电池消耗的空气在标准状况下的体积是5.6L(假设空气中 体积分数为20%),则理论上消耗甲烷
体积分数为20%),则理论上消耗甲烷________ mol。
(1)元素Se在元素周期表中的位置为

(2)Ge的最高正价为
(3)根据元素周期律推断:
①氢化物稳定性最强的卤族元素是
②
 、
、 的酸性强弱:
的酸性强弱:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③氢化物的还原性:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)过渡元素中可以寻找到 (填序号)。
| A.农药 | B.黑色金属 | C.半导体材料 | D.优良的催化剂 |
 常用作溶剂,其电子式为
常用作溶剂,其电子式为②镓(
 )的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是
)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是A.原子半径:
 B.N的非金属性比O强 C.Ga的金属性比Al弱 D.As和Sb的氧化物可能是两性氧化物
B.N的非金属性比O强 C.Ga的金属性比Al弱 D.As和Sb的氧化物可能是两性氧化物(6)甲烷可直接应用于燃料电池,该电池采用可传导
 的固体氧化物为电解质,其工作原理如图所示:
的固体氧化物为电解质,其工作原理如图所示:
①外电路电子移动方向:
②若燃料电池消耗的空气在标准状况下的体积是5.6L(假设空气中
 体积分数为20%),则理论上消耗甲烷
体积分数为20%),则理论上消耗甲烷
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】X、Y、Z、W四种元素在元素周期表中序数逐渐增大。X为非金属元素,且X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z、W的元素符号分别是:________ 、________ 、________ 、__________ 。
(2)W的最高价氧化物对应的水化物的电子式为_____ 。Y的气态氢化物的结构式为_______ 。
(3)写出Y的最高价氧化物对应的水化物与W的最高价氧化物对应的水化物反应的离子方程式____________________________ 。
(1)X、Y、Z、W的元素符号分别是:
(2)W的最高价氧化物对应的水化物的电子式为
(3)写出Y的最高价氧化物对应的水化物与W的最高价氧化物对应的水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】表中的实线表示当前元素周期表的边界。①~⑩分别表示元素周期表中对应位置的元素。
(1)元素⑧在周期表的位置是_______ ;元素①-⑩中,非金属性最强的是_______ (用元素符号表示);元素④-⑦中,简单离子半径最小的是_______ (用离子符号表示)。
(2)元素①和④组成化合物的电子式为_______ ;元素③-⑦中,最高价氧化物对应水化物的酸性最强的为_______ (用化学式表示)。
(3)元素⑤在生产生活中有重要用途,写出工业制取其单质的化学方程式_______ 。
(4)已知一定条件下,4 g 元素⑥的固态单质在元素②的过量单质中充分燃烧反应放热a kJ。写出此条件下该反应的热化学方程式_______ 。
(5)用离子交换膜控制电解液中 c(OH-)制备由②⑨组成的纳米材料 Cu2O,其装置如图:
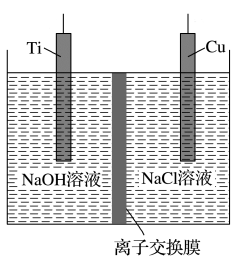
该电解池的阳极反应式为_______ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ||||||||||||||
| ⑧ | ⑨ | ||||||||||||||||
| ⑩ |
(2)元素①和④组成化合物的电子式为
(3)元素⑤在生产生活中有重要用途,写出工业制取其单质的化学方程式
(4)已知一定条件下,4 g 元素⑥的固态单质在元素②的过量单质中充分燃烧反应放热a kJ。写出此条件下该反应的热化学方程式
(5)用离子交换膜控制电解液中 c(OH-)制备由②⑨组成的纳米材料 Cu2O,其装置如图:

该电解池的阳极反应式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表标出的是元素周期表的一部分元素,回答下列问题:
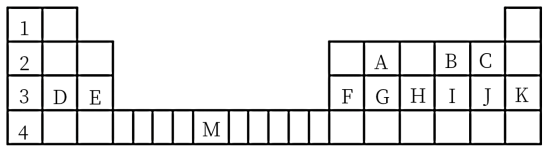
(1)除稀有气体外第三周期中原子半径最大的是___________ (填元素符号)
(2)表中用字母标出的12种元素中,化学性质最不活泼的是___________ (用元素符号表示,下同),非金属性最强的是___________ (用元素符号表示),属于过渡元素的是___________ (用表中的字母表示)。
(3)化合物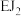 中含有的化学键为
中含有的化学键为___________ 。(填“离子键’”、“极性共价键”、“非极性共价键”)
(4)用电子式表示A的简单气态氢化物的形成过程___________ 。
(5)D、F元素最高价氧化物对应水化物相互反应的离子方程式为___________

(1)除稀有气体外第三周期中原子半径最大的是
(2)表中用字母标出的12种元素中,化学性质最不活泼的是
(3)化合物
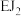 中含有的化学键为
中含有的化学键为(4)用电子式表示A的简单气态氢化物的形成过程
(5)D、F元素最高价氧化物对应水化物相互反应的离子方程式为
您最近一年使用:0次



