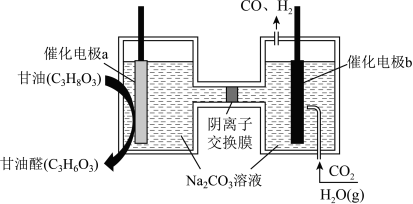
Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产Na2FeO4,下列有关说法不正确的是


| A.右侧电极反应方程式:Fe+8OH--6e-=FeO42-+4H2O |
| B.左侧为阳离子交换膜,当Cu电极生成1mol气体时,有2molNa+通过阳离子交换膜 |
| C.可以将左侧流出的氢氧化钠补充到该装置中部,以保证装置连续工作 |
| D.Na2FeO4具有强氧化性且产物为Fe3+,因此可以利用Na2FeO4除去水中的细菌、固体颗粒以及Ca2+等 |
更新时间:2018-05-13 17:10:27
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】二氧化氯、铁酸钠以及次氯酸是饮用水的“三净客”,用铁酸钠(Na2FeO4)处理来自河流湖泊的水,以作为人们生活饮用水,是一项较新的技术。以下叙述中正确的是
① Na2FeO4溶液有强酸性 ② Na2FeO4溶液有强氧化性
③ Na2FeO4溶液有强还原性 ④该过程中水既被消毒又被净化
① Na2FeO4溶液有强酸性 ② Na2FeO4溶液有强氧化性
③ Na2FeO4溶液有强还原性 ④该过程中水既被消毒又被净化
| A.①③ | B.③④ | C.①② | D.②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾( )是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,微溶于浓KOH溶液,且能与水反应放出氧气,并生成
)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,微溶于浓KOH溶液,且能与水反应放出氧气,并生成 胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下其氧化性强于
胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下其氧化性强于 、
、 等。下列关于
等。下列关于 的说法不正确的是
的说法不正确的是
 )是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,微溶于浓KOH溶液,且能与水反应放出氧气,并生成
)是一种暗紫色固体,低温碱性条件下比较稳定。高铁酸钾能溶于水,微溶于浓KOH溶液,且能与水反应放出氧气,并生成 胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下其氧化性强于
胶体,常用作水处理剂。高铁酸钾有强氧化性,酸性条件下其氧化性强于 、
、 等。下列关于
等。下列关于 的说法不正确的是
的说法不正确的是A.将 与盐酸混合使用,可增强其杀菌消毒效果 与盐酸混合使用,可增强其杀菌消毒效果 |
B.与水反应,每消耗1mol  转移3mol电子 转移3mol电子 |
C. 用作水处理剂时,既能杀菌消毒,又能吸附悬浮杂质 用作水处理剂时,既能杀菌消毒,又能吸附悬浮杂质 |
D. 中,基态 中,基态 的核外电子排布为 的核外电子排布为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】工业是制取高铁酸钾(K2FeO4),是先制取高铁酸钠,然后在低温下,往高铁酸钠溶液中加入KOH至饱和就可以析出高铁酸钾。湿法制备Na2FeO4的主要反应为:2Fe(OH)3+3ClO-+4OH﹣=2 +3Cl﹣+5H2O;干法备Na2FeO4的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是
+3Cl﹣+5H2O;干法备Na2FeO4的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是
 +3Cl﹣+5H2O;干法备Na2FeO4的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是
+3Cl﹣+5H2O;干法备Na2FeO4的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2SO4+O2↑。下列有关说法不正确的是| A.湿法和干法制备中,生成1 mol Na2FeO4转移电子数目不相同 |
| B.高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小 |
| C.干法制备的主要反应中Na2O2只做氧化剂 |
| D.K2FeO4处理水时,既能杀菌消毒,生成的Fe(OH)3胶体还能吸附水中的悬浮杂质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】鹤壁高中化学组老师们,积极参与理化学科的跨学科备课,组装了如图A、B、C三个装置,并用导线先将A、B两槽并联,再与C槽串联,当6号电极减少0.128g时,1号电极增加了0.108g,则下列说法中错误的是
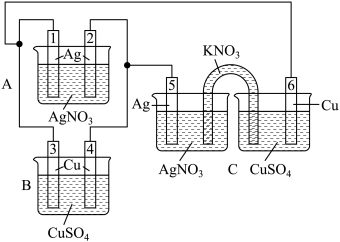

| A.盐桥中K+向左移动 | B.6号电极减少的质量大于4号电极减少的质量 |
| C.3号电极将减轻0.096g | D.A、B烧杯内溶液浓度不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某充电宝锂离子电池的总反应为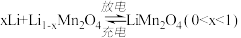 。某手机镍氢电池总反应为
。某手机镍氢电池总反应为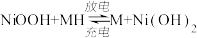 (M为储氢金属或合金),有关上述两种电池的说法错误的是
(M为储氢金属或合金),有关上述两种电池的说法错误的是
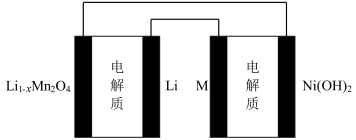
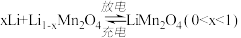 。某手机镍氢电池总反应为
。某手机镍氢电池总反应为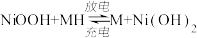 (M为储氢金属或合金),有关上述两种电池的说法错误的是
(M为储氢金属或合金),有关上述两种电池的说法错误的是
| A.锂离子电池放电时,Li+移向正极 |
| B.如图表示用锂离子电池给镍氢电池充电 |
C.锂离子电池充电时,阴极的电极反应式: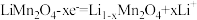 |
D.镍氢电池放电时,正极的电极反应式: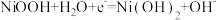 |
您最近一年使用:0次