锌的化合物在工农业生产中有广泛的应用。请回答下列问题:
(1)基态锌原子中,核外电子占据的最高能级的符号是_________ 。锌的熔点比铝的熔点低,原因是______________ 。
(2)锌冶炼过程中会产生污染性气体二氧化硫,已知液态二氧化硫可以发生类似于水的自身电离2SO2(l) SO2++
SO2++ ,S和O两种元素中电负性较强的是
,S和O两种元素中电负性较强的是_______ ,与SO2+互为等电子体的单质分子为_______ (填化学式),SO2+中的σ键和π键数目比为______________ 。
(3) [Zn(CN)4]2−在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2−+4H++4H2O [Zn(H2O)4]2++4HOCH2CN,HOCH2CN分子中碳原子轨道的杂化类型是
[Zn(H2O)4]2++4HOCH2CN,HOCH2CN分子中碳原子轨道的杂化类型是_________ ,HCHO的立体构型为_______________ ,[Zn(CN)4]2−中Zn2+与CN−中的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2−的结构可用示意图表示为__________________ 。
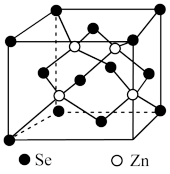
(4)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为_________ 。若该晶胞密度为ρ g·cm−3,硒化锌的摩尔质量为M g/mol,NA代表阿伏伽德罗常数,则晶胞参数a为__________ cm。
(1)基态锌原子中,核外电子占据的最高能级的符号是
(2)锌冶炼过程中会产生污染性气体二氧化硫,已知液态二氧化硫可以发生类似于水的自身电离2SO2(l)
 SO2++
SO2++ ,S和O两种元素中电负性较强的是
,S和O两种元素中电负性较强的是(3) [Zn(CN)4]2−在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2−+4H++4H2O
 [Zn(H2O)4]2++4HOCH2CN,HOCH2CN分子中碳原子轨道的杂化类型是
[Zn(H2O)4]2++4HOCH2CN,HOCH2CN分子中碳原子轨道的杂化类型是(4)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为

2018高三·全国·专题练习 查看更多[2]
更新时间:2018-05-18 13:05:49
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】[化学—选修3;物质结构与性质]
明朝《天工开物》中有世界上最早的关于炼锌技术的记载,锌也是人体必需的微量元素。回答下列问题:
(1)基态Zn原子核外的最高能层符号是________ ,基态Zn2+最外层电子排布式为________ 。
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①组成[Zn(NH3)4]SO4的元素中,除Zn外其余元素的电负性由大到小排序为________ 。
②向[Zn(NH3)4]SO4溶液中逐滴滴加NaOH溶液,未出现浑浊,其原因是________ 。
③已知[Zn(NH3)4]2+的空间构型与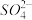 相同,则在[Zn(NH3)4]2+中Zn2+的杂化类型为
相同,则在[Zn(NH3)4]2+中Zn2+的杂化类型为________ ,NH3易液化的原因是________________________________ 。
④在[Zn(NH3)4]SO4晶体中存在的作用力有________ 。
A.离子键 B.极性共价键 C.氢键
D.配位键 E.范德华力 F.金属键
(3)ZnO与ZnS结构相似,ZnO的熔点为1975℃,ZnS的熔点约为1700℃。ZnO熔点比ZnS高的原因是________________________________ 。
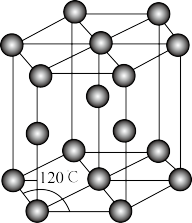
(4)常温下金属锌晶体的晶胞为六方最密堆积(如图所示),若锌原子的半径为rnm,六棱柱的高为 ,则金属锌晶体的空间利用率是
,则金属锌晶体的空间利用率是________ (用含π的代数式表示)。
明朝《天工开物》中有世界上最早的关于炼锌技术的记载,锌也是人体必需的微量元素。回答下列问题:
(1)基态Zn原子核外的最高能层符号是
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①组成[Zn(NH3)4]SO4的元素中,除Zn外其余元素的电负性由大到小排序为
②向[Zn(NH3)4]SO4溶液中逐滴滴加NaOH溶液,未出现浑浊,其原因是
③已知[Zn(NH3)4]2+的空间构型与
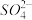 相同,则在[Zn(NH3)4]2+中Zn2+的杂化类型为
相同,则在[Zn(NH3)4]2+中Zn2+的杂化类型为④在[Zn(NH3)4]SO4晶体中存在的作用力有
A.离子键 B.极性共价键 C.氢键
D.配位键 E.范德华力 F.金属键
(3)ZnO与ZnS结构相似,ZnO的熔点为1975℃,ZnS的熔点约为1700℃。ZnO熔点比ZnS高的原因是
(4)常温下金属锌晶体的晶胞为六方最密堆积(如图所示),若锌原子的半径为rnm,六棱柱的高为
 ,则金属锌晶体的空间利用率是
,则金属锌晶体的空间利用率是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氟及其化合物用途十分广泛,回答下列问题:
(1)CuF的熔点为1008℃,熔化呈液态时能导电。CuCl的熔点为326℃,能升华,熔化呈液态时不导电;
①CuF中Cu+的基态价电子排布图为:_______ , 铜元素位于元素周期表_______ 区;
②CuF的熔点比CuCl的高,原因是_______ 。
(2)[H2F]+[SbF6]-(氟锑酸 是一种超强酸,阳离子
是一种超强酸,阳离子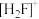 的空间构型为
的空间构型为_______ 。基态氟原子核外电子占据最高能级的电子云形状为_______ 形。
(3)工业上电解 制取单质铝,常利用冰晶石
制取单质铝,常利用冰晶石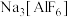 降低
降低 的熔点。通常将Al(OH)3和Na2CO3一同溶于氢氟酸来制取冰晶石,反应时放出CO2气体,写出该反应的化学方程式:
的熔点。通常将Al(OH)3和Na2CO3一同溶于氢氟酸来制取冰晶石,反应时放出CO2气体,写出该反应的化学方程式: _______ ;
(4)硒化锌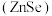 是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为(0,0,0),B点坐标为
是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为(0,0,0),B点坐标为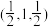 ,则 D点坐标为
,则 D点坐标为_______ 。
(甲)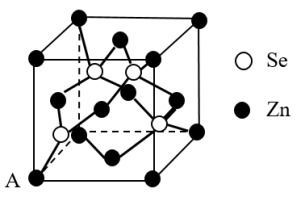 (乙)
(乙)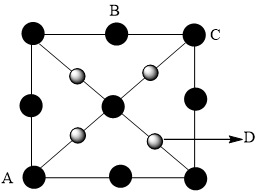
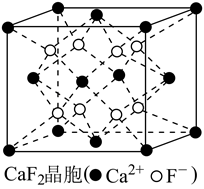
(5)CaF2的晶胞如图所示,密度为 ,相邻的两个
,相邻的两个 的最近核间距为a nm,则
的最近核间距为a nm,则 的摩尔质量为
的摩尔质量为_______ g/mol  列出代数式,设
列出代数式,设 为阿伏加德罗常数的值
为阿伏加德罗常数的值 。
。
(1)CuF的熔点为1008℃,熔化呈液态时能导电。CuCl的熔点为326℃,能升华,熔化呈液态时不导电;
①CuF中Cu+的基态价电子排布图为:
②CuF的熔点比CuCl的高,原因是
(2)[H2F]+[SbF6]-(氟锑酸
 是一种超强酸,阳离子
是一种超强酸,阳离子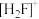 的空间构型为
的空间构型为(3)工业上电解
 制取单质铝,常利用冰晶石
制取单质铝,常利用冰晶石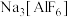 降低
降低 的熔点。通常将Al(OH)3和Na2CO3一同溶于氢氟酸来制取冰晶石,反应时放出CO2气体,写出该反应的化学方程式:
的熔点。通常将Al(OH)3和Na2CO3一同溶于氢氟酸来制取冰晶石,反应时放出CO2气体,写出该反应的化学方程式: (4)硒化锌
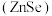 是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为(0,0,0),B点坐标为
是一种重要的半导体材料,其晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为(0,0,0),B点坐标为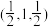 ,则 D点坐标为
,则 D点坐标为(甲)
 (乙)
(乙)
(5)CaF2的晶胞如图所示,密度为
 ,相邻的两个
,相邻的两个 的最近核间距为a nm,则
的最近核间距为a nm,则 的摩尔质量为
的摩尔质量为 列出代数式,设
列出代数式,设 为阿伏加德罗常数的值
为阿伏加德罗常数的值 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】近期央视以《王者归“铼”》为专题报道了中国金属铼加工领域的最新成就,即用金属铼造出了航空发动机核心部件,打破了西方国家的技术封锁。已知铼在元素周期表中呈现的信息如下,回答下列问题:
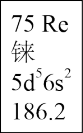
(1)铼元素位于元素周期表的的位置为______ ,位于________ 区。
(2)基态Re原子核外有_____ 种不同运动状态的电子,其中核外电子占据最高能层的符号是______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(3)已知Ba与Re位于同一周期,且核外最外层电子数相同,但金属Ba的熔点、沸点都比金属Re的低,原因是________ 。
(4)铼的许多有机配合物是电致发光材料,已知配合物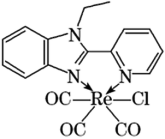 具有MLCT发射性质,该配合物中,与N原子直接相连的苯环上的C原子的杂化类型为
具有MLCT发射性质,该配合物中,与N原子直接相连的苯环上的C原子的杂化类型为_______ ,写出与配体CO互为等电子体的离子:_________ 。
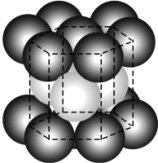
(5)已知金属Re的一种晶胞结构如图所示,则该晶胞与Mg的堆积方式相同为_______ 堆积,Re原子的配位数为_______ ,若Re原子的半径为r nm,则晶体的密度是_______ g·cm-3(用含r的代数式表示)。
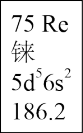
(1)铼元素位于元素周期表的的位置为
(2)基态Re原子核外有
(3)已知Ba与Re位于同一周期,且核外最外层电子数相同,但金属Ba的熔点、沸点都比金属Re的低,原因是
(4)铼的许多有机配合物是电致发光材料,已知配合物
 具有MLCT发射性质,该配合物中,与N原子直接相连的苯环上的C原子的杂化类型为
具有MLCT发射性质,该配合物中,与N原子直接相连的苯环上的C原子的杂化类型为(5)已知金属Re的一种晶胞结构如图所示,则该晶胞与Mg的堆积方式相同为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】铁元素在工业生产中有重要的作用。回答下列问题:
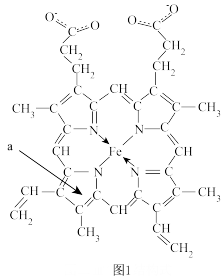
I.血红素(结构如图1)是血红蛋白的活性部位,其中心元素是Fe(II)。
(1)基态 的价电子轨道表示式为:
的价电子轨道表示式为:_______ 。
(2)血红素分子中Fe、N、O三种元素第一电离能由大到小的顺序是_______ (用元素符号表示)。
(3)图1中a环为平面结构,该环大 键可表示为
键可表示为_______ 。(大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数)
键的电子数)
II.铁离子可与EDTA(结构如图2)络合。
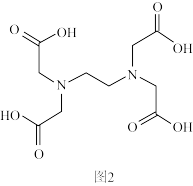
(4)EDTA中C原子杂化类型为_______ 。
(5)已知:一个配位体含有几个能提供孤电子对的原子就叫几齿配位体,则EDTA是_______ 齿配位体(羰炭基中的氧原子不能提供孤对电子)。
III.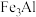 晶体的晶胞结构如图3所示,该晶胞为立方晶胞,其中黑球均在晶胞体内,晶胞参数为apm。
晶体的晶胞结构如图3所示,该晶胞为立方晶胞,其中黑球均在晶胞体内,晶胞参数为apm。
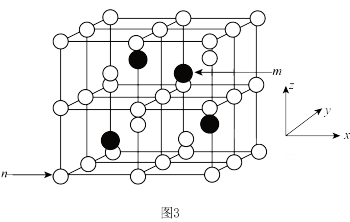
(6)以晶胞参数为单位长度建立坐标系可表示各原子的位置。若n原子分数坐标为 ,则m原子分数坐标为
,则m原子分数坐标为_______ ;若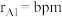 ,
,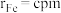 ,则该晶胞的空间利用率为
,则该晶胞的空间利用率为_______ (以含 的代数式表示)。
的代数式表示)。
I.血红素(结构如图1)是血红蛋白的活性部位,其中心元素是Fe(II)。

(1)基态
 的价电子轨道表示式为:
的价电子轨道表示式为:(2)血红素分子中Fe、N、O三种元素第一电离能由大到小的顺序是
(3)图1中a环为平面结构,该环大
 键可表示为
键可表示为 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数)
键的电子数) II.铁离子可与EDTA(结构如图2)络合。

(4)EDTA中C原子杂化类型为
(5)已知:一个配位体含有几个能提供孤电子对的原子就叫几齿配位体,则EDTA是
III.
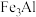 晶体的晶胞结构如图3所示,该晶胞为立方晶胞,其中黑球均在晶胞体内,晶胞参数为apm。
晶体的晶胞结构如图3所示,该晶胞为立方晶胞,其中黑球均在晶胞体内,晶胞参数为apm。
(6)以晶胞参数为单位长度建立坐标系可表示各原子的位置。若n原子分数坐标为
 ,则m原子分数坐标为
,则m原子分数坐标为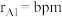 ,
,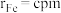 ,则该晶胞的空间利用率为
,则该晶胞的空间利用率为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁元素被称为“人类第一元素”,铁及其化合物具有广泛的应用,回答下列问题:
(1)铁元素在元素周期表第四周期第___________ 列,属于___________ 区元素,基态铁原子M层的电子排布式为___________ 。
(2)铁形成的常见离子有Fe2+和Fe3+,Fe2+易被氧化为Fe3+,请利用核外电子排布的相关原理解释其原因___________ 。
(3)检验 Fe2+是否被氧化为Fe3+的方法之一是:取待测液,加入KSCN溶液,观察是否有红色的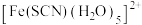 生成。
生成。
①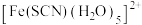 中Fe3+的杂化轨道类型为
中Fe3+的杂化轨道类型为___________ (填字母)。
A. B.
B.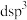 C.
C. D.
D.
②配体SCN-和H2O的键角大小:SCN-___________ H2O (填“<”“>”或“=”。用杂化轨道理论解释,其原因为___________ 。
③SCN-中所有原子均满足最外层8电子结构。写出SCN-的电子式___________ 。
(4)铁酸钇是一种典型的单相多铁性材料,其正交晶胞结构如图a所示,沿x轴与z轴的投影图分别如图b和图c所示。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的相对位置,称作原子坐标。如1号原子的坐标为 ,2号原子的坐标为
,2号原子的坐标为 ,则3号Fe原子的坐标为
,则3号Fe原子的坐标为___________ 。
②若晶胞参数分别为apm、bpm、cpm,阿伏加德罗常数的值为NA,则晶体的密度为___________ g∙cm-3 (列出计算表达式)。
(1)铁元素在元素周期表第四周期第
(2)铁形成的常见离子有Fe2+和Fe3+,Fe2+易被氧化为Fe3+,请利用核外电子排布的相关原理解释其原因
(3)检验 Fe2+是否被氧化为Fe3+的方法之一是:取待测液,加入KSCN溶液,观察是否有红色的
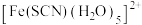 生成。
生成。①
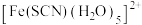 中Fe3+的杂化轨道类型为
中Fe3+的杂化轨道类型为A.
 B.
B.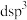 C.
C. D.
D.
②配体SCN-和H2O的键角大小:SCN-
③SCN-中所有原子均满足最外层8电子结构。写出SCN-的电子式
(4)铁酸钇是一种典型的单相多铁性材料,其正交晶胞结构如图a所示,沿x轴与z轴的投影图分别如图b和图c所示。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的相对位置,称作原子坐标。如1号原子的坐标为
 ,2号原子的坐标为
,2号原子的坐标为 ,则3号Fe原子的坐标为
,则3号Fe原子的坐标为②若晶胞参数分别为apm、bpm、cpm,阿伏加德罗常数的值为NA,则晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻.能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____ 、_____ (填标号)。
A.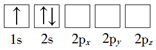 B.
B.
C.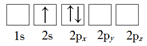 D.
D.
(2)Li+与H−具有相同的电子构型,r(Li+)小于r(H−),原因是_______ 。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的[AlH4]—的空间构型是_____
(4)Li2O是离子晶体,其晶格能可通过图(a)的Born−Haber循环计算得到。

可知,Li原子的第一电离能为________ kJ·mol−1,O=O键键能为______ kJ·mol−1,Li2O晶格能为______ kJ·mol−1。
(5)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为______ g·cm−3(列出计算式)。
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(2)Li+与H−具有相同的电子构型,r(Li+)小于r(H−),原因是
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的[AlH4]—的空间构型是
(4)Li2O是离子晶体,其晶格能可通过图(a)的Born−Haber循环计算得到。

可知,Li原子的第一电离能为
(5)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为
您最近一年使用:0次



