NH4Al(SO4)2是常见的焙烤食品添加剂;NH4HSO4在医药、电子工业中用途广泛。请回答下列问题:
(1)相同条件下,0.1mol/L NH4Al(SO4)2中c(NH4+)________ (填“等于”“大于”或“小于”) 0.1mol/L NH4HSO4中c(NH4+)。
0.1mol/L NH4Al(SO4)2溶液的pH随温度变化的曲线如图甲所示:
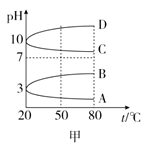
(2)图甲中符合0.1mol/L NH4Al(SO4)2的pH随温度变化的曲线是________ (填字母)。
(3)向100mL 0.1mol/L NH4Al(SO4)2溶液中滴入90ml 0.5mol/L NaOH溶液,产生白色沉淀__________ 克。
(4)写出NH4HSO4溶液中滴加足量NaOH溶液的化学方程式______________________________ ;
25℃时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图乙所示。
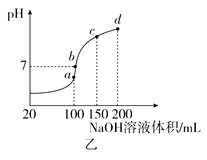
(5)试分析图乙中a、b、c、d四个点,水的电离程度最大的是__________ 。
(1)相同条件下,0.1mol/L NH4Al(SO4)2中c(NH4+)
0.1mol/L NH4Al(SO4)2溶液的pH随温度变化的曲线如图甲所示:

(2)图甲中符合0.1mol/L NH4Al(SO4)2的pH随温度变化的曲线是
(3)向100mL 0.1mol/L NH4Al(SO4)2溶液中滴入90ml 0.5mol/L NaOH溶液,产生白色沉淀
(4)写出NH4HSO4溶液中滴加足量NaOH溶液的化学方程式
25℃时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图乙所示。

(5)试分析图乙中a、b、c、d四个点,水的电离程度最大的是
更新时间:2018/06/06 11:46:15
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】I.水在25℃和95℃时电离平衡曲线如图。
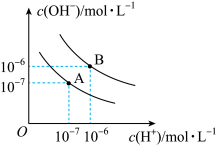
(1)25℃时水的电离平衡曲线应为_______ (“A”或“B”)。25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为_______ 。
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性;则a与b之间应满足的关系是_______ 。
II.醋酸钠一种常见的强碱弱酸盐
(3)醋酸钠在水溶液中水解的离子方程式:_______ 。
(4)将物质的量浓度相同的盐酸与氨水混合后,溶液中的呈中性,则盐酸的体积_______ 氨水的体积(填“>”“<””或“=”)。
(5)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后,CH3COONa溶液的pH_______ NaOH溶液的pH(填“>”“<””或“=”)。

(1)25℃时水的电离平衡曲线应为
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性;则a与b之间应满足的关系是
II.醋酸钠一种常见的强碱弱酸盐
(3)醋酸钠在水溶液中水解的离子方程式:
(4)将物质的量浓度相同的盐酸与氨水混合后,溶液中的呈中性,则盐酸的体积
(5)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后,CH3COONa溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】勒夏特列原理适用于许多平衡体系。试用该原理分析水的电离平衡(H2O H++OH-),填写下列表格
H++OH-),填写下列表格
 H++OH-),填写下列表格
H++OH-),填写下列表格| 改变条件 | 平衡移动方向 | c(H+)的变化 | c(OH-)的变化 | Kw |
| 加入醋酸 | ||||
| 加入烧碱 | ||||
| 升高温度 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列物质中:①醋酸溶液②氨水③熔融的NaOH④稀盐酸⑤Na2CO3固体⑥NaHSO4固体⑦CH3COONa溶液⑧Ba(OH)2固体。
(1)上述物质中属于强电解质的是_____ (填序号)。
(2)写出⑥分别在水溶液和熔融状态下的电离方程式:
水溶液中:_____ ;熔融状态下:_____ 。
(3)25℃时,将⑤的溶液和⑥的溶液等浓度、等体积混合,混合溶液中:c(Na+)+c(H+)-c(SO )
)_____ (填“>”、“<”或“=”)c(HCO )+c(CO
)+c(CO )+c(OH-)。25℃时,将V1Lcmol•L-1②V2Lcmol•L-1加入④中,当V1=V2时,混合溶液中离子浓度大小顺序为
)+c(OH-)。25℃时,将V1Lcmol•L-1②V2Lcmol•L-1加入④中,当V1=V2时,混合溶液中离子浓度大小顺序为_____ (填离子符号)。
(4)25℃时,0.1mol•L-1的⑤的溶液、⑥的溶液、⑧的溶液和⑦四种溶液的pH由大到小的排列顺序:______ (填标号,下同)。
(5)25℃时,将等pH、VL的②和⑧的溶液分别稀释至2VL,则稀释后溶液的pH大小关系为_____ 。
(1)上述物质中属于强电解质的是
(2)写出⑥分别在水溶液和熔融状态下的电离方程式:
水溶液中:
(3)25℃时,将⑤的溶液和⑥的溶液等浓度、等体积混合,混合溶液中:c(Na+)+c(H+)-c(SO
 )
) )+c(CO
)+c(CO )+c(OH-)。25℃时,将V1Lcmol•L-1②V2Lcmol•L-1加入④中,当V1=V2时,混合溶液中离子浓度大小顺序为
)+c(OH-)。25℃时,将V1Lcmol•L-1②V2Lcmol•L-1加入④中,当V1=V2时,混合溶液中离子浓度大小顺序为(4)25℃时,0.1mol•L-1的⑤的溶液、⑥的溶液、⑧的溶液和⑦四种溶液的pH由大到小的排列顺序:
(5)25℃时,将等pH、VL的②和⑧的溶液分别稀释至2VL,则稀释后溶液的pH大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列方程式
(1)完成下列物质的电离方程式
①NaHSO4(在水溶液中):___________
②)H2S:___________
(2)完成下列物质的化学方程式
①钠与水反应:___________
②铁与水蒸气反应:___________
③二氧化氮与水的反应:___________
④碳酸氢钠受热分解的反应:___________
(3)完成下列物质的水解离子方程式
①Al2(SO4)3:___________
②Na2CO3(两步):___________
(4)配平下列化学方程式
①___________ :_____KNO3+______FeCl2+_______HCl—______KCl+_______FeCl3+______NO↑+_______H2O
②___________ :_______ClO-+______Fe(OH)3+_______OH-—_____Cl-+______FeO +______H2O
+______H2O
(1)完成下列物质的电离方程式
①NaHSO4(在水溶液中):
②)H2S:
(2)完成下列物质的化学方程式
①钠与水反应:
②铁与水蒸气反应:
③二氧化氮与水的反应:
④碳酸氢钠受热分解的反应:
(3)完成下列物质的水解离子方程式
①Al2(SO4)3:
②Na2CO3(两步):
(4)配平下列化学方程式
①
②
 +______H2O
+______H2O
您最近一年使用:0次

 2SO3(g) ΔH <0,写出该反应的化学平衡常数表达式K=
2SO3(g) ΔH <0,写出该反应的化学平衡常数表达式K=

