己二酸主要用于生产尼龙66盐、合成树脂及增塑剂等。己二酸的合成路线如下:
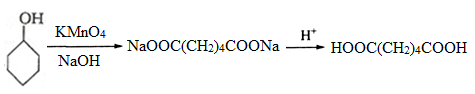
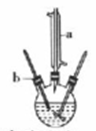
制备己二酸的装置示意图如图所示(加热和夹持装置等略)。
实验步骤:
I.己二酸的制备
连装好装置后,通过瓶口b慢慢滴加1.5g环己醇至适量KMnO4和NaOH的混合溶液中,然后塞上带有温度计的胶塞,再用沸水浴加热数分钟。
II.分离提纯
趁热过滤,收集滤液,用少量热水洗涤滤渣2次,合并滤液和洗涤液,边搅拌边滴加浓盐酸至溶液呈强酸性,小心加热蒸发浓缩至10mL左右,在冷水浴中冷却,析出己二酸粗品。
回答下列问题:
(1)写出仪器a的名称:______________ 。
(2)分离提纯过程中滴加的浓盐酸的作用是______________ 。
(3)将己二酸粗品提纯的方法是_______________ 。
A.过滤 B.萃取 C.重结晶 D.蒸馏
(4)步骤II中过滤时需要用到的玻璃仪器有玻璃棒____ 、_____ 。洗涤滤渣的目的是__________ 。
(5)若制得纯己二酸的质量为1.5g,则己二酸的产率为__________ 。
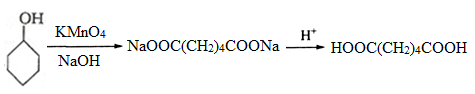
制备己二酸的装置示意图如图所示(加热和夹持装置等略)。

实验步骤:
I.己二酸的制备
连装好装置后,通过瓶口b慢慢滴加1.5g环己醇至适量KMnO4和NaOH的混合溶液中,然后塞上带有温度计的胶塞,再用沸水浴加热数分钟。
II.分离提纯
趁热过滤,收集滤液,用少量热水洗涤滤渣2次,合并滤液和洗涤液,边搅拌边滴加浓盐酸至溶液呈强酸性,小心加热蒸发浓缩至10mL左右,在冷水浴中冷却,析出己二酸粗品。
回答下列问题:
(1)写出仪器a的名称:
(2)分离提纯过程中滴加的浓盐酸的作用是
(3)将己二酸粗品提纯的方法是
A.过滤 B.萃取 C.重结晶 D.蒸馏
(4)步骤II中过滤时需要用到的玻璃仪器有玻璃棒
(5)若制得纯己二酸的质量为1.5g,则己二酸的产率为
更新时间:2018-06-22 15:11:48
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室常用环己醇脱水合成环己烯。实验装置图和有关实验数据如下。
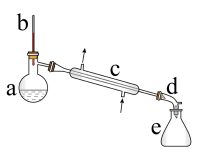
合成反应:在a中加入20g环己醇,冷却搅动下慢慢加入1mL浓硫酸。c中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。当烧瓶中只剩下很少量的残渣并出现阵阵白雾时停止蒸馏。
分离提纯:将e中粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,蒸馏,收集82~85℃范围内的馏分,得到纯净环己烯12.0g。
(1)仪器e的名称为___________ ,实验中加入 的作用是
的作用是___________ ;
(2)合成时,若加热后发现未加沸石,应如何补救___________ ,实验中最容易产生的副产物结构简式为___________ ;
(3)该合成反应的化学方程式是___________ ;
(4)合成反应中,控制馏出物的温度不超过90℃的目的是___________ ;
(5)本实验所制得的环己烯的产率为___________ (保留三位有效数字)。
| 相对分子质量 | 密度/( ) ) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |

合成反应:在a中加入20g环己醇,冷却搅动下慢慢加入1mL浓硫酸。c中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。当烧瓶中只剩下很少量的残渣并出现阵阵白雾时停止蒸馏。
分离提纯:将e中粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,蒸馏,收集82~85℃范围内的馏分,得到纯净环己烯12.0g。
(1)仪器e的名称为
 的作用是
的作用是(2)合成时,若加热后发现未加沸石,应如何补救
(3)该合成反应的化学方程式是
(4)合成反应中,控制馏出物的温度不超过90℃的目的是
(5)本实验所制得的环己烯的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】酯类是工业上重要的有机原料,具有广泛用途。乙酸苯甲酯 对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业。乙酸苯甲酯的合成路线如下:
对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业。乙酸苯甲酯的合成路线如下:

已知:R-Cl R-OH,R-为烃基
R-OH,R-为烃基
(1)乙酸苯甲酯的分子式是________ ,B所含官能团的名称是________ 。
(2)写出反应③的化学反应方程式:________ 。反应①的反应类型是__________ ,反应③的反应类型是________________ 。
(3)下列转化中________ (填序号)原子的理论利用率为100%,符合绿色化学的要求。
A.乙醇制取乙醛 B.由 制备
制备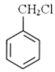 C.2CH3CHO+O2
C.2CH3CHO+O2 2A
2A
(4)提纯乙酸苯甲酯的有关实验步骤如下:将反应液冷至室温后倒入分液漏斗中,分别用饱和碳酸钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏,收集馏分,得到乙酸苯甲酯。
回答下列问题:
①在洗涤、分液操作中。应充分振荡,然后静置,待分层后________ (填标号)。
a.直接将乙酸苯甲酯从分液漏斗上口倒出
b.直按将乙酸苯甲酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸苯甲酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸苯甲酯从上口放出
②实验中加入少量无水MgSO4的目的是__________________ 。
③在蒸馏操作中,仪器选择及安装都正确的是____________ (填标号)。

(注:箭头方向表示水流方向)
 对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业。乙酸苯甲酯的合成路线如下:
对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业。乙酸苯甲酯的合成路线如下:
已知:R-Cl
 R-OH,R-为烃基
R-OH,R-为烃基(1)乙酸苯甲酯的分子式是
(2)写出反应③的化学反应方程式:
(3)下列转化中
A.乙醇制取乙醛 B.由
 制备
制备 C.2CH3CHO+O2
C.2CH3CHO+O2 2A
2A(4)提纯乙酸苯甲酯的有关实验步骤如下:将反应液冷至室温后倒入分液漏斗中,分别用饱和碳酸钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏,收集馏分,得到乙酸苯甲酯。
回答下列问题:
①在洗涤、分液操作中。应充分振荡,然后静置,待分层后
a.直接将乙酸苯甲酯从分液漏斗上口倒出
b.直按将乙酸苯甲酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸苯甲酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸苯甲酯从上口放出
②实验中加入少量无水MgSO4的目的是
③在蒸馏操作中,仪器选择及安装都正确的是

(注:箭头方向表示水流方向)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】亚氯酸钠(NaClO2)是一种应用广泛的高效氧化型漂白剂。以下是某小组模拟工业制法利用ClO2与H2O2在碱性条件下制备少量NaClO2的实验装置:

已知:
①硫酸作酸化剂时,甲醇(CH3OH)可将NaClO3还原为ClO2。
②ClO2沸点为9.9℃,可溶于水,有毒,气体中ClO2浓度较高时易发生爆炸。
③饱和NaClO2溶液在温度低于38℃时析出晶体NaClO2•3H2O,在温度高于38℃时析出晶体NaClO2,高于60℃时分解生成NaClO3和NaCl。
回答下列问题:
(1)实验前用浓硫酸与50%甲醇溶液配制混合溶液的操作是:___________ 。
(2)装置A中,若氧化产物为CO2,则氧化剂与还原剂的物质的量之比为___________ 。
(3)装置B中生成NaClO2的化学方程式是___________ 。
(4)装置C中ClO2与NaOH溶液反应生成等物质的量的两种钠盐,其中一种为NaClO2,装置C中ClO2与NaOH溶液反应的离子方程式是___________
(5)从反应后的B溶液中制得NaClO2晶体的操作步骤是:a.控制在38~60℃之间蒸发浓缩;b.___________ ;c.用38~60℃的热水洗涤;d.在低于60oC的真空中蒸发,干燥。
(6)NaClO2纯度测定:①称取所得NaClO2样品1.000g于烧杯中,加入适量蒸馏水与过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(C1O 的还原产物为Cl-),将所得混合液配成250mL待测溶液;②取25.00mL待测液,用0.2000mol/LNa2S2O3标准液滴定(I2+2S2O
的还原产物为Cl-),将所得混合液配成250mL待测溶液;②取25.00mL待测液,用0.2000mol/LNa2S2O3标准液滴定(I2+2S2O =2I-+S4O
=2I-+S4O ),以淀粉溶液做指示剂重复滴定3次,测得Na2S2O3标准液平均用量为18.00mL,则该样品中NaClO2的质量分数为
),以淀粉溶液做指示剂重复滴定3次,测得Na2S2O3标准液平均用量为18.00mL,则该样品中NaClO2的质量分数为___________ 。

已知:
①硫酸作酸化剂时,甲醇(CH3OH)可将NaClO3还原为ClO2。
②ClO2沸点为9.9℃,可溶于水,有毒,气体中ClO2浓度较高时易发生爆炸。
③饱和NaClO2溶液在温度低于38℃时析出晶体NaClO2•3H2O,在温度高于38℃时析出晶体NaClO2,高于60℃时分解生成NaClO3和NaCl。
回答下列问题:
(1)实验前用浓硫酸与50%甲醇溶液配制混合溶液的操作是:
(2)装置A中,若氧化产物为CO2,则氧化剂与还原剂的物质的量之比为
(3)装置B中生成NaClO2的化学方程式是
(4)装置C中ClO2与NaOH溶液反应生成等物质的量的两种钠盐,其中一种为NaClO2,装置C中ClO2与NaOH溶液反应的离子方程式是
(5)从反应后的B溶液中制得NaClO2晶体的操作步骤是:a.控制在38~60℃之间蒸发浓缩;b.
(6)NaClO2纯度测定:①称取所得NaClO2样品1.000g于烧杯中,加入适量蒸馏水与过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(C1O
 的还原产物为Cl-),将所得混合液配成250mL待测溶液;②取25.00mL待测液,用0.2000mol/LNa2S2O3标准液滴定(I2+2S2O
的还原产物为Cl-),将所得混合液配成250mL待测溶液;②取25.00mL待测液,用0.2000mol/LNa2S2O3标准液滴定(I2+2S2O =2I-+S4O
=2I-+S4O ),以淀粉溶液做指示剂重复滴定3次,测得Na2S2O3标准液平均用量为18.00mL,则该样品中NaClO2的质量分数为
),以淀粉溶液做指示剂重复滴定3次,测得Na2S2O3标准液平均用量为18.00mL,则该样品中NaClO2的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
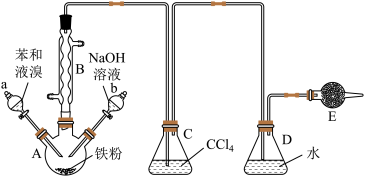
【推荐2】用浓盐酸与氯酸钾固体反应制氯气时,发现所得气体颜色偏深,经分析该气体主要含有Cl2和ClO2两种气体,某研究性学习小组拟用如图所示装置分离制得的混合气体,并测定两种气体的物质的量之比。
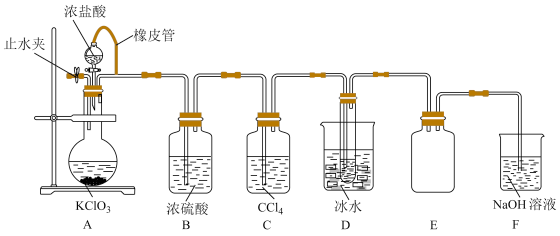
Ⅰ.查阅资料:
常温下二氧化氯为黄绿色气体,其熔点为-59.5℃,沸点为11.0℃,能溶于水,不溶于浓硫酸、四氯化碳,有强氧化性,能与NaOH溶液反应生成等物质的量的两种盐,其中一种为NaClO3。
Ⅱ.制备与分离:
(1)实验加药品前应进行的实验操作是____________ 。
(2)装置C、E的作用分别是_________ 、_________ 。
(3)F中ClO2与NaOH溶液反应的离子方程式为_____________ 。
Ⅲ.测量与计算:
反应结束后,测得B、C装置分别增重2.0g和14 .2g,将D中的液体溶于水,配成2.5 L溶液,取25.00 mL该溶液,调节试样的pH﹤2.0,加入足量的KI晶体,振荡后,静置片刻;加入指示剂X,用0.200mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液25.00 mL。(已知:2ClO2+8H++10I-===5I2+2Cl-+4H2O;2Na2S2O3+I2===Na2S4O6+2NaI)
(4)指示剂X为_____ ,滴定终点时的现象是_______________ 。
(5)原装置收集到的ClO2物质的量为___________ 。
Ⅳ.结论:
(6)浓盐酸与氯酸钾固体反应的化学方程式为____________ 。

Ⅰ.查阅资料:
常温下二氧化氯为黄绿色气体,其熔点为-59.5℃,沸点为11.0℃,能溶于水,不溶于浓硫酸、四氯化碳,有强氧化性,能与NaOH溶液反应生成等物质的量的两种盐,其中一种为NaClO3。
Ⅱ.制备与分离:
(1)实验加药品前应进行的实验操作是
(2)装置C、E的作用分别是
(3)F中ClO2与NaOH溶液反应的离子方程式为
Ⅲ.测量与计算:
反应结束后,测得B、C装置分别增重2.0g和14 .2g,将D中的液体溶于水,配成2.5 L溶液,取25.00 mL该溶液,调节试样的pH﹤2.0,加入足量的KI晶体,振荡后,静置片刻;加入指示剂X,用0.200mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液25.00 mL。(已知:2ClO2+8H++10I-===5I2+2Cl-+4H2O;2Na2S2O3+I2===Na2S4O6+2NaI)
(4)指示剂X为
(5)原装置收集到的ClO2物质的量为
Ⅳ.结论:
(6)浓盐酸与氯酸钾固体反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】羟基乙酸钠(HOCH2COONa)是有机合成的中间体,易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。实验室拟用氯乙酸和 NaOH 溶液制备少量羟基乙酸钠(已知此反应剧烈,且为放热反应),实验装置如图。
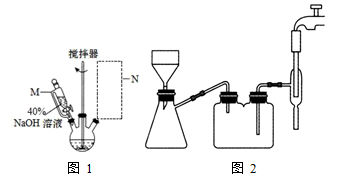
实验步骤:
步骤 l:向如图 1 所示装置(夹持和加热仪器略)三颈烧瓶中加入56.7g 氯乙酸、50mL水,搅拌。缓缓加入足量 40%NaOH 溶液,在 95℃继续搅拌反应 2 小时,反应过程中控制 pH 为 9~10。
步骤 2:取三颈烧瓶中液体,蒸发至液面有晶膜,加少量热水,进行操作Ⅰ。滤液冷却至15℃,过滤得粗产品。
步骤 3:将粗产品溶解于适量热水中,加活性炭脱色,并分离掉活性炭。
步骤 4:将去除活性炭后的溶液加到适量乙醇中,经操作Ⅱ、抽滤、干燥等,得羟基乙酸钠。
回答下列问题:
(1)仪器 M 的名称为___________ 。步骤 1 中,采用的加热方式为 ___________ , 发生反应的化学方程式为___________ 。
(2)N 处仪器作用为___________ ,使用正确且效果最好的是___________ (填标号)。
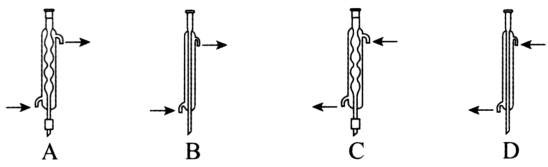
(3)加入 40%NaOH 溶液时,需“缓缓”加入的目的是___________ 、 ___________ 。
(4)上述步骤中,操作Ⅰ、Ⅱ的名称分别是___________ 、 ___________ 。
(5)上述步骤4中,加入乙醇的目的为___________ ; 抽滤(图 2)时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是 ___________ 。
(6)步骤4中,得纯净羟基乙酸钠 44.1g,则实验产率为___________ 。

实验步骤:
步骤 l:向如图 1 所示装置(夹持和加热仪器略)三颈烧瓶中加入56.7g 氯乙酸、50mL水,搅拌。缓缓加入足量 40%NaOH 溶液,在 95℃继续搅拌反应 2 小时,反应过程中控制 pH 为 9~10。
步骤 2:取三颈烧瓶中液体,蒸发至液面有晶膜,加少量热水,进行操作Ⅰ。滤液冷却至15℃,过滤得粗产品。
步骤 3:将粗产品溶解于适量热水中,加活性炭脱色,并分离掉活性炭。
步骤 4:将去除活性炭后的溶液加到适量乙醇中,经操作Ⅱ、抽滤、干燥等,得羟基乙酸钠。
回答下列问题:
(1)仪器 M 的名称为
(2)N 处仪器作用为

(3)加入 40%NaOH 溶液时,需“缓缓”加入的目的是
(4)上述步骤中,操作Ⅰ、Ⅱ的名称分别是
(5)上述步骤4中,加入乙醇的目的为
(6)步骤4中,得纯净羟基乙酸钠 44.1g,则实验产率为
您最近一年使用:0次